解答题-原理综合题 适中0.65 引用1 组卷131
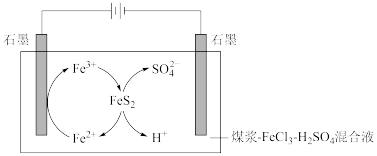
电化学原理被广泛应用于生产、生活的许多方面,利用电解法脱除煤中的含硫物质(主要是 )的原理如图所示。
)的原理如图所示。
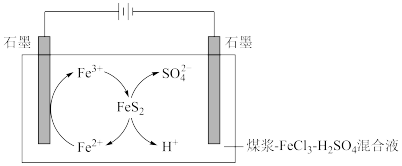
(1)阴极石墨棒上有无色气体产生,该气体是_______ 。
(2)阳极的电极反应式为_______ 。
(3)补全脱硫反应方程式:_______ 。
(4)相同反应时间, 对脱硫率的影响如图所示。
对脱硫率的影响如图所示。
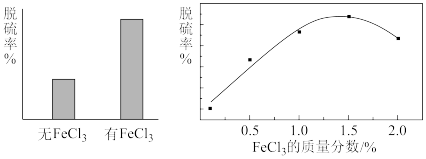
①电解脱硫过程中, 的作用是催化剂,结合简单碰撞理论说明使用
的作用是催化剂,结合简单碰撞理论说明使用 能加快反应速率的原因
能加快反应速率的原因_______ 。
② 的质量分数大于1.5%时,脱硫率随
的质量分数大于1.5%时,脱硫率随 浓度的增大而下降,解释原因
浓度的增大而下降,解释原因_______ 。
(5)研究发现,电解时若电压过高,阳极有副反应发生,造成电解效率降低。电解效率 的定义:
的定义: ,某电压下电解100mL煤浆-
,某电压下电解100mL煤浆- -
- 混合液,煤浆中除
混合液,煤浆中除 外不含其它含硫物质,混合液中
外不含其它含硫物质,混合液中 浓度为
浓度为 ,
, 的质量分数为1.5%。当阴极收集到224mL(标准状况)气体时(阴极无副反应发生),测得溶液中
的质量分数为1.5%。当阴极收集到224mL(标准状况)气体时(阴极无副反应发生),测得溶液中 ,
,
_______ (忽略电解前后溶液的体积变化)。
(6)综上,电解法脱硫的优点有_______ (写出两点)。

(1)阴极石墨棒上有无色气体产生,该气体是
(2)阳极的电极反应式为
(3)补全脱硫反应方程式:
(4)相同反应时间,

①电解脱硫过程中,
②
(5)研究发现,电解时若电压过高,阳极有副反应发生,造成电解效率降低。电解效率
(6)综上,电解法脱硫的优点有
21-22高三下·北京朝阳·阶段练习
类题推荐
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网
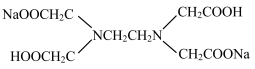 )溶液中,每个H2Y2-电离出2个H+生成酸根Y4-,然后与Fe3+配位。已知该配位反应受溶液pH的影响,若溶液pH太低或太高,分别存在的问题是
)溶液中,每个H2Y2-电离出2个H+生成酸根Y4-,然后与Fe3+配位。已知该配位反应受溶液pH的影响,若溶液pH太低或太高,分别存在的问题是