单选题 较易0.85 引用2 组卷352
电解法处理酸性含铬废水(主要含有Cr2O )时,以铁板作阴、阳极,处理过程中存在反应Cr2O
)时,以铁板作阴、阳极,处理过程中存在反应Cr2O +6Fe2++14H+=2Cr3++6Fe3++7H2O,最后Cr3+以Cr(OH)3形式除去。下列说法正确的是
+6Fe2++14H+=2Cr3++6Fe3++7H2O,最后Cr3+以Cr(OH)3形式除去。下列说法正确的是
| A.阴极反应为Fe-3e-=Fe3+ |
| B.电解过程中溶液pH不会变化 |
| C.电路中每转移6mol电子,最多有1molCr2O |
| D.过程中有Fe(OH)3沉淀生成 |
2022·黑龙江哈尔滨·模拟预测
类题推荐
还原沉淀法是处理含铬(含Cr2O72-和CrO42-)工业废水的常用方法,过程如下:
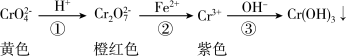
已知:转化过程中的反应为2CrO42-(aq)+2H+(aq) Cr2O72-(aq)+H2O(l)。常温下Ksp[Cr(OH)3]=1×10-32。下列说法错误的是( )
Cr2O72-(aq)+H2O(l)。常温下Ksp[Cr(OH)3]=1×10-32。下列说法错误的是( )

已知:转化过程中的反应为2CrO42-(aq)+2H+(aq)
 Cr2O72-(aq)+H2O(l)。常温下Ksp[Cr(OH)3]=1×10-32。下列说法错误的是( )
Cr2O72-(aq)+H2O(l)。常温下Ksp[Cr(OH)3]=1×10-32。下列说法错误的是( )| A.反应①v正(CrO42-)=2v逆(Cr2O72-)时,反应处于平衡状态 |
| B.反应②转移0.6mole-,则有0.2mol Cr2O72-被还原 |
| C.除去废水中含铬离子的过程包括氧化还原反应和复分解反应 |
| D.常温下,要使处理后废水中的c(Cr3+)降至1×10-5mol·L-1,反应③应调溶液pH=5 |
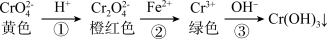
还原沉淀法是处理含铬(含Cr2O 和CrO
和CrO )工业废水的常用方法,过程如下,下列说法错误的是(已知:常温下,Ksp[Cr(OH)3]=1×10-32)
)工业废水的常用方法,过程如下,下列说法错误的是(已知:常温下,Ksp[Cr(OH)3]=1×10-32)

| A.反应①,增大c(H+), |
| B.反应①2v正(CrO |
| C.反应②转移0.6mole-,则有0.1molCr2O |
| D.常温下,要使处理后废水中的c( |
还原沉淀法是处理含铬(Cr2O 和CrO
和CrO )废水常用方法,过程如下:CrO
)废水常用方法,过程如下:CrO
 Cr2O
Cr2O
 Cr3+
Cr3+ Cr(OH)3,已知废水中Cr的含量为26.0g/L,当溶液中离子浓度小于10-5mol/L时认为离子已经沉淀完全,常温下,Ksp[Cr(OH)3]=1×10-32, Ksp(FeS)=6.3×10-18;Ksp(CuS)=1.3×10-36;Ksp(ZnS)=1.6×10-24,有关叙述中不正确的是( )
Cr(OH)3,已知废水中Cr的含量为26.0g/L,当溶液中离子浓度小于10-5mol/L时认为离子已经沉淀完全,常温下,Ksp[Cr(OH)3]=1×10-32, Ksp(FeS)=6.3×10-18;Ksp(CuS)=1.3×10-36;Ksp(ZnS)=1.6×10-24,有关叙述中不正确的是( )
| A.上述三个转化中只有一个涉及氧化还原反应 |
| B.第二步离子方程式为Cr2O |
| C.足量CuSO4溶解在0.1mol/L的H2S溶液中,Cu2+能达到的最大浓度为1.3×10-35mol/L |
| D.在ZnS的饱和溶液中加入FeCl2溶液,一定不产生FeS沉淀 |
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


