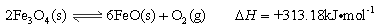解答题-原理综合题 适中0.65 引用1 组卷44
氢能是理想的清洁能源,资源丰富。以太阳能为热源分解 ,经由热化学铁氧化合物循环分解水制
,经由热化学铁氧化合物循环分解水制 的过程如下:
的过程如下:

(1)过程Ⅰ:

①过程Ⅰ需要将 不断分离出去,目的是
不断分离出去,目的是_______ 。
②一定温度下,在容积可变的密闭容器中,该反应已达到平衡。下列说法正确的是_______ (填字母标号)。
a.容器内气体密度和相对分子质量都不再改变b.升高温度,容器内气体密度变大
c.向容器中通入 ,
, 转化率不变d.缩小容器容积,
转化率不变d.缩小容器容积, 浓度变大
浓度变大
(2)已知 的燃烧热是
的燃烧热是 ,则液态水通过过程Ⅱ转化的热化学方程式为
,则液态水通过过程Ⅱ转化的热化学方程式为_______ 。
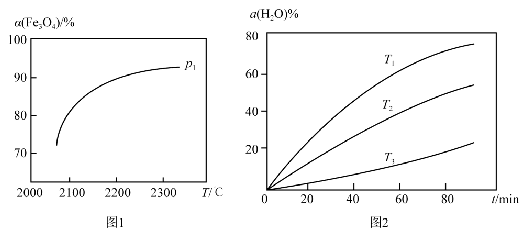
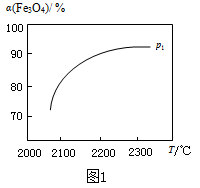
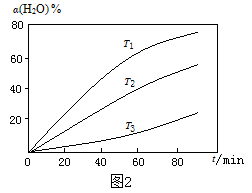
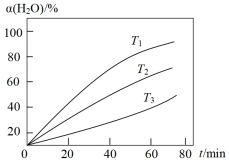
(3)其他条件不变时,过程Ⅱ在不同温度下, 的转化率随时间的变化
的转化率随时间的变化 曲线如图所示,温度
曲线如图所示,温度 、
、 、
、 由大到小的关系是
由大到小的关系是_______ ,判断依据是_______ 。
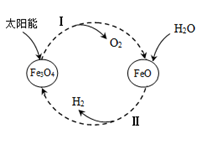
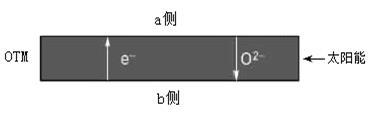
(4)科研人员研制出透氧膜,它允许电子和 同时透过,可实现水连续分解制
同时透过,可实现水连续分解制 ,工作时
,工作时 、
、 分别在透氧膜两侧反应。工作原理如图所示:
分别在透氧膜两侧反应。工作原理如图所示:
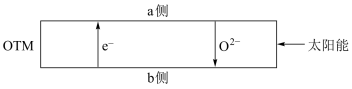
CO在_______ 侧反应(填“a”或“b”),另一侧的电极反应式为_______ 。

(1)过程Ⅰ:
①过程Ⅰ需要将
②一定温度下,在容积可变的密闭容器中,该反应已达到平衡。下列说法正确的是
a.容器内气体密度和相对分子质量都不再改变b.升高温度,容器内气体密度变大
c.向容器中通入
(2)已知
(3)其他条件不变时,过程Ⅱ在不同温度下,

(4)科研人员研制出透氧膜,它允许电子和

CO在
21-22高二下·湖北宜昌·阶段练习
类题推荐
甲烷水汽重整反应是我国主要的制氢技术,有关反应如下:
反应i: ;
;
反应ii: 。
。
回答下列问题:
反应 、反应
、反应 的平衡常数分别为
的平衡常数分别为 、
、 ,反应温度为
,反应温度为 。
。
(1)b_____ (填“<”或“>”)0.
(2)对于反应i, ,
, (
( 、
、 为速率常数,仅与温度有关)。向等压密闭容器中充入
为速率常数,仅与温度有关)。向等压密闭容器中充入 、
、 仅发生反应
仅发生反应 ,达到平衡后生成
,达到平衡后生成 和
和 。下列说法不正确的是_____(填标号)。
。下列说法不正确的是_____(填标号)。
(3)一定温度下,向恒容密闭反应器中通入 和
和 ,起始时
,起始时 和
和 的分压分别为
的分压分别为 、
、 ,发生反应
,发生反应 和反应ii.反应进行
和反应ii.反应进行 时达到平衡状态,此时
时达到平衡状态,此时 、
、 的分压分别为
的分压分别为 、
、 。
。
① 的平衡分压为
的平衡分压为_____  用含
用含 的代数式表示,下同)。
的代数式表示,下同)。
②反应ii的
_____ (用平衡时各物质的分压代替物质的量浓度)。
(4)复合载氧体可以氧化甲烷制取合成气 、
、 ,如图为
,如图为 时载氧体的质量与时间的关系[一定条件下有积碳反应发生,反应iii:
时载氧体的质量与时间的关系[一定条件下有积碳反应发生,反应iii: 或反应iv:
或反应iv: 。
。
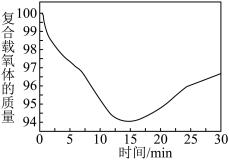
①从开始到 的时候,曲线呈下降趋势的原因主要是甲烷还原载氧体,载氧体失去氧而出现失重的情况;反应在
的时候,曲线呈下降趋势的原因主要是甲烷还原载氧体,载氧体失去氧而出现失重的情况;反应在 时,出现了一个短暂的小平台,其主要的原因是
时,出现了一个短暂的小平台,其主要的原因是_____ 。
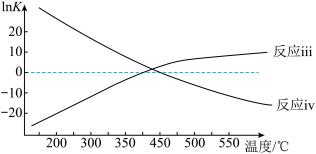
②已知 ,反应iii和反应iv的
,反应iii和反应iv的 与温度的关系如图所示,则
与温度的关系如图所示,则 时,主要发生的积碳反应是
时,主要发生的积碳反应是_____ ,共理由是_____ 。
(5)在混合导体透氧膜反应器中只需一步就可同时制备氨合成气 和液体燃料合成气
和液体燃料合成气 ,其工作原理如图所示。
,其工作原理如图所示。
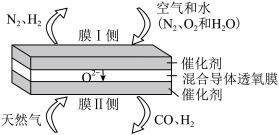
①膜I侧发生的反应为 、
、_____ 。
②膜II侧相当于原电池的_____ 极,膜II侧发生的反应为_____ 。
反应i:
反应ii:
回答下列问题:
反应
(1)b
(2)对于反应i,
| A. |
| B.及时分离出 |
| C.1000°C时,k正一定小于k逆 |
| D.其他条件不变,达平衡后再向容器中充入 |
①
②反应ii的
(4)复合载氧体可以氧化甲烷制取合成气

①从开始到
②已知

(5)在混合导体透氧膜反应器中只需一步就可同时制备氨合成气

①膜I侧发生的反应为
②膜II侧相当于原电池的
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网