解答题-工业流程题 困难0.15 引用1 组卷789
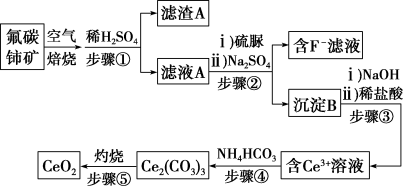
氧化铈(CeO2)是一种应用非常广 泛的稀土氧化物。现以氟碳铺矿(含CeFCO3、BaO、SiO2等)为原料制备氧化铈,其工艺流程如图所示:
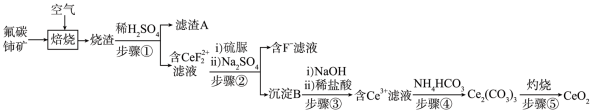
已知:
①稀土离子易与 形成复盐沉淀,Ce3+和
形成复盐沉淀,Ce3+和 发生反应:Ce2(SO4)3+ Na2SO4 +nH2O=Ce2(SO4)3·Na2SO4·nH2O↓;
发生反应:Ce2(SO4)3+ Na2SO4 +nH2O=Ce2(SO4)3·Na2SO4·nH2O↓;
②硫脲: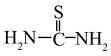 具有还原性,酸性条件下易被氧化为(SCN2H3)2;
具有还原性,酸性条件下易被氧化为(SCN2H3)2;
③Ce3+在空气中易被氧化为Ce4+,两者均能形成氢氧化物沉淀;
④Ce2(CO3)2为白色粉末,难溶于水。
回答下列问题:
(1)滤渣A的主要成分是_______ (填写化学式)。
(2)在另一种生产工艺中,在氟碳铈矿矿石粉中加入碳酸氢钠同时通入氧气焙烧,焙烧得到NaF和CeO2两种固体以及两种高温下的气态物质,请写出焙烧过程中相应的化学方程式_______ 。
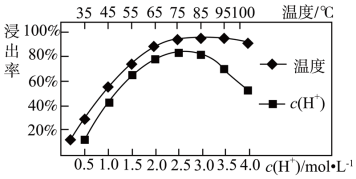
(3)焙烧后加入稀硫酸浸出,Ce的浸出率和稀硫酸浓度、温度有关,其关系如图所示,图示中H+浓度大于2.5mol·L-1时,浸出率降低的原因是_______ 。
(4)加入硫脲的目的是将 还原为Ce3+,反应的 离子方程式为
还原为Ce3+,反应的 离子方程式为_______ 。
(5)步骤③加入盐酸后,通常还需加入另一种化学试剂X,根据题中信息推测,加入X的作用为_______ 。
(6)下列关于步骤④的说法错误的是_______ (填字 母)。
(7)取所得产品CeO2 8.00g溶解后配成250mL溶液。取25.00 mL该溶液用0.20 mol·L-1硫酸亚铁铵[(NH4)2Fe(SO4)2]溶液滴定,滴定时发生反应Fe2++Ce4+=Fe3+ +Ce3+,达到滴定终点时消耗硫酸亚铁铵溶液20.50mL,则该产品的纯度为_______ 。(保留两位小数)。

已知:
①稀土离子易与
②硫脲:
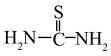 具有还原性,酸性条件下易被氧化为(SCN2H3)2;
具有还原性,酸性条件下易被氧化为(SCN2H3)2;③Ce3+在空气中易被氧化为Ce4+,两者均能形成氢氧化物沉淀;
④Ce2(CO3)2为白色粉末,难溶于水。
回答下列问题:
(1)滤渣A的主要成分是
(2)在另一种生产工艺中,在氟碳铈矿矿石粉中加入碳酸氢钠同时通入氧气焙烧,焙烧得到NaF和CeO2两种固体以及两种高温下的气态物质,请写出焙烧过程中相应的化学方程式
(3)焙烧后加入稀硫酸浸出,Ce的浸出率和稀硫酸浓度、温度有关,其关系如图所示,图示中H+浓度大于2.5mol·L-1时,浸出率降低的原因是

(4)加入硫脲的目的是将
(5)步骤③加入盐酸后,通常还需加入另一种化学试剂X,根据题中信息推测,加入X的作用为
(6)下列关于步骤④的说法错误的是_______ (填字 母)。
| A.该步骤发生的反应是2Ce3+ +6 |
| B.可以用(NH4)2CO3溶液代替NH4 HCO3溶液,不影响产品纯度 |
| C.过滤时选择减压过滤能够大大提高过滤效率 |
| D.过滤后的滤液中仍含有较多Ce3+,需要将滤液循环以提高产率 |
2022·河南·二模
类题推荐
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网

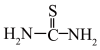 具有还原性,酸性条件下易被氧化为
具有还原性,酸性条件下易被氧化为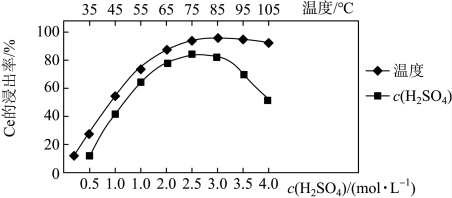
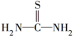 酸性条件下易被氧化为(SCN2H3)2;
酸性条件下易被氧化为(SCN2H3)2;

 ,酸性条件下易被氧化为(SCN2H3)2;
,酸性条件下易被氧化为(SCN2H3)2;


