解答题-工业流程题 较难0.4 引用1 组卷195
锌是一种应用广泛的金属。一种以闪锌矿(主要成分为ZnS,还含有SiO2和少量FeS、CdS、PbS杂质)为原料制备金属锌的流程如图所示:
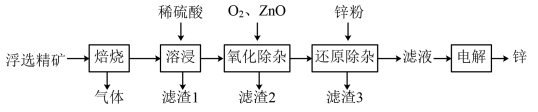
相关金属离子[c(Mn+)=0.1mol·L-1]形成氢氧化物沉淀的pH范围如表:
回答下列问题:
(1)焙烧过程中主要反应的化学方程式为____ 。
(2)滤渣1的主要成分除SiO2外还有____ 。
(3)氧化除杂工序中通入氧气的作用是____ ,ZnO的作用是____ 。
(4)溶液中的Cd2+可用锌粉除去,还原除杂工序中反应的离子方程式为____ 。为什么不能省去“还原除杂”步骤,直接在“氧化除杂”步骤中除去Cd2+____ 。
(5)电解硫酸锌溶液制备单质锌时,阴极的电极反应式为____ ;沉积锌后的电解液可返回___ 工序继续使用。
(6)改进的锌冶炼工艺,采用了“氧压酸浸”的全湿法流程,既省略了易导致空气污染的焙烧过程,又可获得一种有工业价值的非金属单质,“氧压酸浸”中发生的主要反应的离子方程式为____ 。

相关金属离子[c(Mn+)=0.1mol·L-1]形成氢氧化物沉淀的pH范围如表:
| 金属离子 | Fe3+ | Fe2+ | Zn2+ | Cd2+ |
| 开始沉淀的pH | 1.5 | 6.3 | 6.2 | 7.4 |
| 沉淀完全的pH | 2.8 | 8.3 | 8.2 | 9.4 |
(1)焙烧过程中主要反应的化学方程式为
(2)滤渣1的主要成分除SiO2外还有
(3)氧化除杂工序中通入氧气的作用是
(4)溶液中的Cd2+可用锌粉除去,还原除杂工序中反应的离子方程式为
(5)电解硫酸锌溶液制备单质锌时,阴极的电极反应式为
(6)改进的锌冶炼工艺,采用了“氧压酸浸”的全湿法流程,既省略了易导致空气污染的焙烧过程,又可获得一种有工业价值的非金属单质,“氧压酸浸”中发生的主要反应的离子方程式为
2022·新疆克拉玛依·三模
类题推荐
我国是世界上最早制得和使用金属锌的国家。一种以闪锌矿(ZnS,含有SiO2和少量FeS、CdS、PbS杂质)为原料制备金属锌的流程如图所示:
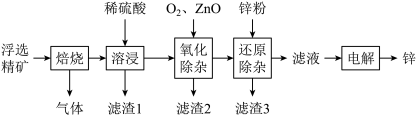
相关金属离子[c0(Mn+)=0.1 mol·L-1]形成氢氧化物沉淀的pH范围如下:
回答下列问题:
(1)焙烧过程中主要反应的化学方程式为_____ 。
(2)滤渣1的主要成分除SiO2外还有__ ;氧化除杂工序中ZnO的作用是___ ,若不通入氧气,其后果是__ 。
(3)溶液中的Cd2+可用锌粉除去,还原除杂工序中反应的离子方程式为___ 。
(4)电解硫酸锌溶液制备单质锌时,阴极的电极反应式为___ 。

相关金属离子[c0(Mn+)=0.1 mol·L-1]形成氢氧化物沉淀的pH范围如下:
金属离子 | Fe3+ | Fe2+ | Zn2+ | Cd2+ |
开始沉淀的pH | 1.5 | 6.3 | 6.2 | 7.4 |
沉淀完全的pH | 2.8 | 8.3 | 8.2 | 9.4 |
(1)焙烧过程中主要反应的化学方程式为
(2)滤渣1的主要成分除SiO2外还有
(3)溶液中的Cd2+可用锌粉除去,还原除杂工序中反应的离子方程式为
(4)电解硫酸锌溶液制备单质锌时,阴极的电极反应式为
我国是世界上最早制得和使用金属锌的国家,一种以闪锌矿(ZnS,含有 和少量FeS、CdS、PbS杂质)为原料制备金属锌的流程如图所示:
和少量FeS、CdS、PbS杂质)为原料制备金属锌的流程如图所示:

相关金属离子[ ]形成氢氧化物沉淀的pH范围如下:
]形成氢氧化物沉淀的pH范围如下:
回答下列问题:
(1)焙烧过程中主要反应的化学方程式为_______ 。
(2)滤渣1的主要成分除 外还有
外还有_______ ;滤渣2的主要成分_______ 。
(3)氧化除杂工序中ZnO的作用是_______ ,若不通入氧气,其后果是_______ 。
(4)溶液中的 可用锌粉除去,还原除杂工序中反应的离子方程式为
可用锌粉除去,还原除杂工序中反应的离子方程式为_______ 。
(5)电解硫酸锌溶液制备单质锌时,阴极的电极反应式为_______ ;沉积锌后的电解液可返回_______ 工序继续使用。

相关金属离子[
| 金属离子 | ||||
| 开始沉淀的pH | 1.5 | 6.3 | 6.2 | 7.4 |
| 沉淀完全的pH | 2.8 | 8.3 | 8.2 | 9.4 |
(1)焙烧过程中主要反应的化学方程式为
(2)滤渣1的主要成分除
(3)氧化除杂工序中ZnO的作用是
(4)溶液中的
(5)电解硫酸锌溶液制备单质锌时,阴极的电极反应式为
我国是世界上最早制得和使用金属锌的国家,一种以闪锌矿(ZnS,含有SiO2和少量FeS、CdS、PbS杂质)为原料制备金属锌的流程如图所示:
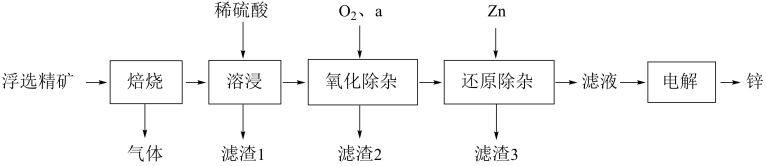
相关金属离子[c0(Mn+)=0.1mol·L-1]形成氢氧化物沉淀的pH范围如表:
回答下列问题:
(1)焙烧过程中主要反应的化学方程式为_____ ;滤渣1的主要成分____ 。
(2)氧化除杂工序中,O2的作用是____ ;为调节溶液pH进行除杂,试剂a可选择____ 。
(3)溶液中的Cd2+可用锌粉除去,还原除杂工序中反应的离子方程式为___ 。
(4)电解硫酸锌溶液制备单质锌并沉积锌后的电解液可返回___ 工序继续使用。
(5)已知Ksp[Fe(OH)3]=2.6×10-39,求pH=3.0时,溶液中Fe3+的浓度___ 。

相关金属离子[c0(Mn+)=0.1mol·L-1]形成氢氧化物沉淀的pH范围如表:
| 金属离子 | Fe3+ | Fe2+ | Zn2+ | Cd2+ |
| 开始沉淀的pH | 1.5 | 6.3 | 6.2 | 7.4 |
| 沉淀完全的pH | 3.0 | 8.3 | 8.2 | 9.4 |
(1)焙烧过程中主要反应的化学方程式为
(2)氧化除杂工序中,O2的作用是
(3)溶液中的Cd2+可用锌粉除去,还原除杂工序中反应的离子方程式为
(4)电解硫酸锌溶液制备单质锌并沉积锌后的电解液可返回
(5)已知Ksp[Fe(OH)3]=2.6×10-39,求pH=3.0时,溶液中Fe3+的浓度
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


