解答题-工业流程题 适中0.65 引用1 组卷281
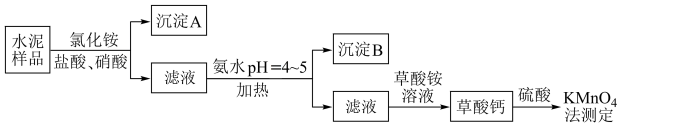
水泥是重要的建筑材料。水泥熟料的主要成分为CaO、 ,并含有一定量的铁、铝和镁等金属的氧化物。实验室测定水泥样品中钙含量的过程如图所示:
,并含有一定量的铁、铝和镁等金属的氧化物。实验室测定水泥样品中钙含量的过程如图所示:
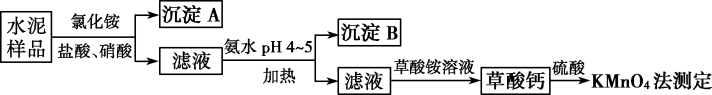
回答下列问题:
(1)在分解水泥样品过程中,以盐酸为溶剂,氯化铵为助溶剂,还需加入几滴硝酸。加入硝酸的目的是_______ ,还可使用_______ 代替硝酸。
(2)沉淀A的主要成分是_______ ,其不溶于强酸但可与一种弱酸反应,该反应的化学方程式为_______ 。
(3)加氨水过程中加热的目的是_______ 。沉淀B的主要成分为 、
、_______ (填化学式)
(4)草酸钙沉淀经稀 处理后,用
处理后,用 标准溶液滴定,通过测定草酸的量可间接获知钙的含量,滴定反应为:
标准溶液滴定,通过测定草酸的量可间接获知钙的含量,滴定反应为: 。实验中称取0.400g水泥样品,滴定时消耗了
。实验中称取0.400g水泥样品,滴定时消耗了 的
的 溶液36.00mL,则该水泥样品中钙的质量分数为
溶液36.00mL,则该水泥样品中钙的质量分数为_______ ,(相对原子质量Ca:40)

回答下列问题:
(1)在分解水泥样品过程中,以盐酸为溶剂,氯化铵为助溶剂,还需加入几滴硝酸。加入硝酸的目的是
(2)沉淀A的主要成分是
(3)加氨水过程中加热的目的是
(4)草酸钙沉淀经稀
2022·广东潮州·二模
类题推荐
Ⅰ.水泥是重要的建筑材料。水泥熟料的主要成分为CaO、SiO2,并含有一定量的铁、铝和镁等金属的氧化物。实验室测定水泥样品中钙含量的某种方法过程如图所示:
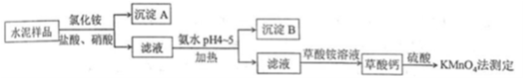
(1)在分解水泥样品过程中,以盐酸为溶剂,氯化铵为助溶剂,还需加入几滴硝酸。加入硝酸的目的是_____________ ,还可使用__________ 代替硝酸。
(2)沉淀A的主要成分是________ ,其不溶于强酸但可与一种弱酸反应,该反应的化学方程式为____________ 。
(3)加氨水过程中加热的目的是_____ 。沉淀B的主要成分为_______ 、_________ (填化学式)。
Ⅱ、已知25℃时草酸的电离常数为K1=5.0×10-2,K2=5.4×10-5.草酸钙的Kap=4.0×10-8.碳酸钙的Ksp=2.5×10-9.不同温度下水的离子积常数见下表:
(1)计算25℃时KHC2O4溶液的水解平衡常数Kb=_____ ;写出水溶液中草酸的电离方程式_____ ;常温下将0.2mol/L的KOH溶液10mL与0.2mol/L的草酸溶液20mL混合后溶液显________ 性。(填“酸性”“中性”或“无法确定”)
(2)25℃时向20mL草酸钙的饱和溶液中逐滴加入8.0×10-4mol/L的碳酸钾溶液10mL,能否产生沉淀,_______ (填“能”或“否”). 碳酸钙转化为草酸钙的离子方程式为______ ,列式计算该反的平衡常数K=_________ 。
(3)90℃时,将0.005mol/L的氢氧化钙溶液20mL与0.0012mol/L的草酸溶液20mL混合,则混合后溶液的pH______ 。(可能用到的对数:lg38=1.6,lg26=2.4,lg2=0.3)

(1)在分解水泥样品过程中,以盐酸为溶剂,氯化铵为助溶剂,还需加入几滴硝酸。加入硝酸的目的是
(2)沉淀A的主要成分是
(3)加氨水过程中加热的目的是
Ⅱ、已知25℃时草酸的电离常数为K1=5.0×10-2,K2=5.4×10-5.草酸钙的Kap=4.0×10-8.碳酸钙的Ksp=2.5×10-9.不同温度下水的离子积常数见下表:
| t/℃ | 0 | 10 | 20 | 25 | 40 | 50 | 90 | 100 |
| Kw/10-14 | 0.134 | 0.292 | 0.681 | 1.00 | 2.92 | 5.57 | 38.0 | 55.0 |
(1)计算25℃时KHC2O4溶液的水解平衡常数Kb=
(2)25℃时向20mL草酸钙的饱和溶液中逐滴加入8.0×10-4mol/L的碳酸钾溶液10mL,能否产生沉淀,
(3)90℃时,将0.005mol/L的氢氧化钙溶液20mL与0.0012mol/L的草酸溶液20mL混合,则混合后溶液的pH
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网