解答题-工业流程题 较难0.4 引用1 组卷115
无水氯化钴(CoCl2)用作彩色水泥的添加剂、催化剂、饲料等,以钴渣(主要成分是CoO含少量NiO、CuO、FeO和SiO2等)为原料制备无水氯化钴的工艺流程如图:
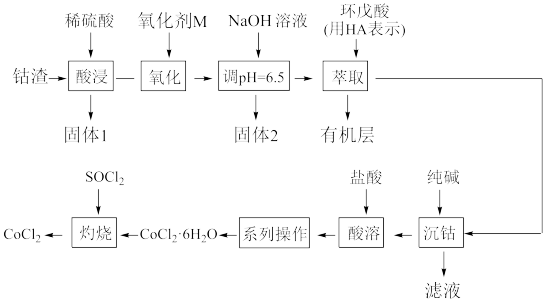
已知几种金属氢氧化物沉淀的pH如表所示:
请回答下列问题:
(1)固体1的主要成分是____ (填化学式)。
(2)从绿色化学角度考虑选择试剂M为H2O2,其作用是____ (用离子方程式表示)。“调pH=6.5”除去的固体2的成分是____ (填化学式)。
(3)“萃取”目的是除去____ (填离子符号)。
(4)“系列操作”的实验操作依次为缓缓加热,浓缩至溶液表面出现结晶薄膜为止、____ 、过滤、洗涤、干燥,即得产品。
(5)“灼烧”过程生成两种溶于水呈酸性的气体,请写出相应的化学方程式____ 。
(6)测定CoCl2产品纯度:准确称取mg产品溶于蒸馏水配制成250mL溶液,量取25.0mL于锥形瓶中,加入几滴K2CrO4溶液作指示剂,用cmol·L-1AgNO3滴定至终点,消耗滴定液体积为xmL。该产品纯度为____ (用含m、c和x的代数式表示)。

已知几种金属氢氧化物沉淀的pH如表所示:
| 金属离子 | Co2+ | Cu2+ | Ni2+ | Fe3+ | Fe2+ |
| 开始沉淀时pH | 7.6 | 4.4 | 6.8 | 1.9 | 7.5 |
| 完全沉淀时pH | 9.2 | 6.4 | 8.4 | 3.2 | 9.5 |
请回答下列问题:
(1)固体1的主要成分是
(2)从绿色化学角度考虑选择试剂M为H2O2,其作用是
(3)“萃取”目的是除去
(4)“系列操作”的实验操作依次为缓缓加热,浓缩至溶液表面出现结晶薄膜为止、
(5)“灼烧”过程生成两种溶于水呈酸性的气体,请写出相应的化学方程式
(6)测定CoCl2产品纯度:准确称取mg产品溶于蒸馏水配制成250mL溶液,量取25.0mL于锥形瓶中,加入几滴K2CrO4溶液作指示剂,用cmol·L-1AgNO3滴定至终点,消耗滴定液体积为xmL。该产品纯度为
21-22高二下·广东梅州·阶段练习
类题推荐
无水氯化钴 用作彩色水泥的添加剂、催化剂、饲料等,以钴渣(主要成分是CoO含少量NiO、CuO、FeO和
用作彩色水泥的添加剂、催化剂、饲料等,以钴渣(主要成分是CoO含少量NiO、CuO、FeO和 等)为原料制备无水氯化钴的工艺流程如下:
等)为原料制备无水氯化钴的工艺流程如下:
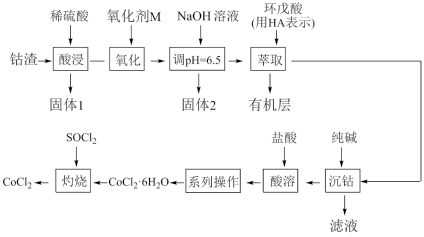
已知几种金属氢氧化物沉淀的pH如下表所示:
请回答下列问题:
(1)固体1的主要成分是___________ (填化学式)。
(2)试剂M为 ,其作用是
,其作用是___________ 。(用离子方程式表示)
(3)“调 ”时除去的“固体2”的成分是
”时除去的“固体2”的成分是___________ (填化学式),“萃取”目的是除去___________ 离子(填离子符号)。
(4)测定 产品纯度:准确称取m g产品溶于水配制成250mL溶液,量取25.0mL于锥形瓶中,加入几滴
产品纯度:准确称取m g产品溶于水配制成250mL溶液,量取25.0mL于锥形瓶中,加入几滴 溶液作指示剂,用
溶液作指示剂,用 滴定至终点,消耗滴定液体积为x mL。该产品纯度为
滴定至终点,消耗滴定液体积为x mL。该产品纯度为___________ (用含m、c和x的代数式表示)。
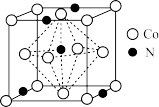
(5)金属钴与氮元素可形成氮化物晶体,所成晶体的结构其中一种为立方晶胞如图。则该晶体的化学式为___________ ,目前最常用测定晶体结构方法是利用___________ 技术。

已知几种金属氢氧化物沉淀的pH如下表所示:
| 金属离子 | |||||
| 开始沉淀时pH | 7.6 | 4.4 | 6.8 | 1.9 | 7.5 |
| 完全沉淀时pH | 9.2 | 6.4 | 8.4 | 3.2 | 9.5 |
请回答下列问题:
(1)固体1的主要成分是
(2)试剂M为
(3)“调
(4)测定
(5)金属钴与氮元素可形成氮化物晶体,所成晶体的结构其中一种为立方晶胞如图。则该晶体的化学式为

无水氯化钴( )可用作彩色水泥的添加剂、催化剂、饲料等,以钴渣(主要成分是CoO,含少量NiO、CuO、FeO和
)可用作彩色水泥的添加剂、催化剂、饲料等,以钴渣(主要成分是CoO,含少量NiO、CuO、FeO和 等)为原料制备无水氯化钴的流程如下:
等)为原料制备无水氯化钴的流程如下:
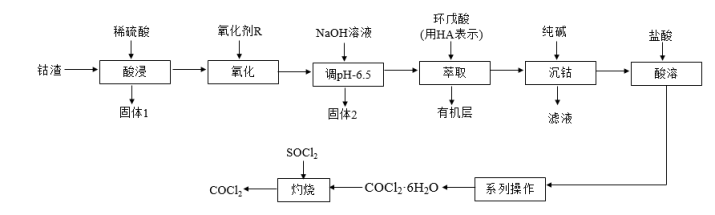
已知:几种金属离子沉淀的pH如下表所示:
请回答下列问题:
(1)“酸浸”时,用稀硝酸代替稀硫酸,缺点是___________ 。
(2)“氧化剂R”的作用是___________ 。
(3)“固体2”的主要成分是___________ 。(填化学式)
(4)M代表被萃取的离子,萃取过程简化为 (水层)+2xHA (有机层)
(水层)+2xHA (有机层) 2MAx(有机层)+xH2SO4 (水层)。在萃取过程中加入适量氨水,其作用是
2MAx(有机层)+xH2SO4 (水层)。在萃取过程中加入适量氨水,其作用是___________ 。
(5)室温下,“沉钴”时,当溶液中 时,
时, ,
, =
=___________ 。
(6) 与水反应生成SO2和HCl。“灼烧”时发生反应的化学方程式为
与水反应生成SO2和HCl。“灼烧”时发生反应的化学方程式为___________ 。
(7)测定CoCl2产品纯度:准确称取mg CoCl2产品溶于蒸馏水配制成250mL溶液,量取25.00mL所配制溶液于锥形瓶中,滴几滴K2CrO4溶液,用cmol/L的AgNO3溶液滴定至终点,消耗AgNO3溶液的体积为xmL。该产品纯度为___________ (用含m、c和x的代数式表示)。

已知:几种金属离子沉淀的pH如下表所示:
| 金属离子 | 开始沉淀时的pH | 完全沉淀时的pH |
| Co2+ | 7.6 | 9.2 |
| Cu2+ | 4.4 | 6.4 |
| Ni2+ | 6.8 | 8.4 |
| Fe3+ | 1.9 | 3.2 |
| Fe2+ | 7.5 | 9.5 |
请回答下列问题:
(1)“酸浸”时,用稀硝酸代替稀硫酸,缺点是
(2)“氧化剂R”的作用是
(3)“固体2”的主要成分是
(4)M代表被萃取的离子,萃取过程简化为
(5)室温下,“沉钴”时,当溶液中
(6)
(7)测定CoCl2产品纯度:准确称取mg CoCl2产品溶于蒸馏水配制成250mL溶液,量取25.00mL所配制溶液于锥形瓶中,滴几滴K2CrO4溶液,用cmol/L的AgNO3溶液滴定至终点,消耗AgNO3溶液的体积为xmL。该产品纯度为
CoCl2·6H2O是一种饲料营养强化剂。一种利用水钴矿(主要成分为Co2O3、Co(OH)3,还含少量Fe2O3、Al2O3、MnO等)制取CoCl2·6H2O的工艺流程如下:
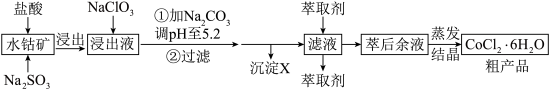
已知:①浸出液含有的阳离子主要有H+、Co2+、Fe2+、Mn2+、Al3+等;
②酸性条件下,ClO3-不会氧化Co2+,ClO3-转化为Cl-;
③部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:(金属离子浓度为:0.01mol/L)
④CoCl2·6H2O熔点为86℃,加热至110~120℃时,失去结晶生成无水氯化钴。
请回答:
(1)写出浸出过程中Co2O3发生反应的离子方程式___________ 。
(2)向浸出液中加入 NaClO3发生主要反应的离子方程式___________ 。
(3)“加Na2CO3调pH至5.2”,过滤所得到的沉淀Ⅹ成分为___________ 。
(4)萃取剂对金属离子的萃取率与pH的关系如图所示,萃取剂使用的适宜pH范围是___________ 。(填选项序号字母)

A 1.0~2.0 B 2.5~3.5 C 4.0~5.0
(5)制得的CoCl2·6H2O在烘干时需减压烘干的原因是___________ 。
(6)为测定粗产品中CoCl2·6H2O含量,称取2g的粗产品溶于水,配成100mL溶液,取出20mL置于锥形瓶,加入K2CrO4做指示剂( Ag2CrO4为砖红色沉淀),用0.2mol/L的AgNO3溶液滴定至终点,重复2-3次,平均消耗AgNO3标准溶液10.00mL。该粗产品中CoCl2·6H2O的质量分数为___________ 。用K2CrO4做指示剂时,需要控制溶液pH值为6.5~10.5,试分析原因______________________ 。

已知:①浸出液含有的阳离子主要有H+、Co2+、Fe2+、Mn2+、Al3+等;
②酸性条件下,ClO3-不会氧化Co2+,ClO3-转化为Cl-;
③部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:(金属离子浓度为:0.01mol/L)
沉淀物 | Fe(OH)3 | Fe(OH)2 | Co(OH)2 | Al(OH)3 | Mn(OH)2 |
开始沉淀 | 2.7 | 7.6 | 7.6 | 4.0 | 7.7 |
完全沉淀 | 3.7 | 9.6 | 9.2 | 5.2 | 9.8 |
④CoCl2·6H2O熔点为86℃,加热至110~120℃时,失去结晶生成无水氯化钴。
请回答:
(1)写出浸出过程中Co2O3发生反应的离子方程式
(2)向浸出液中加入 NaClO3发生主要反应的离子方程式
(3)“加Na2CO3调pH至5.2”,过滤所得到的沉淀Ⅹ成分为
(4)萃取剂对金属离子的萃取率与pH的关系如图所示,萃取剂使用的适宜pH范围是

A 1.0~2.0 B 2.5~3.5 C 4.0~5.0
(5)制得的CoCl2·6H2O在烘干时需减压烘干的原因是
(6)为测定粗产品中CoCl2·6H2O含量,称取2g的粗产品溶于水,配成100mL溶液,取出20mL置于锥形瓶,加入K2CrO4做指示剂( Ag2CrO4为砖红色沉淀),用0.2mol/L的AgNO3溶液滴定至终点,重复2-3次,平均消耗AgNO3标准溶液10.00mL。该粗产品中CoCl2·6H2O的质量分数为
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


