解答题-原理综合题 适中0.65 引用1 组卷75
利用化学反应将储存在物质内部的化学能转化为电能,科学家设计出了原电池,从而为人类生产生活提供能量。回答下列问题:
(1)将2Ag+ +Cu=Cu2+ +2Ag设计成原电池,装置如图所示。
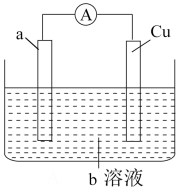
①a电极为_______ (填 “负极”或“正极”),b溶液为_______ (填化学式),Cu电极上发生的反应为_______ 。
②当反应进行到一段时间后取出电极材料,测得某一电极增重了5.4g,则该原电池电路中转移的电子数目是_______ 。
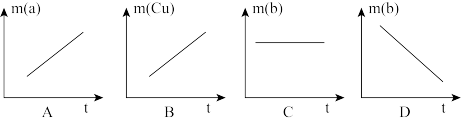
③如图所示能正确表示实验过程中变化的是_______ (填序号)。
(2)某学习小组利用原电池探究浓硝酸或稀硝酸与铁的反应。
①取少量I中溶液,加入KSCN溶液,溶液变红,写出I中发生反应的离子方程式_______ 。
②II中Fe表面产生红棕色气泡,此时Cu是_______ 极,而后停止的原因是_______ 。
(1)将2Ag+ +Cu=Cu2+ +2Ag设计成原电池,装置如图所示。

①a电极为
②当反应进行到一段时间后取出电极材料,测得某一电极增重了5.4g,则该原电池电路中转移的电子数目是
③如图所示能正确表示实验过程中变化的是

(2)某学习小组利用原电池探究浓硝酸或稀硝酸与铁的反应。
| 实验 | 现象 |
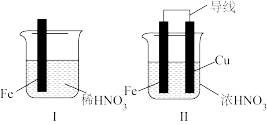 | I中: Fe表面产生大量无色气泡,液面上方变为红棕色 II中:连接导线,一段时间后Fe表面产生红棕色气泡,而后停止;Cu表面始终产生红棕色气泡 |
②II中Fe表面产生红棕色气泡,此时Cu是
21-22高一下·河北张家口·期中
类题推荐
实验小组利用原电池研究物质性质。
【实验1】某学习小组探究浓硝酸或稀硝酸与铁的反应。
(1)取少量Ⅰ中溶液,加入KSCN溶液,_______ (填现象),说明产生了Fe3+;Ⅰ中Fe表面产生大量无色气泡的化学方程式为_______ 。
(2)Ⅱ中现象说明Fe表面形成致密的氧化层,阻止Fe进一步反应。说明浓硝酸具有_______ 性。
【实验2】探究铝片做电极材料时的原电池反应,设计下表中装置进行实验并记录。
(3)实验2中,电解质溶液为盐酸,镁条做原电池的_______ 极。
【实验3】将实验2中的电解质溶液换为NaOH溶液进行实验2。
(4)该小组同学认为,此时原电池的总反应为2Al+2NaOH+2H2O=2NaAlO2+3H2↑,据此推测实验现象为_______ ,负极反应为_______ 。
【实验1】某学习小组探究浓硝酸或稀硝酸与铁的反应。
| 实验 | 现象 |
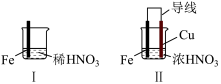 | Ⅰ中:Fe表面产生大量无色气泡,液面上方变为红棕色 II中:连接导线,一段时间后Fe表面产生红棕色气泡,而后停止;Cu表面始终产生红棕色气泡 |
(2)Ⅱ中现象说明Fe表面形成致密的氧化层,阻止Fe进一步反应。说明浓硝酸具有
【实验2】探究铝片做电极材料时的原电池反应,设计下表中装置进行实验并记录。
| 装置 | 实验现象 |
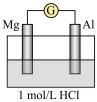 | 装置电流计指针向右偏转,镁条、铝条表面产生无色气泡 |
【实验3】将实验2中的电解质溶液换为NaOH溶液进行实验2。
(4)该小组同学认为,此时原电池的总反应为2Al+2NaOH+2H2O=2NaAlO2+3H2↑,据此推测实验现象为
运用电化学原理可进行工业生产或研究物质的性质。
(1)如图所示,运用电化学原理可生产硫酸,总反应为2SO2+O2+2H2O=2H2SO4。其中质子交换膜将该原电池分隔成氧化反应室和还原反应室,能阻止气体通过而允许H+通过。

①电池的负极是____ 。(填“电极a”或“电极b”)
②H+通过质子交换膜时的移动方向是____ 。
a.从左向右 b.从右向左
③通入O2的电极反应式是____ 。
(2)某学习小组利用原电池探究浓硝酸或稀硝酸与铁的反应。
①取少量Ⅰ中溶液,加入KSCN溶液,____ (填现象),说明产生了Fe3+;Ⅰ中Fe表面产生大量无色气泡的化学方程式为____ 。
②Ⅱ中现象说明Fe表面形成致密的氧化层,阻止Fe进一步反应。说明浓硝酸具有____ 性。
(1)如图所示,运用电化学原理可生产硫酸,总反应为2SO2+O2+2H2O=2H2SO4。其中质子交换膜将该原电池分隔成氧化反应室和还原反应室,能阻止气体通过而允许H+通过。

①电池的负极是
②H+通过质子交换膜时的移动方向是
a.从左向右 b.从右向左
③通入O2的电极反应式是
(2)某学习小组利用原电池探究浓硝酸或稀硝酸与铁的反应。
| 实验 | 现象 | |
 |  | Ⅰ中:Fe表面产生大量无色气泡,液面上方变为红棕色 Ⅱ中:连接导线,一段时间后Fe表面产生红棕色气泡,而后停止;Cu表面始终产生红棕色气泡 |
②Ⅱ中现象说明Fe表面形成致密的氧化层,阻止Fe进一步反应。说明浓硝酸具有
化学电源在生产生活中有着广泛的应用,请回答下列问题:
(1)根据构成原电池的本质判断,下列化学(或离子)方程式正确且能设计成原电池的是_______(填字母,下同)。
(2)为了探究化学反应中的能量变化,某同学设计了如下两个实验(如图)。
①有关反应一段时间后的实验现象,下列说法正确的是_______ 。
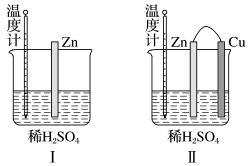
A.图I中温度计的示数高于图II的示数
B.图I和图II中温度计的示数相等,且均高于室温
C.图I和图II的气泡均产生于锌棒表面
D.图II中产生气体的速率比I慢
②写出图II中正极的电极反应式:_______ ;
③图II中随着反应的进行,负极质量将_______ (填“增大”“减小”或“不变”)。当外电路上有2mol电子通过时,溶液中消耗H2SO4的物质的量为_______ 。
(1)根据构成原电池的本质判断,下列化学(或离子)方程式正确且能设计成原电池的是_______(填字母,下同)。
| A.KOH+HCl=KCl+H2O | B.Cu+Fe3+=Fe2++Cu2+ |
| C.Na2O+H2O=2NaOH | D.Fe+H2SO4=FeSO4+H2↑ |
①有关反应一段时间后的实验现象,下列说法正确的是

A.图I中温度计的示数高于图II的示数
B.图I和图II中温度计的示数相等,且均高于室温
C.图I和图II的气泡均产生于锌棒表面
D.图II中产生气体的速率比I慢
②写出图II中正极的电极反应式:
③图II中随着反应的进行,负极质量将
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


