解答题-实验探究题 适中0.65 引用2 组卷369
化学反应速率和限度与生产、生活密切相关。
I.某同学探究外界条件对H2O2分解速率的影响
实验所用试剂:0.4mol·L-1H2O2溶液、蒸馏水、CuSO4粉末、FeCl3粉末。
(1)实验1、2的目的是其他条件相同时,研究____ 对H2O2分解速率的影响。
(2)对比实验3、4,能否推测Fe3+对H2O2分解的催化效果比Cu2+的好?____ (填“能”或“不能”),请说明理由____ 。
(3)实验3、5是其他条件相同时,探究浓度对该化学反应速率的影响。m处取用10mL0.4mol·L-1H2O2溶液,还应添加的剂及用量为____ 。(混合后溶液体积变化忽略不计)
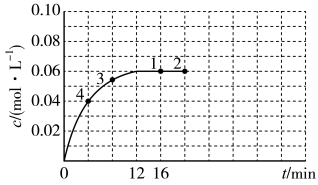
II.NO2(红棕色)和N2O4(无色)之间可发生反应:N2O4(g) 2NO2(g)。在温度为T的条件下,将0.08molN2O4气体充入体积为2L的恒容密闭容器中,容器中某气体的物质的量浓度随时间变化曲线如图所示。
2NO2(g)。在温度为T的条件下,将0.08molN2O4气体充入体积为2L的恒容密闭容器中,容器中某气体的物质的量浓度随时间变化曲线如图所示。____ 。
(5)反应进行到16min时,N2O4的转化率是___ 。
(6)下列可以说明该反应达到平衡的是____ 。
A.c(N2O4):c(NO2)=1:2
B.v正(N2O4)=2v逆(NO2)
C.容器内气体的颜色深浅不再变化
D.混合气体的平均相对分子质量不再变化
E.混合气体的密度不再变化
I.某同学探究外界条件对H2O2分解速率的影响
实验所用试剂:0.4mol·L-1H2O2溶液、蒸馏水、CuSO4粉末、FeCl3粉末。
| 实验 序号 | H2O2溶液 | 温度 | 催化剂 | 收集112mLO2所需时间 | |
| 浓度(mol·L-1) | V(mL) | ||||
| 1 | 0.4 | 20 | 室温 | 无 | 几乎无气体产生 |
| 2 | 0.4 | 20 | 50℃ | 无 | 296 |
| 3 | 0.4 | 20 | 室温 | 0.5molCuSO4 | 45 |
| 4 | 0.4 | 20 | 室温 | 0.5molFeCl3 | 100 |
| 5 | 0.2 | m | 室温 | 0.5molCuSO4 | >45 |
(2)对比实验3、4,能否推测Fe3+对H2O2分解的催化效果比Cu2+的好?
(3)实验3、5是其他条件相同时,探究浓度对该化学反应速率的影响。m处取用10mL0.4mol·L-1H2O2溶液,还应添加的剂及用量为
II.NO2(红棕色)和N2O4(无色)之间可发生反应:N2O4(g)
(5)反应进行到16min时,N2O4的转化率是
(6)下列可以说明该反应达到平衡的是
A.c(N2O4):c(NO2)=1:2
B.v正(N2O4)=2v逆(NO2)
C.容器内气体的颜色深浅不再变化
D.混合气体的平均相对分子质量不再变化
E.混合气体的密度不再变化
21-22高一下·广东深圳·期中
类题推荐
化学反应速率和限度与生产、生活密切相关。
Ⅰ.某同学探究外界条件对H2O2分解速率的影响,实验所用试剂:0.6 mol/LH2O2溶液、蒸馏水、CuSO4粉末、FeCl3粉末。
(1)本实验待测数据可以是_______ 。
(2)实验1、3的目的是在其他条件相同时,研究_______ 对H2O2分解速率的影响。
(3)实验3、4所测得的数据,能否比较Fe3+和Cu2+的催化效果?_______ (填“能”或“不能”),请说明理由_______ 。
(4)实验3、5是在其他条件相同时,探究浓度对该化学反应速率的影响。m处取用15 mL0.6 mol/LH2O2溶液,还应添加的试剂及用量为_______ (混合后溶液体积变化忽略不计)。
Ⅱ.某温度下,在容积恒定为2.0 L的密闭容器中充入4.0 mol N2和4.0 mol H2,一段时间后反应N2(g)+3H2(g) 2NH3(g)达到平衡状态,实验数据如下表所示:
2NH3(g)达到平衡状态,实验数据如下表所示:
(5)0~150 s内的平均反应速率v(N2)=_______ ,250 s时,H2的转化率为_______ 。
(6)为加快反应速率,可以采取的措施是_______ (填字母)。
a.降低温度
b.减小容器容积
c.恒压时充入Ne气
d.恒容时充入Ne气
Ⅰ.某同学探究外界条件对H2O2分解速率的影响,实验所用试剂:0.6 mol/LH2O2溶液、蒸馏水、CuSO4粉末、FeCl3粉末。
| 实验序号 | H2O2溶液 | 温度 | 催化剂 | |
| 浓度(mol/L) | V(mL) | |||
| 1 | 0.6 | 30 | 室温 | 无 |
| 2 | 0.6 | 30 | 50℃ | 无 |
| 3 | 0.6 | 30 | 室温 | 0.005 mol CuSO4 |
| 4 | 0.6 | 30 | 室温 | 0.005 mol FeCl3 |
| 5 | 0.3 | m | 室温 | 0.005 mol CuSO4 |
(2)实验1、3的目的是在其他条件相同时,研究
(3)实验3、4所测得的数据,能否比较Fe3+和Cu2+的催化效果?
(4)实验3、5是在其他条件相同时,探究浓度对该化学反应速率的影响。m处取用15 mL0.6 mol/LH2O2溶液,还应添加的试剂及用量为
Ⅱ.某温度下,在容积恒定为2.0 L的密闭容器中充入4.0 mol N2和4.0 mol H2,一段时间后反应N2(g)+3H2(g)
| t/s | 0 | 50 | 150 | 250 | 350 |
| n(NH3) | 0 | 0.24 | 0.30 | 0.40 | 0.40 |
(6)为加快反应速率,可以采取的措施是
a.降低温度
b.减小容器容积
c.恒压时充入Ne气
d.恒容时充入Ne气
双氧水也是常用消毒剂之一、某同学探究外界条件对H2O2分解速率的影响。
实验所用试剂:0.4mol·L-1H2O2溶液、蒸馏水、CuSO4粉末、FeCl3粉末。
(1)实验1、2的目的是其他条件相同时,研究_______ 对H2O2分解速率的影响。
(2)对比实验3、4,能否推测Fe3+对H2O2分解的催化效果比Cu2+的好?_______ (填“能”或“不能”),请说明理由_______ 。
(3)实验3、5是其他条件相同时,探究浓度对该化学反应速率的影响。m处取用10mL0.4mol·L-1H2O2溶液,还应添加的剂及用量为_______ 。(混合后溶液体积变化忽略不计)
实验所用试剂:0.4mol·L-1H2O2溶液、蒸馏水、CuSO4粉末、FeCl3粉末。
| 实验 序号 | H2O2溶液 | 温度 | 催化剂 | 收集112mLO2所需时间 | |
| 浓度(mol·L-1) | V(mL) | ||||
| 1 | 0.4 | 20 | 室温 | 无 | 几乎无气体产生 |
| 2 | 0.4 | 20 | 50℃ | 无 | 296 |
| 3 | 0.4 | 20 | 室温 | 0.5molCuSO4 | 45 |
| 4 | 0.4 | 20 | 室温 | 0.5molFeCl3 | 100 |
| 5 | 0.2 | m | 室温 | 0.5molCuSO4 | >45 |
(2)对比实验3、4,能否推测Fe3+对H2O2分解的催化效果比Cu2+的好?
(3)实验3、5是其他条件相同时,探究浓度对该化学反应速率的影响。m处取用10mL0.4mol·L-1H2O2溶液,还应添加的剂及用量为
化学反应速率和限度与生产、生活密切相关。
I.某同学探究外界条件对H2O2分解速率的影响
实验所用试剂:0.4mol·L-1H2O2溶液、蒸馏水、CuSO4粉末、FeCl3粉末。
(1)实验1、2的目的是其他条件相同时,研究____ 对H2O2分解速率的影响。
(2)对比实验3、4,能否推测Cu2+对H2O2分解的催化效果比Fe3+的好?____ (填“能”或“不能”),请说明理由___ 。
(3)实验3、5是其他条件相同时,探究浓度对该化学反应速率的影响。m处取用10mL0.4mol·L-1的H2O2溶液,还应添加的试剂及用量为____ 。(混合后溶液体积变化忽略不计)
Ⅱ.某同学探究影响硫代硫酸钠与稀硫酸反应速率的因素时,设计了如下系列实验:
(4)硫代硫酸钠与稀硫酸反应的化学方程式为____ 。
(5)该反应速率的快慢可通过观察___ 来判断。
(6)计算实验①中v(Na2S2O3)=___ (用含t1的代数式表示)。
(7)该实验②中V1是_____ ;实验③中V3是___ 。
I.某同学探究外界条件对H2O2分解速率的影响
实验所用试剂:0.4mol·L-1H2O2溶液、蒸馏水、CuSO4粉末、FeCl3粉末。
| 实验序号 | H2O2溶液 | 温度 | 催化剂 | 收集112mLO2所需时间 | |
| 浓度(mol·L-1) | V(mL) | ||||
| 1 | 0.4 | 20 | 室温 | 无 | 几乎无气体产生 |
| 2 | 0.4 | 20 | 50℃ | 无 | 296 |
| 3 | 0.4 | 20 | 室温 | 0.5molCuSO4 | 45 |
| 4 | 0.4 | 20 | 室温 | 0.5molFeCl3 | 100 |
| 5 | m | 室温 | 0.5molCuSO4 | >45 | |
(2)对比实验3、4,能否推测Cu2+对H2O2分解的催化效果比Fe3+的好?
(3)实验3、5是其他条件相同时,探究浓度对该化学反应速率的影响。m处取用10mL0.4mol·L-1的H2O2溶液,还应添加的试剂及用量为
Ⅱ.某同学探究影响硫代硫酸钠与稀硫酸反应速率的因素时,设计了如下系列实验:
| 实验序号 | 反应温度 | Na2S2O3浓度 | 稀硫酸 | H2O | 反应结束时间 | ||
| V/mL | c/(mol/L) | V/mL | c/(mol/L) | V/mL | min | ||
| ① | 20 | 10.0 | 0.10 | 10.0 | 0.50 | 0 | t1 |
| ② | 40 | V1 | 0.10 | 10.0 | 0.50 | V2 | t2 |
| ③ | 20 | 10.0 | 0.10 | 4.0 | 0.50 | V3 | t3 |
(5)该反应速率的快慢可通过观察
(6)计算实验①中v(Na2S2O3)=
(7)该实验②中V1是
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


