解答题-工业流程题 较难0.4 引用1 组卷185
在钢铁工业中,主要用锰脱硫和脱氧:锰也是作为合金的添加料。一种以高铁锰矿(含 、
、 及少量
及少量 、
、 、
、 、
、 )为原料生产金属锰的工艺流程如图。
)为原料生产金属锰的工艺流程如图。
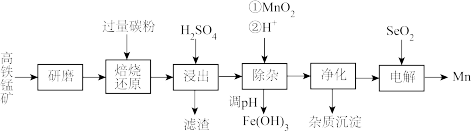
已知:常温下, 的
的 ;
; ;溶液中某离子浓度小于
;溶液中某离子浓度小于 认为该离子沉淀完全。
认为该离子沉淀完全。
回答下列问题:
(1)研磨的目的是_______ 。
(2)“焙烧还原”时,原料中高铁锰矿中 被还原为
被还原为 ,还有能被还原的成分为
,还有能被还原的成分为_______ 、_______ 。(填化学式)
(3)下表数据是焙烧后 元素在主要含锰物质中的分布情况,则焙烧时应选择的温度为
元素在主要含锰物质中的分布情况,则焙烧时应选择的温度为_______  。
。
(4)“浸出”产生两种“滤渣”的成分为_______ 、_______ (填化学式):该步骤中,工业上往往需再加入少量固体 以促进其中一种主要“滤渣”析出,结合化学反应原理解释其原因
以促进其中一种主要“滤渣”析出,结合化学反应原理解释其原因_______ 。
(5)常温下,“除杂”时 参加的反应的离子方程式为
参加的反应的离子方程式为_______ ;再逐步调
_______ 至 完全沉淀。
完全沉淀。
(6)研究表明,加入适量的 有利于
有利于 在电极上析出,电解过程中
在电极上析出,电解过程中 与水反应生成的
与水反应生成的 (二元弱酸)在阴极放电生成
(二元弱酸)在阴极放电生成 单质,该电极反应式为
单质,该电极反应式为_______ 。

已知:常温下,
回答下列问题:
(1)研磨的目的是
(2)“焙烧还原”时,原料中高铁锰矿中
(3)下表数据是焙烧后
| 还原温度/ | 焙烧后 | ||
| 高价锰( | 低价锰( | ||
| 600 800 1000 1100 1200 | 40.92 10.56 6.01 痕量 痕量 | 34.76 6.63 2.70 0.46 0.30 | 24.32 82.81 91.29 98.76 97.94 |
(5)常温下,“除杂”时
(6)研究表明,加入适量的
2021·江西赣州·二模
类题推荐
锰的重要用途是制造锰钢。一种以高铁锰矿(含MnO2、Fe2O3及少量FeO、CaO、K2O、Na2O)为原料生产金属锰的工艺流程如下:
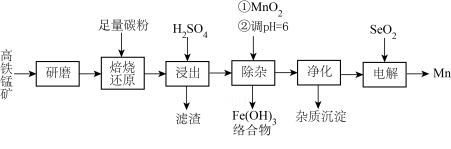
回答下列问题:
(1)“焙烧还原”时,高铁锰矿中MnO2被还原为MnO。
①理论上,还能被还原的成分有___________ 、___________ (填化学式)。
②根据下表数据,焙烧时应选择的温度为___________ 。
(2)“浸出”产生“滤渣”的主要成分为___________ (填化学式);该步骤中需再加入MnSO4以促进“滤渣"析出,结合化学反应原理解释其原因:___________ 。
(3)“除杂”时,加入的MnO2将Fe2+氧化为Fe3+,其离子方程式为___________ ;再将pH逐步调至6,Fe3+水解为Fe(OH)3,同时Fe3+与Na+、K+形成络合物沉淀。
(4)电解“净化”所得溶液(MnSO4的酸性溶液)制备Mn。
①电解时,溶液中的阳离子在阴极存在两个相互竞争的电极反应,其产物分别为Mn和___________ (填化学式)。
②研究表明,加入适量的SeO2有利于Mn在电极上析出。机理为:SeO2与水反应生成的H2SeO3(二元弱酸)在阴极放电生成Se单质,该电极反应为___________ ,电极上的Se对Mn2+有特殊的吸附性能,使Mn2+的电还原沉积成为主要反应。

回答下列问题:
(1)“焙烧还原”时,高铁锰矿中MnO2被还原为MnO。
①理论上,还能被还原的成分有
②根据下表数据,焙烧时应选择的温度为
| 还原温度/℃ | 焙烧后Mn元素在主要含锰物质中的分布/% | ||
| MnO2 | 高价锰(MnxOy) | 低价锰(MnO) | |
| 600 | 40.92 | 34.76 | 24.32 |
| 800 | 10.56 | 6.63 | 82.81 |
| 1000 | 5.77 | 2.70 | 91.29 |
| 1100 | 痕量 | 0.46 | 98.76 |
| 1200 | 痕量 | 0.30 | 97.94 |
(2)“浸出”产生“滤渣”的主要成分为
(3)“除杂”时,加入的MnO2将Fe2+氧化为Fe3+,其离子方程式为
(4)电解“净化”所得溶液(MnSO4的酸性溶液)制备Mn。
①电解时,溶液中的阳离子在阴极存在两个相互竞争的电极反应,其产物分别为Mn和
②研究表明,加入适量的SeO2有利于Mn在电极上析出。机理为:SeO2与水反应生成的H2SeO3(二元弱酸)在阴极放电生成Se单质,该电极反应为
锰的重要用途是制造锰钢.一种以高铁锰矿(含MnO2、Fe2O3及少量FeO、CaO、K2O、Na2O)为原料生产金属锰的工艺流程如图:

回答下列问题:
(1)“焙烧还原”时,高铁锰矿中MnO2被还原为MnO。
①理论上,还能被还原的成分有__ 、__ (填化学式)。
②根据表中数据,焙烧时应选择的温度为__ 。
(2)“浸出”产生“滤渣”的主要成分为___ (填化学式);该步骤中需再加入MnSO4以促进“滤渣”析出,结合化学反应原理解释其原因:___ 。
(3)“除杂”时,加入的MnO2将Fe2+氧化为Fe3+,其离子方程式为___ ;再将pH逐步调至6,Fe3+水解为Fe(OH)3,同时Fe3+与Na+、K+形成络合物沉淀。
(4)电解“净化”所得溶液(MnSO4的酸性溶液)制备Mn。
①电解时,溶液中的阳离子在阴极存在两个相互竞争的电极反应,其产物分别为Mn和__ (填化学式)。
②研究表明,加入适量的SeO2有利于Mn在电极上析出.机理为:SeO2与水反应生成的H2SeO3(二元弱酸)在阴极放电生成Se单质,该电极反应为__ ;电极上的Se对Mn2+有特殊的吸附性能,使Mn2+的电还原沉积成为主要反应。
③电解废液可在上述流程的___ 步骤中循环使用。

回答下列问题:
(1)“焙烧还原”时,高铁锰矿中MnO2被还原为MnO。
①理论上,还能被还原的成分有
②根据表中数据,焙烧时应选择的温度为
| 还原温度/℃ | 焙烧后Mn元素在主要含锰物质中的分布/% | ||
| MnO2 | 高价锰(MnxOy) | 低价锰(MnO) | |
| 600 800 1000 1100 1200 | 40.92 10.56 5.77 痕量 痕量 | 34.76 6.63 2.70 0.46 0.30 | 24.32 82.81 91.29 98.76 97.94 |
(3)“除杂”时,加入的MnO2将Fe2+氧化为Fe3+,其离子方程式为
(4)电解“净化”所得溶液(MnSO4的酸性溶液)制备Mn。
①电解时,溶液中的阳离子在阴极存在两个相互竞争的电极反应,其产物分别为Mn和
②研究表明,加入适量的SeO2有利于Mn在电极上析出.机理为:SeO2与水反应生成的H2SeO3(二元弱酸)在阴极放电生成Se单质,该电极反应为
③电解废液可在上述流程的
锰的重要用途是制造锰钢。一种以高铁锰矿(含MnO2、Fe2O3及少量FeO、CaO、K2O、Na2O)为原料生产金属锰的工艺流程如图:
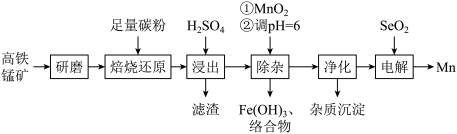
回答下列问题:
(1)“焙烧还原”时,高铁锰矿中MnO2被还原为MnO。
①理论上,还能被还原的成分有___________ 、___________ (填化学式)。
②根据表中数据,焙烧时应选择的温度为___________ 。
(2)“浸出”产生“滤渣”的主要成分为___________ (填化学式)。
(3)“除杂”时,加入的MnO2将Fe2+氧化为Fe3+,其离子方程式为___________ ;再将pH逐步调至6,Fe3+水解为Fe(OH)3,同时Fe3+与Na+、K+形成络合物沉淀。
(4)电解“净化”所得溶液(MnSO4的酸性溶液)制备Mn。
①电解时,溶液中的阳离子在阴极存在两个相互竞争的电极反应,其产物分别为Mn和___________ (填化学式)。
②研究表明,加入适量的SeO2有利于Mn在电极上析出,机理为:SeO2与水反应生成的H2SeO3(二元弱酸)在阴极放电生成Se单质,该电极反应为___________ ;电极上的Se对Mn2+有特殊的吸附性能,使Mn2+的电还原沉积成为主要反应。
③电解废液可在上述流程的___________ 步骤中循环使用。

回答下列问题:
(1)“焙烧还原”时,高铁锰矿中MnO2被还原为MnO。
①理论上,还能被还原的成分有
②根据表中数据,焙烧时应选择的温度为
| 还原温度/℃ | 焙烧后Mn元素在主要含锰物质中的分布/% | ||
| MnO2 | 高价锰(MnxOy) | 低价锰(MnO) | |
| 600 800 1000 1100 1200 | 40.92 10.56 5.77 痕量 痕量 | 34.76 6.63 2.70 0.46 0.30 | 24.32 82.81 91.29 98.76 97.94 |
(2)“浸出”产生“滤渣”的主要成分为
(3)“除杂”时,加入的MnO2将Fe2+氧化为Fe3+,其离子方程式为
(4)电解“净化”所得溶液(MnSO4的酸性溶液)制备Mn。
①电解时,溶液中的阳离子在阴极存在两个相互竞争的电极反应,其产物分别为Mn和
②研究表明,加入适量的SeO2有利于Mn在电极上析出,机理为:SeO2与水反应生成的H2SeO3(二元弱酸)在阴极放电生成Se单质,该电极反应为
③电解废液可在上述流程的
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


