单选题 困难0.15 引用6 组卷1763
电位滴定法(potentiometric titration)是在滴定过程中通过测量电位变化以确定滴定终点的方法,当电极电位(ERC)产生了突跃,被测离子浓度产生突跃,进而确定滴定终点。向10mL 0.1
 溶液(
溶液( 为二元弱酸)中逐滴滴加0.1
为二元弱酸)中逐滴滴加0.1 二元酸
二元酸 溶液,第一个电位突跃时消耗a mL
溶液,第一个电位突跃时消耗a mL 溶液,第二个电位突跃时又消耗b mL
溶液,第二个电位突跃时又消耗b mL 溶液,根据消耗
溶液,根据消耗 溶液体积,可判断
溶液体积,可判断 和
和 各级电离常数大小关系。下列说法错误的是
各级电离常数大小关系。下列说法错误的是
| A.若a=5mL、b=5mL, |
| B.若a=5mL、b=15mL,则 |
| C.若a=5mL、b=15mL,第一个电位突跃时,溶液中: |
| D.若a=10mL、b=10mL,则用0.1 |
2022·山东·模拟预测
类题推荐
25℃时,向10mL0.2mol·L-1的H3R溶液中滴加0.2mol·L-1的NaOH溶液,pH曲线如图所示。判断多元弱酸滴定中的突跃个数以及能否被准确滴定的方法(以二元弱酸为例):若cKa1≥10-8(c代表弱酸的浓度、K代表弱酸的电离平衡常数),且 ≥104,则可分步滴定至第1终点,产生第1个突跃;若同时cKa2≥10-8,则可继续滴定至第2终点,产生第2个突跃;若cKa1和cKa2都大于10-8,但
≥104,则可分步滴定至第1终点,产生第1个突跃;若同时cKa2≥10-8,则可继续滴定至第2终点,产生第2个突跃;若cKa1和cKa2都大于10-8,但 <104,则只能滴定到第2终点,产生1个突跃;对于其他多元弱酸分步滴定的判断,方法类似。下列说法不正确的是
<104,则只能滴定到第2终点,产生1个突跃;对于其他多元弱酸分步滴定的判断,方法类似。下列说法不正确的是
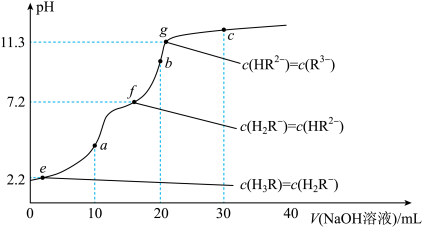

| A.Ka1(H3R)=10-2.2 |
| B.b点溶液中,c(R3-)+c(OH-)=c(H+)+c(H2R-)+2c(H3R) |
| C.NaOH溶液滴定H3R溶液过程中,可分3步滴定,产生3个滴定突跃 |
| D.H3R溶液第一步滴定可用酚酞作指示剂 |
25℃时,向10mL0.2mol•L-1的H3R溶液中滴加0.2mol•L-1的NaOH溶液,pH曲线如图所示。判断多元弱酸滴定中的突跃个数以及能否被准确滴定的方法(以二元弱酸为例):若cKa1≥10-8(c代表弱酸的浓度、K代表弱酸的电离平衡常数),且 ≥104,则可分步滴定至第1终点,产生第1个突跃;若同时cKa2≥10-8,则可继续滴定至第2终点,产生第2个突跃;若cKa1和cKa2都大于10-8,但
≥104,则可分步滴定至第1终点,产生第1个突跃;若同时cKa2≥10-8,则可继续滴定至第2终点,产生第2个突跃;若cKa1和cKa2都大于10-8,但 <104,则只能滴定到第2终点,产生1个突跃;对于其他多元弱酸分步滴定的判断,方法类似。下列说法错误的是
<104,则只能滴定到第2终点,产生1个突跃;对于其他多元弱酸分步滴定的判断,方法类似。下列说法错误的是
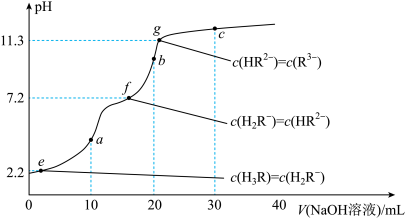

| A.Ka1(H3R)=10-2.2 |
| B.b点溶液中,c(R3-)+c(H+)=c(OH-)+c(H2R-)+2c(H3R) |
| C.NaOH溶液滴定H3R溶液过程中,可分3步滴定,产生3个滴定突跃 |
| D.H3R溶液第二步滴定可用酚酞作指示剂 |
电位滴定法是根据滴定过程中指示电极电位的变化来确定滴定终点的一种滴定分析方法。在化学计量点附近,被测离子浓度发生突跃,指示电极电位也产生了突跃,进而确定滴定终点。常温下,利用cmol·L-1盐酸标准溶液滴定VmL某溶液中碳酸钠的含量(假设其他物质均不反应且不含钠、碳元素),其电位滴定曲线与pH曲线如图所示(已知碳酸的电离常数Ka1=10-6.35,Ka2=10-10.34,不考虑CO2的逸出及溶液中的CO2)。下列说法错误的是
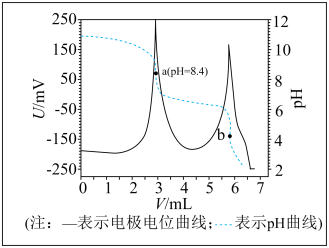

| A.a点溶液中c( |
| B.b点溶液中存在: |
| C.由a点至b点的过程中,水的电离程度逐渐减小 |
| D.若a点至b点消耗xmL盐酸,则VmL该溶液中Na2 CO3的质量为0.l06cxg |
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


