解答题-结构与性质 适中0.65 引用2 组卷219
铝的单质、合金及其化合物在生产、生活中具有广泛的应用。
(1)Al属于周期表中_______ 区元素,其基态原子核外具有_______ 种空间运动状态不同的电子。
(2)与Al位于同一周期,且第一电离能比Al小的元素有_______ (填元素符号)。
(3)一般认为:如果两个成键元素间的电负性差值大于1.7,它们之间通常形成离子键;如果两个成键元素间的电负性差值小于1.7,它们之间通常形成共价键。部分主族元素的电负性如下表所示:
下列含铝化合物属于离子化合物的是_______(填标号)。
(4)Al的熔点为660℃,Ga的熔点为29.76℃,Al的熔点更高的原因为_______ 。
(5)三甲基铝(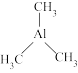 )是一种金属有机化合物,可作烯烃聚合催化剂、引火燃料。
)是一种金属有机化合物,可作烯烃聚合催化剂、引火燃料。
①三甲基铝分子中C原子的VSEPR模型为_______ ,Al原子的杂化轨道类型为_______ 。
②该物质可与胺类( ,R表示烃基)结合,原因是
,R表示烃基)结合,原因是_______ 。
(6)X-射线衍射实验表明,合金Cr-Al晶体(有序)属四方晶系,其晶胞参数如图所示,晶胞棱边夹角均为90°。
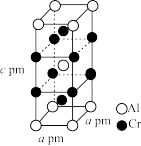
①该合鑫Cr-Al晶体的化学式为_______ 。
②用NA表示阿伏加德罗常数的值,则合金Cr-Al晶体的密度为_______  (写出计算式即可,不要求化简)。
(写出计算式即可,不要求化简)。
(1)Al属于周期表中
(2)与Al位于同一周期,且第一电离能比Al小的元素有
(3)一般认为:如果两个成键元素间的电负性差值大于1.7,它们之间通常形成离子键;如果两个成键元素间的电负性差值小于1.7,它们之间通常形成共价键。部分主族元素的电负性如下表所示:
| 5 B 2.0 | 6 C 2.5 | 7 N 3.0 | 8 O 3.5 | 9 F 4.0 |
| 13 Al 1.5 | 14 Si 1.8 | 15 P 2.1 | 16 S 2.5 | 17 Cl 3.0 |
| 31 Ga 1.6 | 32 Ge 1.8 | 33 As 2.0 | 34 Se 2.4 | 35 Br 2.8 |
| A. | B. | C. | D.AlP |
(5)三甲基铝(
 )是一种金属有机化合物,可作烯烃聚合催化剂、引火燃料。
)是一种金属有机化合物,可作烯烃聚合催化剂、引火燃料。①三甲基铝分子中C原子的VSEPR模型为
②该物质可与胺类(
(6)X-射线衍射实验表明,合金Cr-Al晶体(有序)属四方晶系,其晶胞参数如图所示,晶胞棱边夹角均为90°。

①该合鑫Cr-Al晶体的化学式为
②用NA表示阿伏加德罗常数的值,则合金Cr-Al晶体的密度为
2022·河北张家口·三模
类题推荐
铁被称为“第一金属”,硫被称为“生命元素”,它们形成的物质种类非常丰富,在生产、生活中用途广泛。
(1)基态S原子有___ 种能量不同的电子,其价电子排布图为___ 。
(2)硫能形成S2O 、SO
、SO 等多种含氧酸根,试推测S2O
等多种含氧酸根,试推测S2O 的空间构型为
的空间构型为___ ,SO 的中心原子杂化方式为
的中心原子杂化方式为___ 。
(3)SCN-与Fe3+能发生显色反应,该反应常用作检验Fe3+的存在。
①铁元素位于元素周期表的___ 区。
②SCN-的三种元素的电负性由大到小的顺序为___ (用元素符号表示)。写出与SCN-互为等电子体的分子的分子式___ (任写一种)。
③Fe(SCN)3中不存在的化学键有___ (填标号)。
A.离子键B.极性键C.非极性键D.配位键E.σ键F.π键
(4)部分卤化铁的熔点如下表所示:
解释表中物质之间熔点差异的原因___ 。
(5)某种离子型铁的氧化物晶胞如图所示,它由A、B两种方块组成。
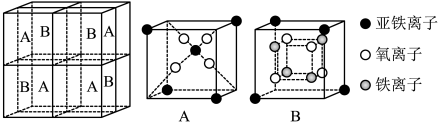
①该氧化物中Fe2+、Fe3+、O2-个数的最简整数比为___ 。
②已知该晶体的密度为dg·cm-3,阿伏加 德罗常数的值为NA,则晶胞参数a为___ nm(用含d和NA的代数式表示)。
(1)基态S原子有
(2)硫能形成S2O
(3)SCN-与Fe3+能发生显色反应,该反应常用作检验Fe3+的存在。
①铁元素位于元素周期表的
②SCN-的三种元素的电负性由大到小的顺序为
③Fe(SCN)3中不存在的化学键有
A.离子键B.极性键C.非极性键D.配位键E.σ键F.π键
(4)部分卤化铁的熔点如下表所示:
| 卤化铁 | FeF3 | FeCl3 |
| 熔点/℃ | 1100 | 306 |
解释表中物质之间熔点差异的原因
(5)某种离子型铁的氧化物晶胞如图所示,它由A、B两种方块组成。

①该氧化物中Fe2+、Fe3+、O2-个数的最简整数比为
②已知该晶体的密度为dg·cm-3,阿伏加 德罗常数的值为NA,则晶胞参数a为
K、Al、Si、Cu、N i均为重要的合金材料,在工业生产、科技、国防领域有着广泛的用途,请回答下列问题:
(1)K元素处于元素周期表的_____ 区。
(2)下列状态的铝中,电离最外层一个电子所需能量最大的是______ (填标号)。
A. [Ne] B. [Ne]
B. [Ne]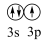 C. [Ne]
C. [Ne] 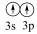 D. [Ne]
D. [Ne]
(3)从核外电子排布角度解释高温下Cu2O比CuO更稳定的原因是_____________ 。
(4)一些化合物的熔点如下表所示:
解释表中化合物之间熔点差异的原因________________________________ 。
(5)NiSO4溶于氨水形成[Ni (NH3)6]SO4。
①N、O、S三种元素中电负性最大的是_______ 。
②写出一种与[Ni (NH3)6]SO4中的阴离子互为等电子体的分子的分子式_________ 。
③1mol[Ni (NH3)6]SO4中含有δ键的数目为___________ 。
④NH3的VSEPR模型为____ ;NH3、SO42-的中心原子的杂化类型分别为___ 、___ 。
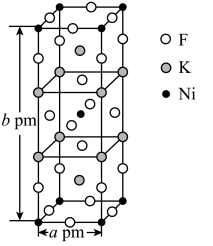
(6)K、Ni、F三种元素组成的一种晶体的长方体晶胞结构如图所示。若NA为阿伏加 德罗常数的值,该晶体的密度ρ=______ g·cm-3(用代数式表示)。
(1)K元素处于元素周期表的
(2)下列状态的铝中,电离最外层一个电子所需能量最大的是
A. [Ne]
 B. [Ne]
B. [Ne] C. [Ne]
C. [Ne]  D. [Ne]
D. [Ne]
(3)从核外电子排布角度解释高温下Cu2O比CuO更稳定的原因是
(4)一些化合物的熔点如下表所示:
| 化合物 | NaCl | KCl | SiO2 |
| 熔点/°C | 801 | 770 | 1723 |
解释表中化合物之间熔点差异的原因
(5)NiSO4溶于氨水形成[Ni (NH3)6]SO4。
①N、O、S三种元素中电负性最大的是
②写出一种与[Ni (NH3)6]SO4中的阴离子互为等电子体的分子的分子式
③1mol[Ni (NH3)6]SO4中含有δ键的数目为
④NH3的VSEPR模型为

(6)K、Ni、F三种元素组成的一种晶体的长方体晶胞结构如图所示。若NA为阿伏加 德罗常数的值,该晶体的密度ρ=
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网