解答题-结构与性质 适中0.65 引用1 组卷211
我国是世界上最早制得和使用铜的国家,铜及其化合物在日常生产和生活中有着广泛的应用。回答下列问题:
(1)Cu在元素周期表中位_______ 区,基态Cu2+价层电子的电子排布图(轨道表达式)为_______ 。
(2)由Cu2+形成的配合物种类繁多,在配离子[Cu(NH3)4]2+中,其配体的立体构型为_______ , 在[Cu(CN)4] 2−中,与其配体互为等电子体的一种分子是_______ (写化学式)。
(3)Cu2+能与吡咯(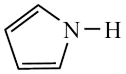 )的阴离子(
)的阴离子(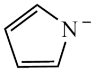 )形成双吡咯铜。
)形成双吡咯铜。
① 中C和N原子的杂化均为
中C和N原子的杂化均为_______ 。
②1mol 含有
含有_______ molσ键,分子中的大π键可用符号π 表示,其中m代表参与形成的大π键原子数,n代表参与形成的大π键电子数(如苯分子中的大π键可表示为π
表示,其中m代表参与形成的大π键原子数,n代表参与形成的大π键电子数(如苯分子中的大π键可表示为π ,则
,则 中的大π键应表示为
中的大π键应表示为_______ 。
(4)试从原子结构角度解释在高温下CuO能分解生成Cu2O的原因_______ 。
(5)高温超导体“钇钡铜氧”广泛应用于超导输电、磁悬浮列车等,其晶胞结构如图:
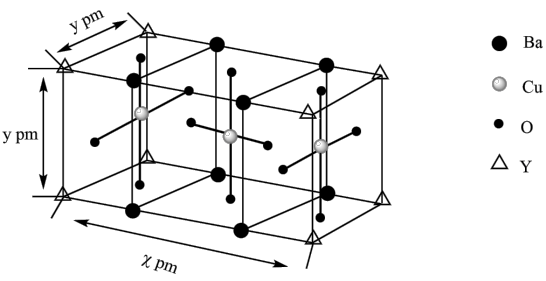
该物质以Y2O3、BaCO3和CuO为原料烧结而成,其原料物质的量之比为_______ ,若阿伏加德罗常数的值为NA,则该晶体的密度为_______ g·cm−3(列出计算表达式)。
(1)Cu在元素周期表中位
(2)由Cu2+形成的配合物种类繁多,在配离子[Cu(NH3)4]2+中,其配体的立体构型为
(3)Cu2+能与吡咯(
 )的阴离子(
)的阴离子( )形成双吡咯铜。
)形成双吡咯铜。①
 中C和N原子的杂化均为
中C和N原子的杂化均为②1mol
 含有
含有 中的大π键应表示为
中的大π键应表示为(4)试从原子结构角度解释在高温下CuO能分解生成Cu2O的原因
(5)高温超导体“钇钡铜氧”广泛应用于超导输电、磁悬浮列车等,其晶胞结构如图:

该物质以Y2O3、BaCO3和CuO为原料烧结而成,其原料物质的量之比为
2022·吉林·三模
类题推荐
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网
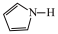 )的阴离子(
)的阴离子(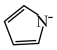 )形成双吡咯铜。
)形成双吡咯铜。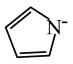 中C和N原子的杂化均为
中C和N原子的杂化均为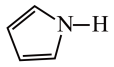 含有
含有 )2中含有的化学键有
)2中含有的化学键有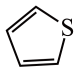 )的沸点为84℃,吡咯(
)的沸点为84℃,吡咯(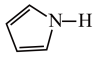 )的沸点在129 ~131℃之间,吡咯沸点较高,其原因是
)的沸点在129 ~131℃之间,吡咯沸点较高,其原因是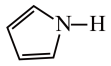 中的大
中的大
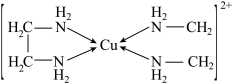 则H、O、N三种元素的电负性从大到小的顺序为
则H、O、N三种元素的电负性从大到小的顺序为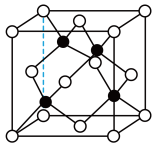
 ,可以HCHO、
,可以HCHO、 及(NH4)2SO4等为原料合成。
及(NH4)2SO4等为原料合成。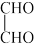 分子中σ键与π键的数目之比为
分子中σ键与π键的数目之比为 中形成的大π键的电子数为
中形成的大π键的电子数为


