解答题-实验探究题 较易0.85 引用1 组卷211
某学生用0.1000 mol∙L−1NaOH溶液测定某未知浓度的盐酸溶液,完成以下填空:
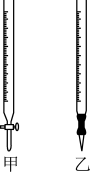
(1)盛装氢氧化钠溶液应该选择图中滴定管____ (填标号)。
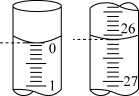
(2)若滴定开始和结束时,碱式滴定管中的液面如图所示,所用NaOH标准溶液的体积为____ mL。
(3)在上述实验中,下列操作会造成测定结果偏低的是____ (填序号)。
(4)氧化还原滴定实验与酸碱中和滴定类似(用已知浓度的氧化剂溶液滴定未知浓度的还原剂溶液或反之)。测血钙的含量时,进行如下实验:
①可将2mL血液用蒸馏水稀释后,向其中加入足量草酸铵(NH4)2C2O4晶体,反应生成CaC2O4沉淀,将沉淀用稀硫酸处理得H2C2O4溶液。
②将①得到的H2C2O4溶液,再用酸性KMnO4溶液滴定,氧化产物为CO2,还原产物为Mn2+。
③终点时用去24.00mL1.0×10−4 mol∙L−1L的KMnO4溶液。
I.判断滴定终点的方法____ 。
II.写出用KMnO4滴定H2C2O4的离子方程式:____ 。
III.计算:血液中含钙离子的浓度为____ mol∙L−1。
(1)盛装氢氧化钠溶液应该选择图中滴定管

(2)若滴定开始和结束时,碱式滴定管中的液面如图所示,所用NaOH标准溶液的体积为

(3)在上述实验中,下列操作会造成测定结果偏低的是
| A.锥形瓶水洗后未干燥 |
| B.滴定终点读数时俯视读数 |
| C.碱式滴定管尖嘴部分开始有气泡,滴定后消失 |
| D.酸式滴定管使用前,水洗后未用待测盐酸润洗 |
①可将2mL血液用蒸馏水稀释后,向其中加入足量草酸铵(NH4)2C2O4晶体,反应生成CaC2O4沉淀,将沉淀用稀硫酸处理得H2C2O4溶液。
②将①得到的H2C2O4溶液,再用酸性KMnO4溶液滴定,氧化产物为CO2,还原产物为Mn2+。
③终点时用去24.00mL1.0×10−4 mol∙L−1L的KMnO4溶液。
I.判断滴定终点的方法
II.写出用KMnO4滴定H2C2O4的离子方程式:
III.计算:血液中含钙离子的浓度为
21-22高二下·广西柳州·期中
类题推荐
(1)某学生用0.1500mol/LNaOH溶液测定某未知浓度的盐酸溶液,完成以下填空:
(1)滴定时边滴边摇动锥形瓶,眼睛应注意观察___ 。
(2)盛装氢氧化钠溶液应该选择图中滴定管___ (填标号)。


(3)滴定结果如表所示:
计算该盐酸的物质的量浓度为___ (精确至0.0001)。
(4)氧化还原滴定实验与酸碱中和滴定类似(用已知浓度的氧化剂溶液滴定未知浓度的还原剂溶液或反之)。测血钙的含量时,进行如下实验:
①可将2mL血液用蒸馏水稀释后,向其中加入足量草酸铵(NH4)2C2O4晶体,反应生成CaC2O4沉淀,将沉淀用稀硫酸处理得H2C2O4溶液。
②将①得到的H2C2O4溶液,再用酸性KMnO4溶液滴定,氧化产物为CO2,还原产物为Mn2+。
③终点时用去24mLl.0×l0-4mol/L的KMnO4溶液。
Ⅰ.判断滴定终点的方法是___ 。
Ⅱ.写出用KMnO4滴定H2C2O4的离子方程式___ 。
Ⅲ.计算:血液中含钙离子的浓度为___ mol/L。
(1)滴定时边滴边摇动锥形瓶,眼睛应注意观察
(2)盛装氢氧化钠溶液应该选择图中滴定管


(3)滴定结果如表所示:
| 滴定次数 | 待测液体积/mL | 标准溶液的体积/mL | |
| 滴定前刻度 | 滴定后刻度 | ||
| 1 | 25.00 | 1.02 | 21.03 |
| 2 | 25.00 | 0.60 | 20.60 |
| 3 | 25.00 | 0.20 | 20.19 |
(4)氧化还原滴定实验与酸碱中和滴定类似(用已知浓度的氧化剂溶液滴定未知浓度的还原剂溶液或反之)。测血钙的含量时,进行如下实验:
①可将2mL血液用蒸馏水稀释后,向其中加入足量草酸铵(NH4)2C2O4晶体,反应生成CaC2O4沉淀,将沉淀用稀硫酸处理得H2C2O4溶液。
②将①得到的H2C2O4溶液,再用酸性KMnO4溶液滴定,氧化产物为CO2,还原产物为Mn2+。
③终点时用去24mLl.0×l0-4mol/L的KMnO4溶液。
Ⅰ.判断滴定终点的方法是
Ⅱ.写出用KMnO4滴定H2C2O4的离子方程式
Ⅲ.计算:血液中含钙离子的浓度为
I.实验室中有一未知浓度的稀盐酸,某学生在实验室中进行测定盐酸浓度的实验。
(1)配制480mL0.1000mol·L-1NaOH标准溶液。
①配制所需的玻璃仪器有:烧杯、量筒、玻璃棒、___________ 、___________ 等。
②称取___________ g氢氧化钠固体所需仪器天平(砝码、镊子)、药匙、小烧杯。
(2)取20.00mL待测稀盐酸放入锥形瓶中,并滴加2~3滴酚酞作指示剂,用___________ (填仪器名称)盛装配制标准NaOH溶液进行滴定。重复上述滴定操作2〜3次,记录数据如下:
(3)①如何判断滴定终点:___________ 。
②根据上述数据,可计算出该盐酸的浓度约为___________ mol·L-1。
(4)在上述实验中,下列操作(其他操作正确)会造成测定果偏低的有___________ (填序号)。
A.酸式滴定管使用前,水洗后未用待测盐酸润洗
B.锥形瓶水洗后未干燥
C.称量NaOH固体中混有Na2CO3固体
D.滴定终点读数时俯视读数
E.碱式滴定管尖嘴部分有气泡,滴定后消失
II.氧化还原滴定实验与酸碱中和滴定类似(用已知浓度的氧化剂溶液滴定未知浓度的还原剂溶液或反之)。测血钙的含量时,进行如下实验:
①可将4mL血液用蒸馏水稀释后,向其中加入足量草酸铵(NH4)2C2O4晶体,反应生成CaC2O4沉淀,将沉淀用稀硫酸处理得H2C2O4溶液。
②将①得到的H2C2O4溶液,再用酸性KMnO4溶液滴定,氧化产物为CO2,还原产物为Mn2+。
③终点时用去20mLl.0×l0-4mol/L的KMnO4溶液。
(5)在进行滴定操作时,KMnO4溶液盛装在___________ (填“酸式”或“碱式”)滴定管中。滴入最后一滴酸性KMnO4溶液,___________ 达到滴定终点。
(6)写出H2C2O4溶液与酸性KMnO4溶液反应的离子方程式___________ 。
(7)计算:血液中含钙离子的浓度为___________ mol/L。
(1)配制480mL0.1000mol·L-1NaOH标准溶液。
①配制所需的玻璃仪器有:烧杯、量筒、玻璃棒、
②称取
(2)取20.00mL待测稀盐酸放入锥形瓶中,并滴加2~3滴酚酞作指示剂,用
| 滴定次数 | 待测盐酸 的体积/mL | 标准NaOH溶液体积 | |
| 滴定前的刻度/mL | 滴定后的刻度/rnL | ||
| 第一次 | 20.00 | 0.40 | 20.50 |
| 第二次 | 20.00 | 4.10 | 24.00 |
| 第三次 | 20.00 | 1.00 | 24.00 |
②根据上述数据,可计算出该盐酸的浓度约为
(4)在上述实验中,下列操作(其他操作正确)会造成测定果偏低的有
A.酸式滴定管使用前,水洗后未用待测盐酸润洗
B.锥形瓶水洗后未干燥
C.称量NaOH固体中混有Na2CO3固体
D.滴定终点读数时俯视读数
E.碱式滴定管尖嘴部分有气泡,滴定后消失
II.氧化还原滴定实验与酸碱中和滴定类似(用已知浓度的氧化剂溶液滴定未知浓度的还原剂溶液或反之)。测血钙的含量时,进行如下实验:
①可将4mL血液用蒸馏水稀释后,向其中加入足量草酸铵(NH4)2C2O4晶体,反应生成CaC2O4沉淀,将沉淀用稀硫酸处理得H2C2O4溶液。
②将①得到的H2C2O4溶液,再用酸性KMnO4溶液滴定,氧化产物为CO2,还原产物为Mn2+。
③终点时用去20mLl.0×l0-4mol/L的KMnO4溶液。
(5)在进行滴定操作时,KMnO4溶液盛装在
(6)写出H2C2O4溶液与酸性KMnO4溶液反应的离子方程式
(7)计算:血液中含钙离子的浓度为
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


