解答题-实验探究题 较难0.4 引用1 组卷295
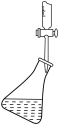
硫氰化钾(KSCN)俗称玫瑰红酸钾,是一种用途广泛的化学药品。实验室模拟工业制备硫氰化钾的实验装置如下图所示:

已知:① 不溶于水,密度比水的大;②
不溶于水,密度比水的大;② 不溶于
不溶于 ;③三颈烧瓶内盛放有
;③三颈烧瓶内盛放有 、水和催化剂。回答下列问题:
、水和催化剂。回答下列问题:
Ⅰ.制备 溶液:
溶液:
(1)实验前,经检验装置的气密性良好。其中装置B中的试剂是_______ 。三颈烧瓶的下层 液体必须浸没导气管口,目的是
液体必须浸没导气管口,目的是_______ 。
(2)实验开始时,打开 ,加热装置A、D,使A中产生的气体缓缓通入D中,发生反应:
,加热装置A、D,使A中产生的气体缓缓通入D中,发生反应: (该反应比较缓慢),当看到
(该反应比较缓慢),当看到_______ 现象时说明该反应接近完全。
Ⅱ.制备KSCN溶液:
(3)熄灭A处的酒精灯,关闭 ,移开水浴,将装置D继续加热至105℃,当
,移开水浴,将装置D继续加热至105℃,当 完全分解后(
完全分解后( ),打开
),打开 ,继续保持液温105℃,缓缓滴入适量的KOH溶液,发生反应的化学方程式为
,继续保持液温105℃,缓缓滴入适量的KOH溶液,发生反应的化学方程式为_______ 。
(4)使用KOH溶液会吸收装置中残留的 使产品KSCN中混有较多的
使产品KSCN中混有较多的 ,工业上用相同浓度的
,工业上用相同浓度的 溶液替换KOH溶液。已知
溶液替换KOH溶液。已知 与
与 在105℃反应会生成两种气体。分析使用
在105℃反应会生成两种气体。分析使用 溶液能减少杂质
溶液能减少杂质 的原因:
的原因:_______ 。
(5)装置E的作用_______ 。
Ⅲ.制备KSCN晶体
Ⅳ.测定晶体中KSCN的含量:称取10.0g样品,配成1000mL溶液。量取20.00mL溶液于锥形瓶中,加入适量稀硝酸,再加入几滴 溶液作指示剂,用0
溶液作指示剂,用0 标准溶液滴定,达到滴定终点时消耗
标准溶液滴定,达到滴定终点时消耗 ,标准溶液20.00mL。
,标准溶液20.00mL。
(6)滴定时发生的反应: (白色)。则判断到达滴定终点的方法是
(白色)。则判断到达滴定终点的方法是_______ 。
(7)晶体中KSCN的质量分数为_______ (计算结果精确至0.1%)。

已知:①
Ⅰ.制备
(1)实验前,经检验装置的气密性良好。其中装置B中的试剂是
(2)实验开始时,打开
Ⅱ.制备KSCN溶液:
(3)熄灭A处的酒精灯,关闭
(4)使用KOH溶液会吸收装置中残留的
(5)装置E的作用
Ⅲ.制备KSCN晶体
Ⅳ.测定晶体中KSCN的含量:称取10.0g样品,配成1000mL溶液。量取20.00mL溶液于锥形瓶中,加入适量稀硝酸,再加入几滴
(6)滴定时发生的反应:
(7)晶体中KSCN的质量分数为
21-22高三下·上海浦东新·阶段练习
类题推荐
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


 C.
C. D.
D.