解答题-实验探究题 适中0.65 引用2 组卷298
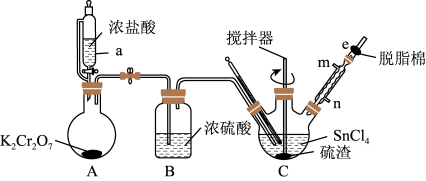
某课题小组利用硫渣与氯气反应制备四氯化锡,其过程如图所示(夹持、加热及控温装置略)。已知:四氯化锡(SnCl4)常温下为无色液体、易水解。
硫渣的化学组成
氯气与硫渣反应相关产物的熔沸点
(1)仪器a的名称_______ ,A中发生反应的化学方程式_______ 。
(2)e中所加物质为_______ ,作用为_______ 。
(3)装置中存在一处缺陷会导致SnCl4产率降低,改进的方法是_______ 。
(4)三颈烧瓶中得到的粗产品进行提纯的方法_______ ;提纯后剩余的固体渣经过处理,可回收的主要金属有_______ 。
(5)已知SnCl4产品中含有少量AsCl3杂质,碘量法可用于测量产品的纯度:取10. 00 g产品溶于水,加入0.100 mol/L标准I2溶液20. 00 mL,并加入少量的淀粉溶液;用0.100×10-2 mol/L的硫代硫酸钠标准溶液滴定过量的碘。滴定终点时消耗20. 00 mL硫代硫酸钠标准溶液。测定过程中发生的相关反应:
①AsCl3+3H2O= H3AsO3+ 3HCl
②H3AsO3+I2+H2O= H3AsO4+2HI
③2 +I2=2I-+
+I2=2I-+
则产品中SnCl4的质量分数_______ (保留小数点后1位);若滴定后发现滴管尖嘴处产生了气泡,则测量结果_______ (填“偏高”或“偏低”)。

硫渣的化学组成
| 物质 | Sn | Cu2S | Pb | As | 其他杂质 |
| 质量分数% | 64.43 | 25.82 | 7.34 | 1.23 | 1.18 |
物质 性质 | SnCl4 | CuCl | PbCl2 | AsCl3 | S |
| 熔点/℃ | -33 | 426 | 501 | -18 | 112 |
| 沸点/℃ | 114 | 1490 | 951 | 130 | 444 |
(2)e中所加物质为
(3)装置中存在一处缺陷会导致SnCl4产率降低,改进的方法是
(4)三颈烧瓶中得到的粗产品进行提纯的方法
(5)已知SnCl4产品中含有少量AsCl3杂质,碘量法可用于测量产品的纯度:取10. 00 g产品溶于水,加入0.100 mol/L标准I2溶液20. 00 mL,并加入少量的淀粉溶液;用0.100×10-2 mol/L的硫代硫酸钠标准溶液滴定过量的碘。滴定终点时消耗20. 00 mL硫代硫酸钠标准溶液。测定过程中发生的相关反应:
①AsCl3+3H2O= H3AsO3+ 3HCl
②H3AsO3+I2+H2O= H3AsO4+2HI
③2
则产品中SnCl4的质量分数
2022·山东德州·二模
类题推荐
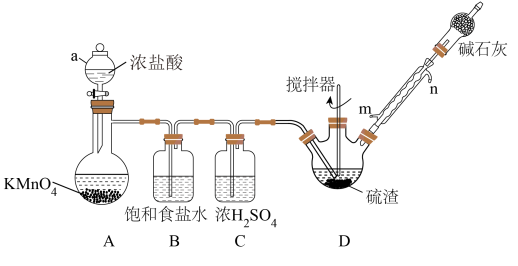
某实验小组利用硫渣(主要成分为Sn,含少量Cu2S、Pb、As等)与氯气反应制备四氯化锡,其过程如图所示(夹持、加热及控温装置略)。已知:SnCl4遇水极易水解。
相关产物的熔沸点:
(1)仪器a的名称___________ ,A中发生反应的化学方程式___________ 。
(2)冷凝管的进水口为___________ (填“m”或“n”),碱石灰的作用为___________ 。
(3)如果缺少B装置,可能造成的影响为___________ 。
(4)实验结束后,将三颈烧瓶中得到的物质冷却至室温,___________ (填操作名称,下同),得到粗产品,粗产品再___________ 可得到纯净的SnCl4。
(5)用碘量法测量粗产品的纯度:取10.00g粗产品溶于水,加入0.100mol·L-1标准I2溶液20.00mL,并加入少量的淀粉溶液:用 的硫代硫酸钠标准溶液滴定过量的碘。滴定终点时消耗20.00mL硫代硫酸钠标准溶液。测定过程中发生的相关反应:
的硫代硫酸钠标准溶液滴定过量的碘。滴定终点时消耗20.00mL硫代硫酸钠标准溶液。测定过程中发生的相关反应:
①
②
③
则产品中SnCl4的质量分数___________ (保留三位有效数字)。某同学认为粗产品中会溶有少量氯气,导致测量结果___________ (填“偏高”“偏低”或“无影响”)。

相关产物的熔沸点:
| 物质性质 | SnCl4 | SnCl2 | CuCl | PbCl2 | AsCl3 | S |
| 熔点/℃ | -33 | 246 | 426 | 501 | -18 | 112 |
| 沸点/℃ | 114 | 652 | 1490 | 951 | 130 | 444 |
(2)冷凝管的进水口为
(3)如果缺少B装置,可能造成的影响为
(4)实验结束后,将三颈烧瓶中得到的物质冷却至室温,
(5)用碘量法测量粗产品的纯度:取10.00g粗产品溶于水,加入0.100mol·L-1标准I2溶液20.00mL,并加入少量的淀粉溶液:用
①
②
③
则产品中SnCl4的质量分数
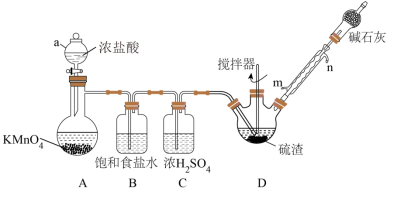
某实验小组利用硫渣(主要成分为Sn,含少量Cu2S、Pb、As等)与氯气反应制备四氯化锡,其过程如图所示(夹持、加热及控温装置略)。已知:SnCl4遇水极易水解。
相关产物的熔沸点:
(1)仪器a的名称___________ 。
(2)冷凝管的进水口为___________ (填“m”或“n”),碱石灰的作用为___________ 。
(3)如果缺少B装置,可能造成的影响为___________ 。
(4)实验结束后,将三颈烧瓶中得到的物质冷却至室温,___________ (填操作名称),得到粗产品,粗产品再精馏可得到纯净的SnCl4。
(5)用碘量法测量粗产品的纯度:取10.00g粗产品溶于水,加入0.100mol·L-1标准I2溶液20.00mL,并加入少量的淀粉溶液:用 的硫代硫酸钠标准溶液滴定过量的碘。滴定终点时消耗20.00mL硫代硫酸钠标准溶液。测定过程中发生的相关反应:
的硫代硫酸钠标准溶液滴定过量的碘。滴定终点时消耗20.00mL硫代硫酸钠标准溶液。测定过程中发生的相关反应:
①
②
③
则产品中SnCl4的质量分数___________ (保留三位有效数字)。

相关产物的熔沸点:
| 物质性质 | SnCl4 | SnCl2 | CuCl | PbCl2 | AsCl3 | S |
| 熔点/℃ | -33 | 246 | 426 | 501 | -18 | 112 |
| 沸点/℃ | 114 | 652 | 1490 | 951 | 130 | 444 |
(2)冷凝管的进水口为
(3)如果缺少B装置,可能造成的影响为
(4)实验结束后,将三颈烧瓶中得到的物质冷却至室温,
(5)用碘量法测量粗产品的纯度:取10.00g粗产品溶于水,加入0.100mol·L-1标准I2溶液20.00mL,并加入少量的淀粉溶液:用
①
②
③
则产品中SnCl4的质量分数
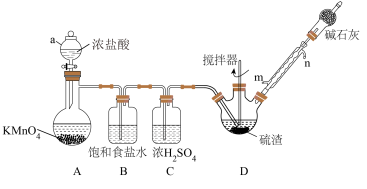
某实验小组利用硫渣(主要成分为Sn,含少量Cu2S、Pb、As等)与氯气反应制备四氯化锡,其过程如图所示(夹持、加热及控温装置略)。已知:SnCl4遇水极易反应。
相关产物的熔沸点:
(1)已知Sn的原子序数为50,则Sn在元素周期表中的位置为______ 。
(2)仪器a的名称______ 。
(3)A中发生反应的化学方程式为______ 。
(4)球形冷凝管的进水口为______ (选填“m”或“n”)。
(5)碱石灰的作用是______ 。
(6)SnCl4极易与水反应产生SnO2•xH2O胶体,请写出其化学方程式______ 。
(7)实验结束后,将三颈烧瓶中得到的物质冷却至室温,______ (填操作名称),得到粗产品,粗产品再______ 可得到纯净的SnCl4。
(8)用碘量法测量粗产品的纯度:取10.00g粗产品溶于水,加入0.100mol•L-1标准I2溶液30.00mL,并加入少量的淀粉溶液:用0.100mol•L-1的硫代硫酸钠标准溶液滴定过量的碘。滴定终点时消耗20.00mL硫代硫酸钠标准溶液。测定过程中发生的相关反应:
①AsCl3+3H2O=H3AsO3+3HCl
②H3AsO3+I2+H2O=H3AsO4+2HI
③2S2O +I2=2I-+S4O
+I2=2I-+S4O
则产品中SnCl4的纯度为______ 。(已知:AsCl3的摩尔质量为181.5g/mol)

相关产物的熔沸点:
| 物质性质 | SnCl4 | SnCl2 | CuCl | PbCl2 | AsCl3 | S |
| 熔点/℃ | -33 | 246 | 426 | 501 | -18 | 112 |
| 沸点/℃ | 114 | 652 | 1490 | 951 | 130 | 444 |
(1)已知Sn的原子序数为50,则Sn在元素周期表中的位置为
(2)仪器a的名称
(3)A中发生反应的化学方程式为
(4)球形冷凝管的进水口为
(5)碱石灰的作用是
(6)SnCl4极易与水反应产生SnO2•xH2O胶体,请写出其化学方程式
(7)实验结束后,将三颈烧瓶中得到的物质冷却至室温,
(8)用碘量法测量粗产品的纯度:取10.00g粗产品溶于水,加入0.100mol•L-1标准I2溶液30.00mL,并加入少量的淀粉溶液:用0.100mol•L-1的硫代硫酸钠标准溶液滴定过量的碘。滴定终点时消耗20.00mL硫代硫酸钠标准溶液。测定过程中发生的相关反应:
①AsCl3+3H2O=H3AsO3+3HCl
②H3AsO3+I2+H2O=H3AsO4+2HI
③2S2O
则产品中SnCl4的纯度为
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


