解答题-原理综合题 适中0.65 引用1 组卷200
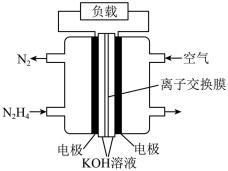
肼(分子式为N2H4,其结构简式为H2N-NH2)是一种应用广泛的化工原料。
(1)发射火箭时用肼为燃料,NO2(g)作氧化剂,两者反应生成氮气和气态水。已知16g N2H4(g)在上述反应中放出284kJ的热量,写出该反应的热化学方程式_______ 。
(2)肼能与N2O4发生如下反应: ,在四种不同情况下的反应速率如下:①
,在四种不同情况下的反应速率如下:① ;②
;② ;③
;③ ④
④ ,则反应速率由快到慢的顺序为
,则反应速率由快到慢的顺序为_______ (用序号表示)。
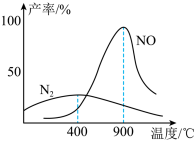
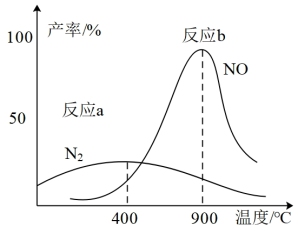
(3)肼和氧气在不同温度和催化剂的恒容密闭容器中生成不同产物(如下图):
温度较低时主要发生反应a:
温度较高时主要发生反应b:
①反应a的化学平衡常数K的表达式为K=_______ 。
②下列有关反应a: 的说法,能说明该反应已达到平衡状态的是
的说法,能说明该反应已达到平衡状态的是_______ 。
a.
b.容器内压强保持不变
c.混合气体的密度保持不变
d.断裂 的同时,有
的同时,有 断裂
断裂
e.容器内 的浓度之比为
的浓度之比为
③若反应b在1000℃时的平衡常数为K1,1100℃时的平衡常数为K2,则K1_______ K2(填“<”、“>”或“=”)。
④1000℃,反应b达到平衡时,下列措施能使容器中 增大的是
增大的是_______ 。
A.恒容条件下,充入 B.恒压条件下,充入
B.恒压条件下,充入
C.缩小容器体积 D.使用催化剂
(1)发射火箭时用肼为燃料,NO2(g)作氧化剂,两者反应生成氮气和气态水。已知16g N2H4(g)在上述反应中放出284kJ的热量,写出该反应的热化学方程式
(2)肼能与N2O4发生如下反应:
(3)肼和氧气在不同温度和催化剂的恒容密闭容器中生成不同产物(如下图):

温度较低时主要发生反应a:
温度较高时主要发生反应b:
①反应a的化学平衡常数K的表达式为K=
②下列有关反应a:
a.
b.容器内压强保持不变
c.混合气体的密度保持不变
d.断裂
e.容器内
③若反应b在1000℃时的平衡常数为K1,1100℃时的平衡常数为K2,则K1
④1000℃,反应b达到平衡时,下列措施能使容器中
A.恒容条件下,充入
C.缩小容器体积 D.使用催化剂
21-22高二下·江苏常州·期中
类题推荐
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网