填空题 较易0.85 引用2 组卷252
在微电子工业中, 作为一种优良的蚀刻气体,在被蚀刻物表面不会留下任何残留物,在芯片制造方面具有重要的应用。已知:键能是指断裂或形成
作为一种优良的蚀刻气体,在被蚀刻物表面不会留下任何残留物,在芯片制造方面具有重要的应用。已知:键能是指断裂或形成 化学键时需要吸收或放出的能量。请回答下列问题:
化学键时需要吸收或放出的能量。请回答下列问题:
(1)几种化学键的键能如表,则 、
、 和
和 三种气体中,稳定性最强的物质为
三种气体中,稳定性最强的物质为_______ (填化学式),判断的依据为_______ ;反应 生成
生成 时,会
时,会_______ (填“吸收”或“放出”)_______ kJ能量
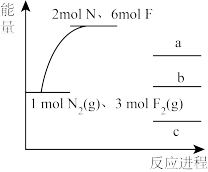
(2)根据上述数据,反应 的能量变化与反应进程的关系如图,图中表示
的能量变化与反应进程的关系如图,图中表示 的能量是
的能量是_______ (填“a”、“b”或“c”);除选用合适的催化剂加快化学反应速率,还可以采取的措施为_______ 、_______ (请任写两条)
| 化学键 | F−F | N−F | |
| 键能/ | 941.7 | 154.8 | 283.0 |
(2)根据上述数据,反应

21-22高一下·云南·期中
知识点:化学键与化学反应中的能量关系根据△H=反应物的键能之和-生成物的键能之和进行计算压强对化学反应速率的影响温度对化学反应速率的影响 答案解析 【答案】很抱歉,登录后才可免费查看答案和解析! 立即登录
类题推荐
化学反应伴随着能量变化。根据所学知识,回答下列问题:
(1) 和
和 均是有害气体,可在
均是有害气体,可在 表面转化为无害气体,其反应原理如下:
表面转化为无害气体,其反应原理如下: 
 。有关化学反应的能量变化过程如图所示。
。有关化学反应的能量变化过程如图所示。___________ (填“放热”或“吸热”)反应,该正反应的活化能为___________  。该反应的
。该反应的
___________  。
。
②若在反应体系中加入 作为该反应的催化剂,则
作为该反应的催化剂,则
___________ (填“增大”、“减小”或“不变”,下同),
___________ 。
(2)利用 还原法可将
还原法可将 还原为
还原为 进行脱除。已知:
进行脱除。已知:

 。若有0.5mol NO被还原,则该反应
。若有0.5mol NO被还原,则该反应___________ (填“释放”或“吸收”)的能量为___________ 。
(3)生产液晶显示器的过程中使用的化学清洗剂 是一种温室气体,在大气中寿命可达740年之久。
是一种温室气体,在大气中寿命可达740年之久。
①已知:键能是指断开(或生成)1mol化学键所需要吸收(或放出)的能量。部分键能数据如下表所示。
则

___________ 
②已知:在25℃,101kPa时。反应I.

 ;
;
反应II.
 。
。
写出 与Na反应生成
与Na反应生成 的热化学方程式:
的热化学方程式:___________ 。
(1)

②若在反应体系中加入
(2)利用
(3)生产液晶显示器的过程中使用的化学清洗剂
①已知:键能是指断开(或生成)1mol化学键所需要吸收(或放出)的能量。部分键能数据如下表所示。
| 化学键 | N≡N | F—F | N—F |
| 键能/( | 941.7 | 154.8 | 283.0 |
②已知:在25℃,101kPa时。反应I.
反应II.
写出
如图表示1molNO2(g)和1molCO(g)反应生成CO2和NO过程中的能量变化示意图,已知E1=134kJ•mol-1、E2=368kJ•mol-1。
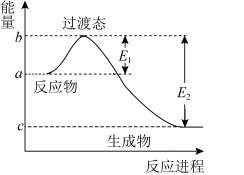
(1)若在反应体系中加入催化剂,反应速率增大,E1的变化是____ (填“增大”、“减小”或“不变”,下同),△H的变化是_____ 。
(2)请写出NO2和CO反应的热化学方程式:_____ 。
(3)当上述反应中放出46.8kJ的热量时,生成标准状况下二氧化碳的体积_____ 。
(4)已知甲醇是重要的化工原料。利用合成气(主要成分为CO、CO2和H2)在催化剂的作用下合成甲醇,可能发生的反应如下:
①CO2(g)+3H2(g)=CH3OH(g)+H2O(g) △H1
②CO2(g)+H2(g)=CO(g)+H2O(g) △H2
③CH3OH(g)=CO(g)+2H2(g) △H3
已知反应②中相关化学键键能(断裂或形成1mol化学键吸收或放出的能量)数据如表所示:
由此计算△H2=_____ kJ•mol-1。已知△H3=+99kJ•mol-1,则△H1=_____ kJ•mol-1。

(1)若在反应体系中加入催化剂,反应速率增大,E1的变化是
(2)请写出NO2和CO反应的热化学方程式:
(3)当上述反应中放出46.8kJ的热量时,生成标准状况下二氧化碳的体积
(4)已知甲醇是重要的化工原料。利用合成气(主要成分为CO、CO2和H2)在催化剂的作用下合成甲醇,可能发生的反应如下:
①CO2(g)+3H2(g)=CH3OH(g)+H2O(g) △H1
②CO2(g)+H2(g)=CO(g)+H2O(g) △H2
③CH3OH(g)=CO(g)+2H2(g) △H3
已知反应②中相关化学键键能(断裂或形成1mol化学键吸收或放出的能量)数据如表所示:
| 化学键 | H-H | C=O | C≡O | H-O |
| E/kJ•mol-1 | 436 | 803 | 1076 | 465 |
由此计算△H2=
Ⅰ.断开1 mol AB(g)分子中的化学键使其分别生成气态A原子和气态B原子所吸收的能量称为A—B的键能。下表列出了一些化学键的键能(E):
请回答下列问题:
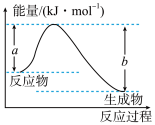
(1)如图表示某反应的能量变化关系,则此反应为___________ (填“吸收”或“放出”) ___________ kJ能量(用含有a、b的关系式表示)。
(2)反应H2(g)+ O2(g)=H2O(g)放出241.8 kJ能量,则根据所给键能数据可得x=
O2(g)=H2O(g)放出241.8 kJ能量,则根据所给键能数据可得x=___________ 。
(3)历史上曾用“地康法”制氯气,这一方法是用CuCl2作催化剂,在450 ℃时利用空气中的氧气与氯化氢反应制氯气。反应的化学方程式为___________ 。
II.工业上用CO生产燃料甲醇,一定条件下发生反应:CO(g)+2H2(g) CH3OH(g),反应过程中的能量变化情况如图所示。曲线I和曲线II分别表示不使用催化剂和使用催化剂的两种情况。
CH3OH(g),反应过程中的能量变化情况如图所示。曲线I和曲线II分别表示不使用催化剂和使用催化剂的两种情况。
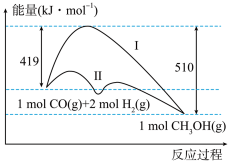
(4)计算当反应生成1.5molCH3OH(g)时,能量变化值是___________ kJ。
(5)推测反应CH3OH(g)⇌CO(g)+2H2(g)是___________ (填“吸热”或“放热”)反应。
Ⅲ.化学键的键能是形成(或断开)1 mol化学键时释放(或吸收)的能量。已知白磷和P4O6的分子结构如图所示:现提供以下化学键的键能(kJ·mol-1):P-P:198;P-O:360;O=O:498。
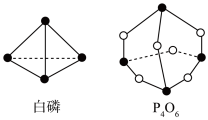
(6)则发生P4(白磷)+3O2(g)=P4O6(s)的反应,其中,生成1 mol P4O6需要___________ (“吸收或放出”)能量为___________ kJ
| 化学键 | H—H | Cl—Cl | O=O | C—Cl | C—H | O—H | H—Cl |
| E/(kJ·mol-1) | 436 | 247 | x | 330 | 413 | 463 | 431 |

(1)如图表示某反应的能量变化关系,则此反应为
(2)反应H2(g)+
(3)历史上曾用“地康法”制氯气,这一方法是用CuCl2作催化剂,在450 ℃时利用空气中的氧气与氯化氢反应制氯气。反应的化学方程式为
II.工业上用CO生产燃料甲醇,一定条件下发生反应:CO(g)+2H2(g)

(4)计算当反应生成1.5molCH3OH(g)时,能量变化值是
(5)推测反应CH3OH(g)⇌CO(g)+2H2(g)是
Ⅲ.化学键的键能是形成(或断开)1 mol化学键时释放(或吸收)的能量。已知白磷和P4O6的分子结构如图所示:现提供以下化学键的键能(kJ·mol-1):P-P:198;P-O:360;O=O:498。

(6)则发生P4(白磷)+3O2(g)=P4O6(s)的反应,其中,生成1 mol P4O6需要
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


