解答题-工业流程题 较难0.4 引用2 组卷183
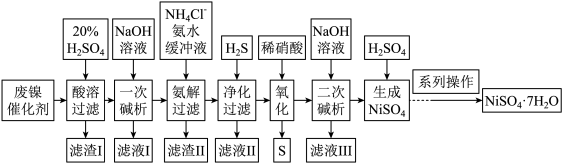
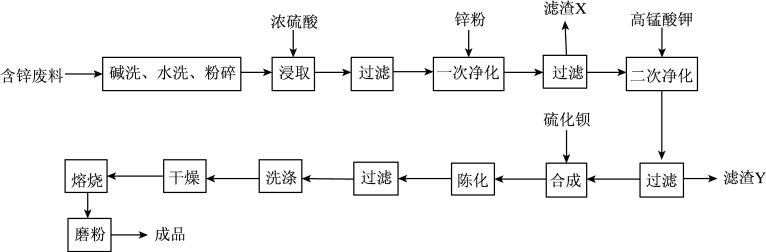
立德粉为ZnS和BaSO4的混合物,是通过硫酸锌和硫化钡合成制备。用含锌废料(主要成分为ZnO,含少量铜、铅、铁、锰的氧化物)制备立德粉的工艺流程如下:
已知:MnO2是两性氧化物,25℃时相关物质的Ksp见下表。
回答下列问题:
(1)硫酸锌溶液的粗制:取一定质量处理后的含锌废料于烧杯中,以固:水=3:1混合,在60~70℃下搅拌并缓慢加入硫酸。当pH=5左右停止加硫酸,控制温度为80~90℃,继续搅拌45min,使样品溶解趋于完全,终点的pH应为5.2~5.4。上述实验过程中,可采用的加热方式为_______ ,若终点处酸度不宜过高或过低,原因是_______ 。
(2)硫酸锌溶液的精制:“一次净化”时,滤渣X的成分主要是_______ 。“二次净化”时,加入高锰酸钾发生反应的离子方程式为_______ ,“二次净化”后过滤所得滤液的pH不低于_______ 。(杂质离子浓度低于10-5mol·L-1认为完全沉淀)
(3)“合成”时反应的化学方程式为_______ 。

已知:MnO2是两性氧化物,25℃时相关物质的Ksp见下表。
| 物质 | Fe(OH)2 | Fe(OH)3 | Mn(OH)2 | Zn(OH)2 |
| Ksp | 1×10-16.3 | 1×10-38.0 | 1×10-12.7 | 1×10-16.2 |
(1)硫酸锌溶液的粗制:取一定质量处理后的含锌废料于烧杯中,以固:水=3:1混合,在60~70℃下搅拌并缓慢加入硫酸。当pH=5左右停止加硫酸,控制温度为80~90℃,继续搅拌45min,使样品溶解趋于完全,终点的pH应为5.2~5.4。上述实验过程中,可采用的加热方式为
(2)硫酸锌溶液的精制:“一次净化”时,滤渣X的成分主要是
(3)“合成”时反应的化学方程式为
21-22高三下·湖南岳阳·阶段练习
类题推荐
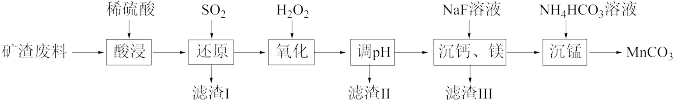
某工业矿渣废料的主要成分为SiO2、MnO2和Fe2O3,还含有少量CaO和MgO。利用该矿渣废料制备高纯MnCO3和回收含铁化合物的工业流程如下:
已知:i.当微粒浓度低于10-5mol·L1时,认为溶液中不存在该微粒;
ⅱ.常温下,部分难溶物的溶度积常数如下表:
回答下列问题:
(1)“滤渣I”的成分为___________ (填化学式,下同);流程最终回收的含铁化合物为___________ 。
(2)通入SO2“还原”时需要不断搅拌,不断搅拌的目的为___________ ,该过程中发生的主要氧化还原反应的离子方程式为___________ 。
(3)“氧化”时需要少量、多次加入H2O2,其目的是___________ 。
(4)“调pH”时可选择的试剂为___________ (填字母)。
A.MnO2 B.Fe2O3 C.NH3·H2O D.FeO
(5)常温下,若“调pH”后所得溶液中c(Mn2+)=0.2 mol·L-1、c(Mg2+)=0.002 mol·L-1,则所调pH的范围为___________ 。
(6)“沉锰”时发生反应的离子方程式为___________ 。

已知:i.当微粒浓度低于10-5mol·L1时,认为溶液中不存在该微粒;
ⅱ.常温下,部分难溶物的溶度积常数如下表:
| 难溶物 | Fe(OH)3 | Fe(OH)2 | Mn(OH)2 | Mg(OH)2 |
| Ksp | 1×10-38 | 1×10-16 | 2×10-13 | 2×10-25 |
(1)“滤渣I”的成分为
(2)通入SO2“还原”时需要不断搅拌,不断搅拌的目的为
(3)“氧化”时需要少量、多次加入H2O2,其目的是
(4)“调pH”时可选择的试剂为
A.MnO2 B.Fe2O3 C.NH3·H2O D.FeO
(5)常温下,若“调pH”后所得溶液中c(Mn2+)=0.2 mol·L-1、c(Mg2+)=0.002 mol·L-1,则所调pH的范围为
(6)“沉锰”时发生反应的离子方程式为
工业上以锌白矿(主要成分为ZnO,还含有PbO、FeO、Fe2O3、CuO、SiO2等杂质)为主要原料制备硫酸锌的工艺流程如图。回答下列问题:

已知:
①某温度下,部分金属阳离子开始沉淀和完全沉淀时的pH值如图:

②硫酸锌晶体的溶解度随温度的变化如图:

(1)“酸浸”时,需不断通入高温水蒸气,其目的是____ ,用到的4.5mol·L-1的硫酸溶液需用18mol·L-1的浓硫酸配制。下列操作使所配溶液浓度偏大的是____ (填字母)。

(2)滤渣1的主要成分是____ ,调节pH时可使用物质B是____ (填化学式)。
(3)从滤液2经一系列操作可得产品级ZnSO4·7H2O,具体操作如图:

滤液2调节pH值沉锌的范围是9.4~____ ,简述从滤液3得到产品级ZnSO4·7H2O的操作:____ ,冷却结晶、过滤、洗涤、干燥。
将硫酸锌与硫化钡混合可以得到很好的白色颜料——锌钡白(俗称:立德粉ZnS·ZnSO4)。由于锌钡白便宜可部分替代TiO2使用,稳定性:TiO2____ 锌钡白(填“大于”或“小于”)。
(4)该工艺废水中含有Zn2+,排放前需处理。向废水中加入CH3COOH和CH3COONa组成的缓冲溶液调节pH,通入H2S发生反应:Zn2++H2S ZnS(s)+2H+。处理后的废水中部分微粒浓度为:
ZnS(s)+2H+。处理后的废水中部分微粒浓度为:
则处理后的废水中c(Zn2+)=____ 。(已知:Ksp(ZnS)=1.0×10-23,Ka1(H2S)=1.0×10-7,Ka2(H2S)=1.0×10-14,Ka(CH3COOH)=2.0×10-5)

已知:
①某温度下,部分金属阳离子开始沉淀和完全沉淀时的pH值如图:

②硫酸锌晶体的溶解度随温度的变化如图:

(1)“酸浸”时,需不断通入高温水蒸气,其目的是

(2)滤渣1的主要成分是
(3)从滤液2经一系列操作可得产品级ZnSO4·7H2O,具体操作如图:

滤液2调节pH值沉锌的范围是9.4~
将硫酸锌与硫化钡混合可以得到很好的白色颜料——锌钡白(俗称:立德粉ZnS·ZnSO4)。由于锌钡白便宜可部分替代TiO2使用,稳定性:TiO2
(4)该工艺废水中含有Zn2+,排放前需处理。向废水中加入CH3COOH和CH3COONa组成的缓冲溶液调节pH,通入H2S发生反应:Zn2++H2S
| 微粒 | H2S | CH3COOH | CH3COO- |
| 浓度/mol·L-1 | 0.20 | 0.10 | 0.20 |
则处理后的废水中c(Zn2+)=
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网