单选题 适中0.65 引用6 组卷500
利用CO2和CH4反应制备合成气(CO、H2)的原理是CH4(g)+CO2(g) 2CO(g)+2H2(g) ΔH>0。温度为T℃时,该反应的平衡常数为K。下列说法正确的是
2CO(g)+2H2(g) ΔH>0。温度为T℃时,该反应的平衡常数为K。下列说法正确的是
| A.K越大,说明反应速率、CO2的平衡转化率越大 |
| B.增大压强,平衡向逆反应方向移动,K减小 |
| C.升高温度,反应速率和平衡常数K都增大 |
| D.加入催化剂,能提高合成气的平衡产率 |
21-22高三下·海南海口·期中
类题推荐
工业上常用如下反应消除氮氧化物的污染:CH4(g)+2NO2(g)⇌N2(g)+CO2(g)+2H2O(g) ΔH<0
(1)书写该反应的平衡常数表达式K=___________ 。
(2)反应达到平衡后,为提高反应速率的同时提高NO2的转化率,可采取的措施有___________。
(3)在体积一定的容器中进行上述反应并达到平衡,保持其它条件不变,通入一定量的CH4,下列说法正确的是___________。
(1)书写该反应的平衡常数表达式K=
(2)反应达到平衡后,为提高反应速率的同时提高NO2的转化率,可采取的措施有___________。
| A.改用高效催化剂 | B.升高温度 |
| C.缩小容器的体积 | D.增加CH4的浓度 |
| A.正反应速率先增大后减小 | B.混合气体的平均密度增大 |
| C.化学平衡常数增大 | D.达到新平衡时 |
甲烷还原可消除NO污染。将NO、O2、CH4混合物按一定体积比通入恒压容器中,发生如下主要反应:①CH4(g)+2NO(g)+O2(g)=N2(g)+CO2(g)+2H2O(g)ΔH1<0
②CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g)ΔH2<0;
③CH4(g)+2O2(g)=CO2(g)+2H2O(g)ΔH3<0
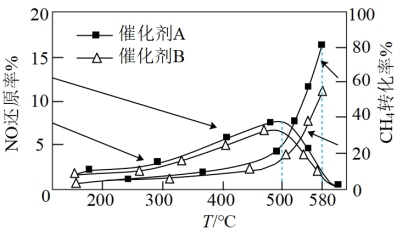
在催化剂A和B的分别作用下,NO的还原率和CH4的转化率分别和温度的关系如图所示。下列有关说法正确的是
②CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g)ΔH2<0;
③CH4(g)+2O2(g)=CO2(g)+2H2O(g)ΔH3<0
在催化剂A和B的分别作用下,NO的还原率和CH4的转化率分别和温度的关系如图所示。下列有关说法正确的是

| A.使用催化剂可增大NO的平衡转化率 |
| B.温度越高,反应②的平衡常数K越大 |
| C.由图可知,消除NO的最佳条件是580℃和催化剂A |
| D.温度高于500℃时,体系中以反应③为主 |
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


