填空题 适中0.65 引用1 组卷62
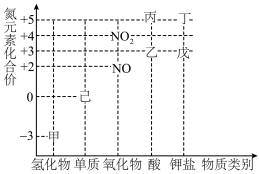
Ⅰ.图象具有直观、线索清晰、引导性强等特点,有利于提高统筹思维和概括能力。图是氮元素的化合价与部分常见含氮物质的关系。

请回答下列问题:
(1)丙的化学式为_______
(2)写出实验室制备甲的化学方程式:_______ ;收集甲物质的常用方法是_______
(3)若己物质的水溶液呈浅绿色,向该溶液中加入稀硫酸,溶液变黄色,同时生成丙,写出该过程中发生反应的离子方程式:_______
(4)丁是一种有颜色的气体,写出丁与水反应生成丙和戊的化学方程式,并用双线桥表示电子转移的情况:_______
(5)常温下,戊的浓溶液可以用干燥的铁罐车运输,原因是_______
Ⅱ.将等物质的量的 、
、 混合于2L的固定体积的密闭容器中,在一定条件下反应合成氨,经5min后达到平衡,其中
混合于2L的固定体积的密闭容器中,在一定条件下反应合成氨,经5min后达到平衡,其中 ;若将混合气体中氨气分离,恰好能与250mL2mol/L的稀硫酸溶液反应生成正盐;
;若将混合气体中氨气分离,恰好能与250mL2mol/L的稀硫酸溶液反应生成正盐;
(6)原容器中 的物质的量是
的物质的量是_______
(7)5min后容器中 的物质的量浓度
的物质的量浓度_______
(8) 的转化率是
的转化率是_______

请回答下列问题:
(1)丙的化学式为
(2)写出实验室制备甲的化学方程式:
(3)若己物质的水溶液呈浅绿色,向该溶液中加入稀硫酸,溶液变黄色,同时生成丙,写出该过程中发生反应的离子方程式:
(4)丁是一种有颜色的气体,写出丁与水反应生成丙和戊的化学方程式,并用双线桥表示电子转移的情况:
(5)常温下,戊的浓溶液可以用干燥的铁罐车运输,原因是
Ⅱ.将等物质的量的
(6)原容器中
(7)5min后容器中
(8)
21-22高一下·河南濮阳·阶段练习
类题推荐
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


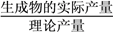 ×100%)。
×100%)。

