解答题-实验探究题 适中0.65 引用2 组卷396
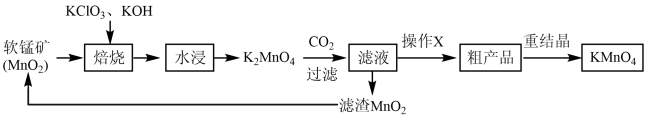
高锰酸钾是常见的强氧化剂,其制备流程如图:
i.制取锰酸钾(K2MnO4)
碱熔:用托盘天平称取5.0gKOH固体、1.5gKClO3固体于坩埚中,混匀、小心加热,不断搅拌,待混合物完全熔融后,加入MnO2粉末3.5g,加热到颜色变为深绿色,用力搅拌到固体干涸、固化,再加热5min,并用铁棒将其尽量捣碎。
浸取:待物料冷却后,置于200mL烧杯中,用50mL蒸馏水浸取,过滤,得到绿色的溶液。
(1)碱熔过程中发生反应的化学方程式为____ ;加热中若不小心将液体溅到皮肤上,应____ 处理;加热时应选择____ (填字母)。
a.瓷坩埚 b.铁坩埚 c.石英坩埚 d.氧化铝坩埚
ii.制取高锰酸钾(KMnO4)
在浸取液中通入CO2气体,至K2MnO4完全反应,用pH试纸测定溶液pH达到10~11时,停止通入CO2。然后把溶液加热,趁热用铺有尼龙布的布氏漏斗进行减压过滤,除去残渣……
已知:常温常压下,饱和碳酸钾溶液的pH为11.6;碳酸氢钾溶液的pH为8.3。
(2)通入CO2发生反应的离子方程式为____ ;判断此反应进行是否完全,也可以用玻璃棒蘸取溶液于滤纸上,若呈现____ 现象,停止通入CO2;过滤时不用滤纸而用尼龙布的原因:____ ;(填“能”或“不能”)____ 用加盐酸的方法代替通入CO2,其理由:____ 。
iii.重结晶提纯
(3)利用重结晶的方法对产品提纯,所得产品质量2.8g,则高锰酸钾的产率为____ 。(精确到0.1%)。

i.制取锰酸钾(K2MnO4)
碱熔:用托盘天平称取5.0gKOH固体、1.5gKClO3固体于坩埚中,混匀、小心加热,不断搅拌,待混合物完全熔融后,加入MnO2粉末3.5g,加热到颜色变为深绿色,用力搅拌到固体干涸、固化,再加热5min,并用铁棒将其尽量捣碎。
浸取:待物料冷却后,置于200mL烧杯中,用50mL蒸馏水浸取,过滤,得到绿色的溶液。
(1)碱熔过程中发生反应的化学方程式为
a.瓷坩埚 b.铁坩埚 c.石英坩埚 d.氧化铝坩埚
ii.制取高锰酸钾(KMnO4)
在浸取液中通入CO2气体,至K2MnO4完全反应,用pH试纸测定溶液pH达到10~11时,停止通入CO2。然后把溶液加热,趁热用铺有尼龙布的布氏漏斗进行减压过滤,除去残渣……
已知:常温常压下,饱和碳酸钾溶液的pH为11.6;碳酸氢钾溶液的pH为8.3。
(2)通入CO2发生反应的离子方程式为
iii.重结晶提纯
(3)利用重结晶的方法对产品提纯,所得产品质量2.8g,则高锰酸钾的产率为
2022·福建·模拟预测
类题推荐
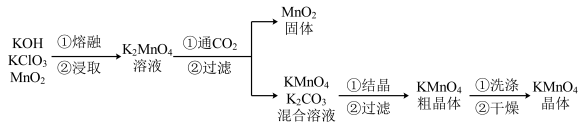
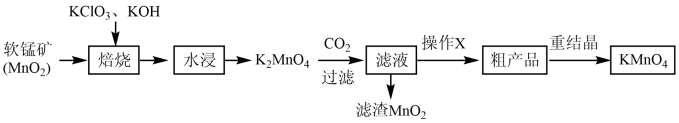
高锰酸钾是常见的强氧化剂,其制备流程如下:
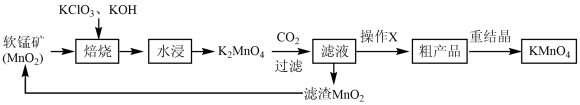
i.制取锰酸钾(K2MnO4)
取适量KOH固体和KClO3固体于坩埚中,混匀、小心加热,不断搅拌,待混合物完全熔融后,加入MnO2粉末8.7g,加热到颜色变为深绿色。
(1)“焙烧”过程中发生反应的化学方程式为_______ ;加热时应选择_______ (填字母)。
a.瓷坩埚 b.铁坩埚 c.石英坩埚 d.氧化铝坩埚
ii.制取高锰酸钾(KMnO4)
在浸取液中通入CO2气体,至K2MnO4完全反应,用pH试纸测定溶液pH达到10~11时,停止通入CO2;然后把溶液加热,趁热过滤,除去滤渣,冷却结晶,过滤、洗涤、干燥。
已知:①常温下,饱和碳酸钾溶液的pH为11.6;饱和碳酸氢钾溶液的pH为8.3。
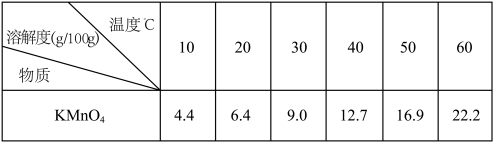
②几种物质在不同温度下的溶解度如下表:
(2)通入CO2发生反应的离子方程式为_______ ;_______ (填“能”或“不能”)用加盐酸的方法代替通入CO2,其理由是_______ 。
(3)趁热过滤的目的是_______ 。
(4)利用重结晶的方法对产品提纯,所得产品质量为10.8g,则高锰酸钾的产率为_______ (精确到0.1%)。

i.制取锰酸钾(K2MnO4)
取适量KOH固体和KClO3固体于坩埚中,混匀、小心加热,不断搅拌,待混合物完全熔融后,加入MnO2粉末8.7g,加热到颜色变为深绿色。
(1)“焙烧”过程中发生反应的化学方程式为
a.瓷坩埚 b.铁坩埚 c.石英坩埚 d.氧化铝坩埚
ii.制取高锰酸钾(KMnO4)
在浸取液中通入CO2气体,至K2MnO4完全反应,用pH试纸测定溶液pH达到10~11时,停止通入CO2;然后把溶液加热,趁热过滤,除去滤渣,冷却结晶,过滤、洗涤、干燥。
已知:①常温下,饱和碳酸钾溶液的pH为11.6;饱和碳酸氢钾溶液的pH为8.3。
②几种物质在不同温度下的溶解度如下表:
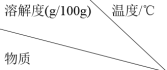 | 10 | 20 | 30 | 40 | 50 | 60 |
| KMnO4 | 4.4 | 6.4 | 9.0 | 12.7 | 16.9 | 22.2 |
(3)趁热过滤的目的是
(4)利用重结晶的方法对产品提纯,所得产品质量为10.8g,则高锰酸钾的产率为
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网