解答题-结构与性质 较难0.4 引用1 组卷102
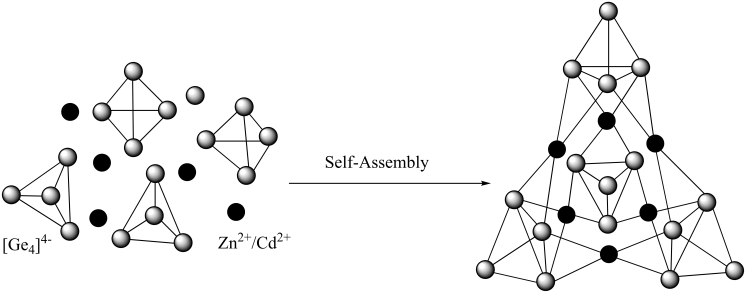
中国科学技术大学俞书宏教授团队和高敏锐教授课题组通过室温过饱和溶液共沉积法,实现了无定形NiFeMo氧化物纳米材料的宏量制备,该方法简便快捷,反应几分钟即可一次性生产多达515克的产物,制备的无定形NiFeMo氧化物在碱性条件下展示出优异的OER催化活性,明显优于结晶型NiFeMo氧化物。根据所学知识回答下列问题:
(1)区别结晶型NiFeMo氧化物和无定形NiFeMo氧化物最可靠的科学方法为_______ ,结晶型NiFeMo氧化物能自发呈现多面体外形,这种性质称为晶体的_______ 。
(2)配合物Ni(CO)4常温下为液态,易溶于CCl4,苯等有机溶剂,是获得高纯度纳米镍的原料,Ni(CO)4的配位原子是_______ 。
(3)下列状态的铁中,电离最外层的一个电子所需能量最大的是_______(填编号)。
(4)FeCl3中的化学键具有明显的共价性,蒸气状态下以双聚分子存在的FeCl3的结构式为_______ ,其中Fe的配位数为_______ 。
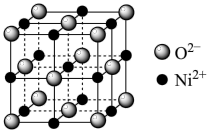
(5)立方NiO(氧化镍)晶体的结构如图所示,其晶胞边长为a pm,列式表示NiO晶体的密度为_______ g/cm3(不必计算出结果,阿伏加德罗常数的值为NA)。
(1)区别结晶型NiFeMo氧化物和无定形NiFeMo氧化物最可靠的科学方法为
(2)配合物Ni(CO)4常温下为液态,易溶于CCl4,苯等有机溶剂,是获得高纯度纳米镍的原料,Ni(CO)4的配位原子是
(3)下列状态的铁中,电离最外层的一个电子所需能量最大的是_______(填编号)。
A. | B.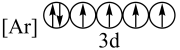 |
C.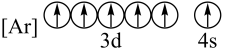 | D.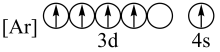 |
(5)立方NiO(氧化镍)晶体的结构如图所示,其晶胞边长为a pm,列式表示NiO晶体的密度为

21-22高二下·广东惠州·期中
类题推荐
根据要求回答以下问题
(1)中国科学技术大学俞书宏教授团队和高敏锐教授课题组通过室温过饱和溶液共沉积法,实现了无定形 NiFeMo 氧化物纳米材料的宏量制备,该方法简便快捷,反应几分钟即可一次性生产多达515克的产物,制备的无定形NiFeMo氧化物在碱性条件下展示出优异的OER催化活性,明显优于结晶型NiFeMo氧化物。区别结晶型NiFeMo氧化物和无定形NiFeMo氧化物最可靠的科学方法为_________ ,结晶型NiFeMo氧化物能自发呈现多面体外形,这种性质称为晶体的_________ 。
(2)①冰的密度小于液态水与冰晶体的结构有关,1mol冰形成_______ mol氢键。
②比较下列镓的卤化物的熔点和沸点,分析其变化规律及其原因:________
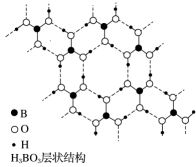
(3)①如图为硼酸(H3BO3)晶体的片层结构(如图),其中硼原子的杂化方式为________ 。该晶体的片层结构中存在的作用力有________ 。__________ 。(注明配位键的箭头)
③一种由Mg2+、N3—、 F—组成的化合物的立方晶胞如图所示:
(1)中国科学技术大学俞书宏教授团队和高敏锐教授课题组通过室温过饱和溶液共沉积法,实现了无定形 NiFeMo 氧化物纳米材料的宏量制备,该方法简便快捷,反应几分钟即可一次性生产多达515克的产物,制备的无定形NiFeMo氧化物在碱性条件下展示出优异的OER催化活性,明显优于结晶型NiFeMo氧化物。区别结晶型NiFeMo氧化物和无定形NiFeMo氧化物最可靠的科学方法为
(2)①冰的密度小于液态水与冰晶体的结构有关,1mol冰形成
②比较下列镓的卤化物的熔点和沸点,分析其变化规律及其原因:
| 镓的卤化物 | GaCl3 | GaBr3 | GaI3 |
| 熔点/℃ | 77.75 | 122.3 | 211.5 |
| 沸点/℃ | 201.2 | 279 | 346 |
③一种由Mg2+、N3—、 F—组成的化合物的立方晶胞如图所示:
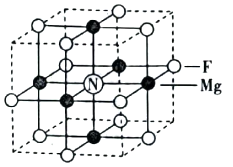
该化合物的化学式为
过渡区金属元素原子或离子易形成配合物,广泛用作催化剂。例如Ni、Fe、Mo三种元素可以合成一种新型高效催化剂,在碱性条件下可展示出优异的OER(电催化析氧)催化活性。回答下列问题:
(1)电催化析氧过程中常用通NH3的方法来调节溶液酸碱性:
I.若溶液中有次氯酸盐,NH3有可能被氧化成NH2-NH2,NH2-NH2中N原子的杂化方式是_______ 。
II.若溶液中含有铜离子,可形成配离子[Cu(NH3)4]2+。
①[Cu(NH3)4]2+具有对称的空间构型,若其中两个NH3被两个Cl-取代,能得到两种不同结构的产物,则[Cu(NH3)4]2+的空间构型为_______ 。
②Cu2+还可与其他微粒形成配离子,如与乙二胺形成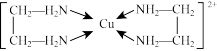 ,此配离子内部不含有的化学键类型是
,此配离子内部不含有的化学键类型是_______ (填标号)。
A.离子键 B.非极性键 C.配位键 D.氢键
③上述乙二胺和三甲胺[N(CH3)3]均属于胺。但乙二胺比三甲胺的沸点高很多,原因是_______ 。
(2)下列状态的铁中,失去最外层的一个电子所需能量最大的是_______(填标号)。
(3)配合物Ni(CO)4常温下为液态,易溶于CCl4、苯等有机溶剂,是获得高纯度纳米镍的原料,推测Ni(CO)4属于_______ (填“极性”或“非极性”)分子。
(4)立方NiO(氧化镍)晶体的晶胞结构如图所示,晶胞边长为apm,则NiO晶体的密度为_______ g/cm3(NA表示阿伏加德罗常数)。

(1)电催化析氧过程中常用通NH3的方法来调节溶液酸碱性:
I.若溶液中有次氯酸盐,NH3有可能被氧化成NH2-NH2,NH2-NH2中N原子的杂化方式是
II.若溶液中含有铜离子,可形成配离子[Cu(NH3)4]2+。
①[Cu(NH3)4]2+具有对称的空间构型,若其中两个NH3被两个Cl-取代,能得到两种不同结构的产物,则[Cu(NH3)4]2+的空间构型为
②Cu2+还可与其他微粒形成配离子,如与乙二胺形成
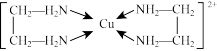 ,此配离子内部不含有的化学键类型是
,此配离子内部不含有的化学键类型是A.离子键 B.非极性键 C.配位键 D.氢键
③上述乙二胺和三甲胺[N(CH3)3]均属于胺。但乙二胺比三甲胺的沸点高很多,原因是
(2)下列状态的铁中,失去最外层的一个电子所需能量最大的是_______(填标号)。
A. | B.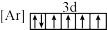 |
C.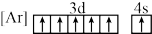 | D.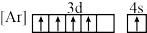 |
(4)立方NiO(氧化镍)晶体的晶胞结构如图所示,晶胞边长为apm,则NiO晶体的密度为

组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网