解答题-实验探究题 较难0.4 引用3 组卷949
某小组用MnO2与浓盐酸混合共热制备氯气。
(1)反应的离子方程式是_______ 。
(2)为净化与收集Cl2,选用下图所示的部分装置进行实验,装置的接口连接顺序为_______ 。
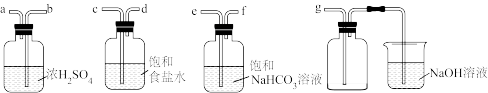
(3)当Cl2不再生成时,反应容器中仍存在MnO2和盐酸,该小组进行以下实验探究。
①实验任务 探究反应后的容器中仍存在MnO2和盐酸,却不再产生Cl2的原因。
②查阅资料 物质氧化性和还原性变化的一般规律是:还原反应中,增大反应物浓度或降低生成物浓度,氧化剂的氧化性增强;氧化反应中,增大反应物浓度或降低生成物浓度,还原剂的还原性增强。
③提出猜想 猜想a:在此反应中,随H+浓度降低,氧化剂_______ (填氧化剂化学式)氧化性减弱。
猜想b:在此反应中,_______ 减弱。
猜想c:在此反应中,随Mn2+浓度升高,氧化剂氧化性减弱。
④设计实验、验证猜想 向反应后的固液混合物中加入试剂,观察并记录有无氯气生成(Na+对各物质的氧化性与还原性均无影响)。请在答题线上完成表中内容。
⑤数据分析,得出结论 猜想a、猜想b和猜想c均正确。
⑥迁移应用 25℃时, 。一般情况下,在金属活动性顺序里,位于氢前面的金属能置换出酸中的氢,资料显示Ag也可以与HI发生置换反应生成H2,依据②中信息,可能的原因是:
。一般情况下,在金属活动性顺序里,位于氢前面的金属能置换出酸中的氢,资料显示Ag也可以与HI发生置换反应生成H2,依据②中信息,可能的原因是:_______ 。
(1)反应的离子方程式是
(2)为净化与收集Cl2,选用下图所示的部分装置进行实验,装置的接口连接顺序为
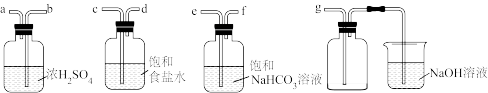
(3)当Cl2不再生成时,反应容器中仍存在MnO2和盐酸,该小组进行以下实验探究。
①实验任务 探究反应后的容器中仍存在MnO2和盐酸,却不再产生Cl2的原因。
②查阅资料 物质氧化性和还原性变化的一般规律是:还原反应中,增大反应物浓度或降低生成物浓度,氧化剂的氧化性增强;氧化反应中,增大反应物浓度或降低生成物浓度,还原剂的还原性增强。
③提出猜想 猜想a:在此反应中,随H+浓度降低,氧化剂
猜想b:在此反应中,
猜想c:在此反应中,随Mn2+浓度升高,氧化剂氧化性减弱。
④设计实验、验证猜想 向反应后的固液混合物中加入试剂,观察并记录有无氯气生成(Na+对各物质的氧化性与还原性均无影响)。请在答题线上完成表中内容。
| 实验序号 | 操作 | 有无氯气生成 |
| 1 | 加入较浓硫酸,使 | 有氯气 |
| 2 | 加入NaCl固体,使 | 有氯气 |
| 3 | 无氯气 |
⑥迁移应用 25℃时,
2022·广东茂名·二模
类题推荐
含氯物质在生产生活中有重要作用。
I.实验室制取氯气的装置如图所示。
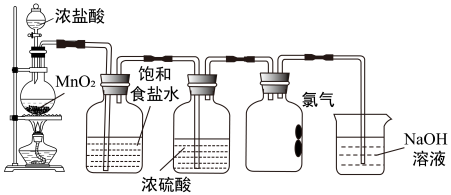
(1)收集氯气的集气瓶中,导管没有画完整,请在答题卡图中补充完整___________ 。
(2)NaOH溶液的作用是(用离子方程式表示)___________
(3)当氯气不再逸出时,圆底烧瓶中的固液混合物中仍存在盐酸和二氧化锰,某合作学习小组分析成因时提出如下猜想:
猜想a;随H+浓度降低,MnO2的氧化性减弱。
猪想b:随Cl-浓度降低,Cl-的还原性___________ (填“增强”、“不变”或“减弱”)。
猜想c:随Mn2+浓度升高,MnO2的氧化性减弱。
①查阅资料:K+、 对体系中各物质的氧化性与还原性均无影响。
对体系中各物质的氧化性与还原性均无影响。
②设计实验验证:将固液混合物均分为三组,保持条件相同,分别向三组固液混合物中加入试剂。
通过三组实验,a、b、c三个猜想都得到了证实,则X为_______ (填化学式),Y为_______ (填化学式)。
II.已知FeCl3固体易升华,其蒸气为黄色。某小组通过下面装置探究MnO2与FeCl3能否反应产生Cl2。
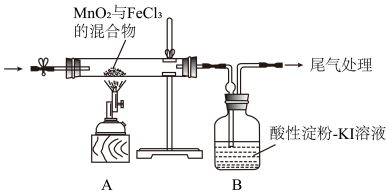
实验操作和现象:
(4)实验前,需要进行的操作为___________ 。
(5)该实验装置从安全角度分析,存在的问题是___________ 。
(6)装置经改进后,继续实验,确认产物有Cl2和MnCl2,则A中发生反应的化学方程式为___________ 。
I.实验室制取氯气的装置如图所示。

(1)收集氯气的集气瓶中,导管没有画完整,请在答题卡图中补充完整
(2)NaOH溶液的作用是(用离子方程式表示)
(3)当氯气不再逸出时,圆底烧瓶中的固液混合物中仍存在盐酸和二氧化锰,某合作学习小组分析成因时提出如下猜想:
猜想a;随H+浓度降低,MnO2的氧化性减弱。
猪想b:随Cl-浓度降低,Cl-的还原性
猜想c:随Mn2+浓度升高,MnO2的氧化性减弱。
①查阅资料:K+、
②设计实验验证:将固液混合物均分为三组,保持条件相同,分别向三组固液混合物中加入试剂。
| 组别 | 试剂 | 产物 |
| 1 | 较浓硫酸 | 有Cl2生成 |
| 2 | X | 有Cl2生成 |
| 3 | X和Y | 无Cl2生成 |
II.已知FeCl3固体易升华,其蒸气为黄色。某小组通过下面装置探究MnO2与FeCl3能否反应产生Cl2。

实验操作和现象:
| 实验操作 | 现象 |
| 点燃酒精喷灯,加热 | 加热一段时间后,装置A中产生黄色气体,装置B中溶液变蓝 |
(5)该实验装置从安全角度分析,存在的问题是
(6)装置经改进后,继续实验,确认产物有Cl2和MnCl2,则A中发生反应的化学方程式为
某小组探究卤素参与的氧化还原反应,从电极反应角度分析物质氧化性和还原性的变化规律。
(1)浓盐酸与MnO2混合加热生成氯气。氯气不再逸出时,固液混合物A中仍存在盐酸和MnO2。
①反应的离子方程式是_______ 。
②电极反应式:
ⅰ.氧化反应:2Cl--2e-=Cl2↑
ⅱ.还原反应:_______ 。
③根据电极反应式,分析A中仍存在盐酸和MnO2的原因。
ⅰ.随c(Cl-)降低,Cl-还原性减弱或Cl2的氧化性增强。
ⅱ.随c(H+)降低或c(Mn2+)浓度升高,_______ 。
④补充实验证实了③中的分析(下面表格)。
a是_______ ,b是_______ 。
(2)利用c(H+)浓度对MnO2氧化性的影响,探究卤素离子的还原性。相同浓度的KCl、KBr和KI溶液,能与MnO2反应所需的最低c(H+)由大到小的顺序是_______ 。
(3)根据(1)中结论推测:酸性条件下,加入某种化合物可以提高溴的氧化性,将Mn2+氧化为MnO2。经实验证实了推测,该化合物是_______ 。
(4)综合上述,可以得到物质氧化性和还原性变化的一般规律:氧化剂(还原剂)的浓度越大,其氧化性(还原性)越强;还原产物(氧化产物)的浓度越大,氧化剂(还原剂)的氧化性(还原性)越小。据此,小组分别利用电解池(图1)和原电池(图2)装置,成功实现了铜与稀硫酸制氢气。
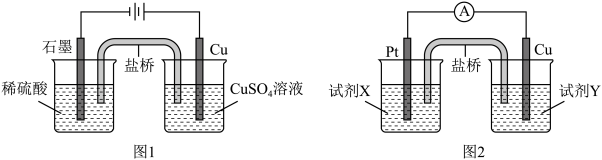
结合上述的探究结论,图2中试剂X是_______ ,试剂Y是_______ 。(限选试剂:稀硫酸、Na2SO4溶液、NaOH溶液、NaNO3溶液、CuSO4溶液,浓度均为1.0 mol·L-1)
(1)浓盐酸与MnO2混合加热生成氯气。氯气不再逸出时,固液混合物A中仍存在盐酸和MnO2。
①反应的离子方程式是
②电极反应式:
ⅰ.氧化反应:2Cl--2e-=Cl2↑
ⅱ.还原反应:
③根据电极反应式,分析A中仍存在盐酸和MnO2的原因。
ⅰ.随c(Cl-)降低,Cl-还原性减弱或Cl2的氧化性增强。
ⅱ.随c(H+)降低或c(Mn2+)浓度升高,
④补充实验证实了③中的分析(下面表格)。
| 实验操作 | 试剂 | 产物 | |
| Ⅰ | 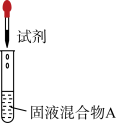 | 较浓H2SO4 | 有氯气 |
| Ⅱ | a | 有氯气 | |
| Ⅲ | a+b | 无氯气 |
(2)利用c(H+)浓度对MnO2氧化性的影响,探究卤素离子的还原性。相同浓度的KCl、KBr和KI溶液,能与MnO2反应所需的最低c(H+)由大到小的顺序是
(3)根据(1)中结论推测:酸性条件下,加入某种化合物可以提高溴的氧化性,将Mn2+氧化为MnO2。经实验证实了推测,该化合物是
(4)综合上述,可以得到物质氧化性和还原性变化的一般规律:氧化剂(还原剂)的浓度越大,其氧化性(还原性)越强;还原产物(氧化产物)的浓度越大,氧化剂(还原剂)的氧化性(还原性)越小。据此,小组分别利用电解池(图1)和原电池(图2)装置,成功实现了铜与稀硫酸制氢气。

结合上述的探究结论,图2中试剂X是
氯气是一种重要的化工原料,在生产生活中有着重要的应用。
(1)某研究小组探究氯气和氯水的漂白性,用浓盐酸与MnO2反应制备氯气,其化学反应方程式为_______ 。生成的氯气通入如图装置,所需装置的接口连接顺序为_______ (填字母序号)。

证明氯水具有漂白性是由于Cl2与H2O反应生成了具有漂白性的物质的实验现象是_______ 。
(2)在用浓盐酸与MnO2混合加热制氯气过程中,发现氯气不再逸出时,固液混合物A中仍存在盐酸和MnO2。关于MnO2剩余的原因,该小组提出如下猜想:
猜想ⅰ:随着反应进行,c(H+)降低,Cl-的还原性减弱,不能还原MnO2。
猜想ⅱ:随着反应进行,c(H+)降低,MnO2的氧化性减弱,不能氧化Cl-。
猜想ⅱi:随着反应进行,c(Cl-)降低,Cl-的还原性减弱,不能还原MnO2。
猜想iv:随着反应进行,c(Mn2+)升高,MnO2的氧化性减弱,不能氧化Cl-。
该小组设计原电池装置验证上述猜想,请补充横线部分的内容。(恒温装置未画出)
(1)某研究小组探究氯气和氯水的漂白性,用浓盐酸与MnO2反应制备氯气,其化学反应方程式为

证明氯水具有漂白性是由于Cl2与H2O反应生成了具有漂白性的物质的实验现象是
(2)在用浓盐酸与MnO2混合加热制氯气过程中,发现氯气不再逸出时,固液混合物A中仍存在盐酸和MnO2。关于MnO2剩余的原因,该小组提出如下猜想:
猜想ⅰ:随着反应进行,c(H+)降低,Cl-的还原性减弱,不能还原MnO2。
猜想ⅱ:随着反应进行,c(H+)降低,MnO2的氧化性减弱,不能氧化Cl-。
猜想ⅱi:随着反应进行,c(Cl-)降低,Cl-的还原性减弱,不能还原MnO2。
猜想iv:随着反应进行,c(Mn2+)升高,MnO2的氧化性减弱,不能氧化Cl-。
该小组设计原电池装置验证上述猜想,请补充横线部分的内容。(恒温装置未画出)
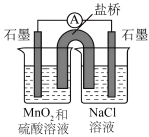 | ||||
| 实验编号 | 实验步骤 | 实验现象 | 实验结论 | 实验反思与评价 |
| i | 向右侧烧杯中滴入几滴浓盐酸 | 猜想i成立 | 该操作不能验证猜想i,理由① | |
| ii | ② | ③ | 猜想ii成立 | 正极的电极反应方程式④ |
| …… | ||||
| iv | 在验证了猜想ii和iii均成立以后,向左侧烧杯中加入⑤ | 电流表几乎无示数 | 猜想iv成立 | |
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


