解答题-原理综合题 适中0.65 引用1 组卷151
恒温下,将amolN2与bmolH2的混合气体通入一个2L的密闭容器中合成氨,当反应进行到5s时,有0.1molNH3生成,并且放出4.62kJ的热量。
(1)0~5s用H2表示该反应的平均反应速率v(H2)=_____ mol·L-1·s-1。
(2)写出合成氨反应的热化学方程式:____ 。
(3)若反应进行到某时刻t时,nt(N2)=3mol,nt(H2)=8mol,nt(NH3)=6mol,
①a=____ ,b=____ 。
②反应达平衡时,混合气体的体积为291.2L(标准状况下),则平衡时NH3的物质的量为____ mol。
③有人设想以N2和H2为反应物,以溶有NH4Cl的稀盐酸为电解质溶液,可制造出既能提供电能,又能固氨的新型燃料电池,装置如图所示。
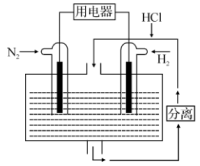
写出该电池负极的电极方程式:____ 。
(1)0~5s用H2表示该反应的平均反应速率v(H2)=
(2)写出合成氨反应的热化学方程式:
(3)若反应进行到某时刻t时,nt(N2)=3mol,nt(H2)=8mol,nt(NH3)=6mol,
①a=
②反应达平衡时,混合气体的体积为291.2L(标准状况下),则平衡时NH3的物质的量为
③有人设想以N2和H2为反应物,以溶有NH4Cl的稀盐酸为电解质溶液,可制造出既能提供电能,又能固氨的新型燃料电池,装置如图所示。

写出该电池负极的电极方程式:
21-22高一下·湖北武汉·期中
类题推荐
为了合理利用化学能确保安全生产,化工设计需要充分考虑化学反应的焓变,并采取相应措施。化学反应的焓变通常用实验进行测定,也可进行理论推算。
(1)实验测得:5g液态甲醇(CH3OH)在氧气中完全燃烧,生成二氧化碳气体和液态水时释放出113.5kJ的热量。试写出甲醇燃烧热的热化学方程式:___ 。
(2)合成甲醇的主要反应是2H2(g)+CO(g) CH3OH(g)ΔH=-90.8kJ·mol-1,t℃时,向2L的密闭容器中投入2molH2和mmolCO,反应10min后测得各组分的浓度如下:
CH3OH(g)ΔH=-90.8kJ·mol-1,t℃时,向2L的密闭容器中投入2molH2和mmolCO,反应10min后测得各组分的浓度如下:
则该时间段内反应速率v(H2)=___ ,m=___ mol。
(3)恒温下,将amolN2与bmolH2的混合气体通入一个固定容积的密闭容器中,发生如下反应:N2(g)+3H2(g) 2NH3(g)
2NH3(g)
①若反应进行到某时刻t时,nt(N2)=13mol,nt(NH3)=6mol,则a=___ mol。
②反应达平衡时,混合气体的体积为716.8L(标况下),其中NH3的含量(体积分数)为25%。则平衡时NH3的物质的量为___ ,原混合气体中a:b=___ (写出最简整数比,下同)。
③达到平衡时,N2和H2的转化率之比α(N2):α(H2)=___ 。
(1)实验测得:5g液态甲醇(CH3OH)在氧气中完全燃烧,生成二氧化碳气体和液态水时释放出113.5kJ的热量。试写出甲醇燃烧热的热化学方程式:
(2)合成甲醇的主要反应是2H2(g)+CO(g)
| 物质 | H2 | CO | CH3OH |
| 浓度(mol·L-1) | 0.2 | 0.1 | 0.4 |
(3)恒温下,将amolN2与bmolH2的混合气体通入一个固定容积的密闭容器中,发生如下反应:N2(g)+3H2(g)
①若反应进行到某时刻t时,nt(N2)=13mol,nt(NH3)=6mol,则a=
②反应达平衡时,混合气体的体积为716.8L(标况下),其中NH3的含量(体积分数)为25%。则平衡时NH3的物质的量为
③达到平衡时,N2和H2的转化率之比α(N2):α(H2)=
I.恒温下,将amolN2与bmolH2的混合气体通入一个恒容密闭容器中,发生如下反应:N2(g)+3H2(g) 2NH3(g)
2NH3(g)
(1)反应进行到某时刻t时,n(N2)=13mol,n(NH3)=6mol,则a=___________ 。
(2)反应达平衡时,混合气体的体积为716.8L(标准状况),其中NH3的含量(体积分数)为25%,平衡时NH3的物质的量为___________ mol。
(3)原混合气体与平衡时混合气体的总物质的量之比,n(始)∶n(平) =________ (最简整数比)
(4)达到平衡时,N2和H2的转化率之比α(N2): α(H2)=___________ (写出最简整数比)。
II.在一定体积的密闭容器中,进行如下化学反应:CO2(g)+H2(g) CO(g)+H2O(g),其化学平衡常数K和温度t的关系如表格。
CO(g)+H2O(g),其化学平衡常数K和温度t的关系如表格。
(5)该反应的化学平衡常数表达式为K=___________ 。
(6)该反应正反应为___________ 反应(选填吸热、放热)。
(1)反应进行到某时刻t时,n(N2)=13mol,n(NH3)=6mol,则a=
(2)反应达平衡时,混合气体的体积为716.8L(标准状况),其中NH3的含量(体积分数)为25%,平衡时NH3的物质的量为
(3)原混合气体与平衡时混合气体的总物质的量之比,n(始)∶n(平) =
(4)达到平衡时,N2和H2的转化率之比α(N2): α(H2)=
II.在一定体积的密闭容器中,进行如下化学反应:CO2(g)+H2(g)
| t/℃ | 700 | 800 | 830 | 1000 | 1200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
(6)该反应正反应为
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


