填空题 较易0.85 引用1 组卷261
海洋是巨大的化学资源宝库。从海水中可以制取氯、溴、镁等多种化工产品。
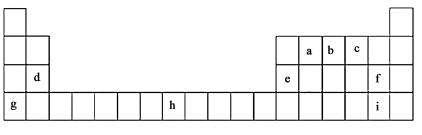
(1)Mg在元素周期表中的位置是第_______ 周期、第IIA族。
(2)Cl的最高价氧化物对应的水化物为HClO4,其中氯元素的化合价是_______ 。
(3)金属性Na强于Mg,用原子结构解释原因:Na和Mg位于同一周期,原子核外电子层数相同,_______ ,原子半径Na大于Mg,失电子能力Na强于Mg。
(4)在元素周期表中,溴(Br)位于第4周期,与Cl同主族。下列实验或事实能说明得电子能力Cl强于Br的是_______ (填字母)。
a.将Cl2通入KBr溶液中可制得Br2
b.常温常压下,Cl2为气态,Br2为液态
c.HBr约500℃开始分解,HCl约1000℃开始缓慢分解
(1)Mg在元素周期表中的位置是第
(2)Cl的最高价氧化物对应的水化物为HClO4,其中氯元素的化合价是
(3)金属性Na强于Mg,用原子结构解释原因:Na和Mg位于同一周期,原子核外电子层数相同,
(4)在元素周期表中,溴(Br)位于第4周期,与Cl同主族。下列实验或事实能说明得电子能力Cl强于Br的是
a.将Cl2通入KBr溶液中可制得Br2
b.常温常压下,Cl2为气态,Br2为液态
c.HBr约500℃开始分解,HCl约1000℃开始缓慢分解
2022高三下·北京·学业考试
类题推荐
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网