解答题-工业流程题 适中0.65 引用1 组卷95
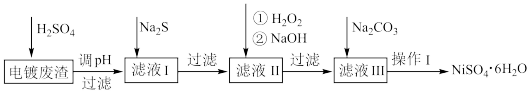
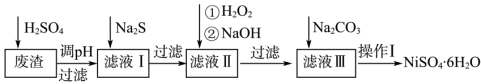
镍(Ni)及其化合物广泛应用于生产电池、电镀和催化剂等领域。NiSO4·6H2O晶体是一种绿色易溶于水的晶体,广泛用于化学镀镍、生产电池等,可由电镀废渣(除含镍外,还含有Cu2+、Zn2+、Fe2+等)为原料获得。操作步骤如图:
已知:Ksp(FeS)=6.3×10-18,Ksp(CuS)=1.3×10-36,Ksp(ZnS)=1.3×10-24,Ksp(NiS)=1.1×10-21,Fe(OH)3的Ksp=1.0×10-39。
(1)加入Na2S的目的是除去Zn2+,Cu2+,反应的离子方程式是____ 、____ 。
(2)滤液II中加入H2O2的目的是____ 。
(3)向滤液II中加入NaOH调节pH在一范围内生成氢化铁沉淀。若要使溶液中c(Fe3+)≤1.0×10-6mol·L-1,则应该控制溶液pH范围不小于____ 。
(4)加入Na2CO3的目的是沉淀Ni2+。Na2CO3溶液中离子浓度由大到小的顺序是____ 。
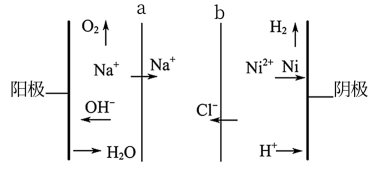
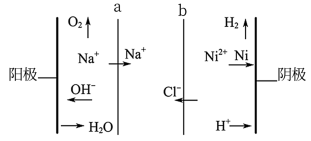
(5)双膜三室电解法处理含镍废水并回收金属镍的原理如图所示。判断a是____ (填“阳膜”或“阴膜”),阴极反应是____ 。

已知:Ksp(FeS)=6.3×10-18,Ksp(CuS)=1.3×10-36,Ksp(ZnS)=1.3×10-24,Ksp(NiS)=1.1×10-21,Fe(OH)3的Ksp=1.0×10-39。
(1)加入Na2S的目的是除去Zn2+,Cu2+,反应的离子方程式是
(2)滤液II中加入H2O2的目的是
(3)向滤液II中加入NaOH调节pH在一范围内生成氢化铁沉淀。若要使溶液中c(Fe3+)≤1.0×10-6mol·L-1,则应该控制溶液pH范围不小于
(4)加入Na2CO3的目的是沉淀Ni2+。Na2CO3溶液中离子浓度由大到小的顺序是
(5)双膜三室电解法处理含镍废水并回收金属镍的原理如图所示。判断a是

21-22高二下·广西河池·阶段练习
类题推荐
NiSO4•6H2O是一种绿色易溶于水的晶体,可由电镀废渣(除镍外,还含有铜、锌、铁等元素的化合物杂质)为原料获得。操作步骤如图:

已知:各离子开始沉淀及完全沉淀时的pH如表所示:
(1)向滤液Ⅰ中加入FeS固体是为了生成更难溶于水的硫化物沉淀而除去Cu2+、Zn2+等杂质,则除去Cu2+的离子方程式为___________ ,当c(Cu2+)≤1.0×10-5mol•L-1时,可认为Cu2+已沉淀完全,此时溶液中S2-的浓度不小于___________ 。(已知:Ksp(CuS)=6.3×10-36)
(2)根据对滤液Ⅱ的操作作答:
①向滤液Ⅱ中加H2O2的目的是___________ 。
②调节滤液Ⅱ的pH,pH应控制在范围___________ 。
③检验滤液Ⅲ中杂质金属离子是否除尽的试剂是___________ 。
(3)滤液Ⅲ溶质的主要成分是NiSO4,加Na2CO3过滤后得到NiCO3固体,再加适量稀硫酸溶解又生成NiSO4,这两步操作的目的是___________ 。

已知:各离子开始沉淀及完全沉淀时的pH如表所示:
| 离子 | 开始沉淀时的pH | 完全沉淀时的pH |
| Fe2+ | 6.3 | 9.7 |
| Fe3+ | 2.2 | 3.2 |
| Ni2+ | 6.4 | 8.4 |
(2)根据对滤液Ⅱ的操作作答:
①向滤液Ⅱ中加H2O2的目的是
②调节滤液Ⅱ的pH,pH应控制在范围
③检验滤液Ⅲ中杂质金属离子是否除尽的试剂是
(3)滤液Ⅲ溶质的主要成分是NiSO4,加Na2CO3过滤后得到NiCO3固体,再加适量稀硫酸溶解又生成NiSO4,这两步操作的目的是
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网