解答题-结构与性质 适中0.65 引用1 组卷80
I.新型储氢材料是开发利用氢能的重要研究方向,Ti(BH4)3是一种储氢材料,可由LiBH4和TiCl4反应制得。
(1)基态Cl原子有_______ 种运动状态的电子,属于_______ 区(填“s”或“p”或“d”或“f”);
(2)LiBH4由Li+和 构成,
构成, 的立体结构是
的立体结构是_______ ,与 互为等电子体的分子为
互为等电子体的分子为_______ ,Li、Be、B元素的第一电离能由大到小排列顺序为_______ ;
(3)某储氢材料是短周期金属元素M的氢化物。M的部分电离能如下表所示:
M是_______ (填元素符号)。
II.叠氮化合物是一类重要的化合物,其中氢叠氮酸(HN3)是一种弱酸,其分子结构可表示为H—N=N≡N,肼(N2H4)被亚硝酸氧化时便可得到氢叠氮酸(HN3),发生的反应为:N2H4+HNO2=2H2O+HN3。HN3的酸性和醋酸相近,可微弱电离出H+和 。试回答下列问题:
。试回答下列问题:
(4)下列有关说法正确的是_______(填序号);
(5)叠氮酸根能与许多金属离子等形成配合物,如[Co(N3)(NH3)5]SO4,在该配合物中钴显_______ 价;根据价层电子对互斥理论判断 的空间构型为
的空间构型为_______ ;
(6)与 互为等电子体的分子有
互为等电子体的分子有_______ (写两种即可)。
(1)基态Cl原子有
(2)LiBH4由Li+和
(3)某储氢材料是短周期金属元素M的氢化物。M的部分电离能如下表所示:
| I1/kJ·mol-1 | I2/kJ·mol-1 | I3/kJ·mol-1 | I4/kJ·mol-1 | I5/kJ·mol-1 |
| 738 | 1451 | 7733 | 10540 | 13630 |
II.叠氮化合物是一类重要的化合物,其中氢叠氮酸(HN3)是一种弱酸,其分子结构可表示为H—N=N≡N,肼(N2H4)被亚硝酸氧化时便可得到氢叠氮酸(HN3),发生的反应为:N2H4+HNO2=2H2O+HN3。HN3的酸性和醋酸相近,可微弱电离出H+和
(4)下列有关说法正确的是_______(填序号);
| A.HN3中含有5个σ键 |
| B.HN3中的三个氮原子均采用sp2杂化 |
| C.HN3、HNO2、H2O、N2H4都是极性分子 |
| D.N2H4沸点高达113.5℃,说明肼分子间可形成氢键 |
(6)与
21-22高二下·甘肃兰州·阶段练习
类题推荐
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网

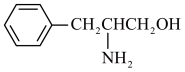 。该有机物分子是
。该有机物分子是

