解答题-结构与性质 较难0.4 引用1 组卷144
硒( )被科学家称为人体微量元素中的“抗癌之王”,硒(
)被科学家称为人体微量元素中的“抗癌之王”,硒( )与氧(O)、硫(S)位于元素周期表中第ⅥA族。回答下列问题:
)与氧(O)、硫(S)位于元素周期表中第ⅥA族。回答下列问题:
(1)基态氧原子的价电子排布图为___________ ,第二周期元素的第一电离能比氧元素大的主族元素有___________ (填元素符号)。
(2)单质硫最稳定的结构是由八个原子组成的环—— ,其中S原子的杂化方式为
,其中S原子的杂化方式为___________ 。
(3)酸性:
___________  (填“强于”或“弱于”),
(填“强于”或“弱于”), 的空间构型为
的空间构型为___________ ,写出一种与 互为等电子体的分子的化学式:
互为等电子体的分子的化学式:___________ 。
(4) 、
、 均为离子化合物,其熔点由高到低的顺序为
均为离子化合物,其熔点由高到低的顺序为___________ (用化学式表示),原因为___________ 。
(5) 的立方晶胞结构如图所示,晶胞参数为
的立方晶胞结构如图所示,晶胞参数为 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 ,则
,则 晶体的密度为
晶体的密度为___________  (用含a、
(用含a、 的代数式表示)。
的代数式表示)。
(1)基态氧原子的价电子排布图为
(2)单质硫最稳定的结构是由八个原子组成的环——
(3)酸性:
(4)
(5)

21-22高三上·重庆巴南·阶段练习
类题推荐
我国科学家研究发现 (
( 家族成员之一,A为一价金属,M为三价金属,X为氧族元素)在室温下具有超离子行为。回答下列问题:
家族成员之一,A为一价金属,M为三价金属,X为氧族元素)在室温下具有超离子行为。回答下列问题:
(1)基态铬原子的电子排布式为_________ ;基态硫原子核外电子中含有_________ 个未成对电子。
(2)同周期元素Si、P、S的电负性由大到小的顺序为________________ (用元素符号表示),O、S为同主族元素, 的键角比
的键角比 大的原因是
大的原因是________________ 。
(3)硫元素能形成多种微粒如 、
、 、
、 、
、 、
、 等,
等, 的中心原子的杂化类型为
的中心原子的杂化类型为_______________ , 的空间构型为
的空间构型为________ 。
(4) 中
中 元素化合价为+6价,常温下呈蓝色,则其结构式可能为
元素化合价为+6价,常温下呈蓝色,则其结构式可能为________ (填标号)。
(5)某含铬化合物立方晶胞如图所示。该晶体的化学式为_____________ ;与Cr最近的氧原子的个数为________ ; 和
和 的最近距离为a nm,设
的最近距离为a nm,设 为阿伏加德罗常数的值,则该晶体密度
为阿伏加德罗常数的值,则该晶体密度______________  (填含a、
(填含a、 的表达式)。
的表达式)。
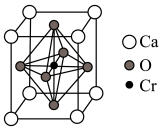
(1)基态铬原子的电子排布式为
(2)同周期元素Si、P、S的电负性由大到小的顺序为
(3)硫元素能形成多种微粒如
(4)
|
|
|
A | B | C |

我国科学家研究发现AgCrS2 (AMX2家族成员之一,A为一价金属,M为三价金属,X为氧族元素)在室温下具有超离子行为。回答下列问题:
(1)基态铬原子的价电子排布式为___________ ;基态硫原子核外电子的空间运动状态有___________ 种。
(2)同周期元素Si、P、S的第一电离能由大到小的顺序为___________ (用元素符号表示),O、S为同主族元素, H2O的沸点比H2S高的原因是___________ 。
(3)硫元素能形成多种微粒如H2S、SO2、SO3、 、
、 等。SO2的立体构型为
等。SO2的立体构型为___________ , 的中心原子的杂化类型是
的中心原子的杂化类型是___________ 。
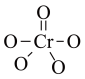
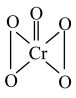
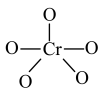
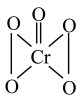
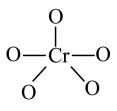
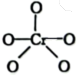
(4)CrO5中Cr元素化合价为+6价,常温下呈蓝色,则其结构式可能为___________ (填标号)。
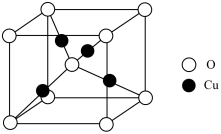
(5)某含铬化合物立方晶胞如图所示。该晶体的化学式为___________ ;与Cr最近的氧原子的个数为___________ ;Ca和Cr的最近距离为a nm,设NA为阿伏加德罗常数的值,则该晶体密度为__________ (填含a、NA的表达式)g·cm-3。
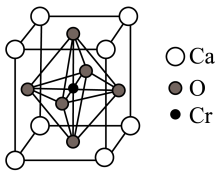
(1)基态铬原子的价电子排布式为
(2)同周期元素Si、P、S的第一电离能由大到小的顺序为
(3)硫元素能形成多种微粒如H2S、SO2、SO3、
(4)CrO5中Cr元素化合价为+6价,常温下呈蓝色,则其结构式可能为
 |  |  |
| A | B | C |

我国科学家研究发现 (
( 家族成员之一,A为一价金属,M为三价金属,X为氧族元素)在室温下具有超离子行为。回答下列问题:
家族成员之一,A为一价金属,M为三价金属,X为氧族元素)在室温下具有超离子行为。回答下列问题:
(1)基态铬原子M层的电子排布式为_______ ;基态硫原子核外电子中含有_______ 个未成对电子。
(2)同周期元素Si、P、S的电负性由大到小的顺序为_______ (用元素符号表示),O、S为同主族元素, 的键角比
的键角比 大的原因是
大的原因是_______ 。
(3)硫元素能形成多种微粒如 、
、 、
、 、
、 、
、 等,
等, 的中心原子的价层电子对数为
的中心原子的价层电子对数为_______ , 的空间构型为
的空间构型为_______ 。
(4) 中
中 元素化合价为+6价,常温下呈蓝色,则其结构式可能为
元素化合价为+6价,常温下呈蓝色,则其结构式可能为_______ (填标号)。
(5)某含铬化合物立方晶胞如图所示。该晶体的化学式为_______ ;与Cr最近的氧原子的个数为_______ ; 和
和 的最近距离为a nm,设
的最近距离为a nm,设 为阿伏加德罗常数的值,则该晶体密度为
为阿伏加德罗常数的值,则该晶体密度为_______  (填含a、
(填含a、 的表达式)。
的表达式)。

(1)基态铬原子M层的电子排布式为
(2)同周期元素Si、P、S的电负性由大到小的顺序为
(3)硫元素能形成多种微粒如
(4)
 |  |  |
| A | B | C |

组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网