解答题-原理综合题 较难0.4 引用1 组卷90
铵盐是比较重要的盐类物质,请回答下列问题。
(1)草酸是二元弱酸,能形成两种铵盐。
①(NH4)2C2O4溶液呈酸性,溶液中HC2O 、 C2O
、 C2O 、NH
、NH 、H2C2O4、 H+五种粒子浓度由大到小的顺序为
、H2C2O4、 H+五种粒子浓度由大到小的顺序为_______ 。
②NH4HC2O4溶液中,c(H2C2O4)-c(C2O )=
)=_______ 。
(2)氯化铵是最常见的铵盐,在工业生产中用途广泛。
①常温下,向100 mL 0.2 mol·L-1的氨水中逐滴加入0.2 mol·L-1的盐酸,所得溶液的pH、溶液中NH 和NH3·H2O的物质的量分数与加入盐酸的体积的关系如图所示。
和NH3·H2O的物质的量分数与加入盐酸的体积的关系如图所示。
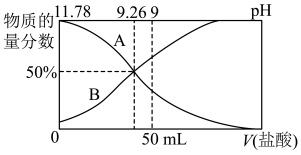
a.表示NH3·H2O物质的量分数变化的曲线是_______ (填“A”或“B”)。
b.NH3·H2O的电离常数为_______ 。
c.当加入盐酸的体积为50 mL时,溶液中c(NH )-c(NH3·H2O)=
)-c(NH3·H2O)=_______ mol·L-1(用式子表示)。
②常温下,在20 mL a mol·L-1氨水中滴加20 mL b mol·L-1盐酸恰好使溶液呈中性。常温下,NH 的水解常数Kh=
的水解常数Kh=_______ (用含a、b的代数式表示)。
(1)草酸是二元弱酸,能形成两种铵盐。
①(NH4)2C2O4溶液呈酸性,溶液中HC2O
②NH4HC2O4溶液中,c(H2C2O4)-c(C2O
(2)氯化铵是最常见的铵盐,在工业生产中用途广泛。
①常温下,向100 mL 0.2 mol·L-1的氨水中逐滴加入0.2 mol·L-1的盐酸,所得溶液的pH、溶液中NH

a.表示NH3·H2O物质的量分数变化的曲线是
b.NH3·H2O的电离常数为
c.当加入盐酸的体积为50 mL时,溶液中c(NH
②常温下,在20 mL a mol·L-1氨水中滴加20 mL b mol·L-1盐酸恰好使溶液呈中性。常温下,NH
21-22高二下·四川乐山·阶段练习
类题推荐
回答下列问题:
(1)根据表中数据回答下列问题。
①(NH4)2C2O4溶液呈酸性,溶液中各离子浓度由大到小的顺序为______ 。
②将0.1mol•L-1的Na2CO3溶液逐渐滴加到同浓度的HCN溶液中,写出发生反应的离子方程式______ 。
③浓度均为0.1mol•L-1的Na2CO3、NaHCO3、NaCN、NaHC2O4溶液,pH最大的是______ 。
(2)氮化铵是最常见的铵盐,在工业生产中用途广泛。
①热的浓氯化铵溶液可以清洗铁器表面锈迹,写出相关反应的离子方程式:______ 。
②常温下,向100mL0.2mol•L-1的氨水中逐滴加入0.2mol•L-1的盐酸,所得溶液的pH、溶液中NH 和NH3•H2O的物质的量分数与加入盐酸的体积的关系如图所示。
和NH3•H2O的物质的量分数与加入盐酸的体积的关系如图所示。
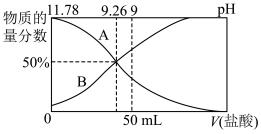
a.NH3•H2O的电离常数为______ 。
b.当加入盐酸的体积为50mL时,溶液中c(NH )-c(NH3•H2O)=
)-c(NH3•H2O)=______ mol•L-1(用式子表示即可,不用算出结果)。
③常温下,在20mLamol•L-1氨水中滴加20mLbmol•L-1盐酸恰好使溶液呈中性,常温下,NH 的水解常数Kh=
的水解常数Kh=______ (用含a、b的代数式表示)。
(1)根据表中数据回答下列问题。
| 酸 | H2C2O4 | HCN | H2CO3 |
| 电离常数(25℃) | K1=5.4×10-2 K2=5.4×10-5 | 4.9×10-10 | K1=4.4×10-7 K2=4.7×10-11 |
②将0.1mol•L-1的Na2CO3溶液逐渐滴加到同浓度的HCN溶液中,写出发生反应的离子方程式
③浓度均为0.1mol•L-1的Na2CO3、NaHCO3、NaCN、NaHC2O4溶液,pH最大的是
(2)氮化铵是最常见的铵盐,在工业生产中用途广泛。
①热的浓氯化铵溶液可以清洗铁器表面锈迹,写出相关反应的离子方程式:
②常温下,向100mL0.2mol•L-1的氨水中逐滴加入0.2mol•L-1的盐酸,所得溶液的pH、溶液中NH

a.NH3•H2O的电离常数为
b.当加入盐酸的体积为50mL时,溶液中c(NH
③常温下,在20mLamol•L-1氨水中滴加20mLbmol•L-1盐酸恰好使溶液呈中性,常温下,NH
已知常温下部分弱电解质的电离平衡常数如下表所示:
(1)25℃时,pH=10的NaClO溶液中各离子浓度的大小关系为_______ (离子浓度如Na+的浓度以c(Na+)表示,下同)。向NaClO溶液中通入少量CO2,反应的离子方程式为_______ 。
(2)NH4Cl溶液中的电荷守恒关系式为_______ 。
(3)NH4F溶液显_______ (填酸性、碱性或中性)。
(4)物质的量浓度相同的NaNO2、NaClO两种溶液,pH较大的是_______ 。
(5)泡沫灭火器利用了硫酸铝溶液和碳酸氢钠溶液的反应,用离子方程式表示原理_______ 。
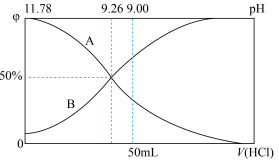
(6)常温下,向100mL0.2mol/L的氨水中逐滴加入0.2mol/L的盐酸,所得溶液的pH、溶液中 和NH3·H2O物质的量分数与加入盐酸的体积的关系如下图所示,根据图像回答下列问题。
和NH3·H2O物质的量分数与加入盐酸的体积的关系如下图所示,根据图像回答下列问题。_______ (填“A”或“B”)。
②当加入盐酸体积为50mL时,溶液中c( )∶c(NH3·H2O)=
)∶c(NH3·H2O)=_______ 。
| 化学式 | HF | HClO | H2CO3 | NH3·H2O | HNO2 |
| 电离常数 |
(1)25℃时,pH=10的NaClO溶液中各离子浓度的大小关系为
(2)NH4Cl溶液中的电荷守恒关系式为
(3)NH4F溶液显
(4)物质的量浓度相同的NaNO2、NaClO两种溶液,pH较大的是
(5)泡沫灭火器利用了硫酸铝溶液和碳酸氢钠溶液的反应,用离子方程式表示原理
(6)常温下,向100mL0.2mol/L的氨水中逐滴加入0.2mol/L的盐酸,所得溶液的pH、溶液中
②当加入盐酸体积为50mL时,溶液中c(
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网



