单选题 较难0.4 引用2 组卷288
如图为某实验测得0.10mol·L-1NaHCO3溶液在升温过程中(不考虑水挥发)的pH变化曲线。下列说法正确的是
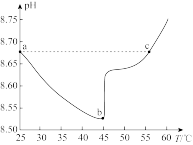

| A.ab段,pH减小说明升温促进了HCO |
| B.b点溶液恰好显中性 |
| C.a点溶液的c(OH-)比c点溶液的小 |
| D.a点时,Kw<Ka1(H2CO3)·Ka2(H2CO3) |
21-22高二上·福建福州·期末
类题推荐
实验测得0.1mol/LNaHCO3溶液的pH随温度升高的变化如图所示。
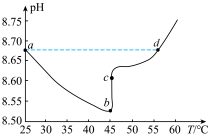
下列说法正确的是

下列说法正确的是
| A.由a点可知Ka1(H2CO3)•Ka2(H2CO3)>Kw |
| B.a→b,HCO |
| C. b→c,可能发生反应:2HCO |
| D.a点溶液和d点溶液的c(OH-)相同 |
I.已知25℃,H2CO3电离平衡常数Ka1=4.0×10-7,Ka2=5.0×10-11,回答下列问题:
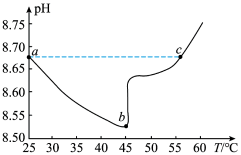
(1)如图为某实验测得0.1mol/LNaHCO3溶液在升温过程中(不考虑水挥发)的pH变化曲线。下列说法正确的是___________(填标号)。
(2)若定义pOH=-lgc(OH-),则25℃时0.01mol/LNa2CO3溶液的pOH为_______ (已知lg2=0.30)
(3)常温下,用NaOH溶液吸收CO2得到pH=8的混合溶液,则吸收过程中水的电离平衡______ (填“向左”“向右”或“不")移动。试计算所得溶液中c(H2CO3):c( )=
)=_______ 。
Ⅱ.0.010mol/L的一元酸HA溶液中HA、A-的物质的量分数δ(X)随pH变化如图所示。HA对应的电离平衡常数为Ka,由图确定下列数据:
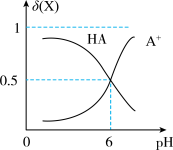
(4)K=___________ 。
(5)若将0.20mol/LNaA溶液和cmol/L盐酸等体积混合,若所得溶液为中性,则c=________ (结果保留两位小数)。
(1)如图为某实验测得0.1mol/LNaHCO3溶液在升温过程中(不考虑水挥发)的pH变化曲线。下列说法正确的是___________(填标号)。

| A.a点溶液的c(OH-)比c点溶液的小 |
| B.a点时,Kw<Ka1(H2CO3)·K2(H2CO3) |
| C.b点溶液中,c(Na+)+c(H+)=c( |
| D.ab段,pH减小说明升温抑制了 |
(3)常温下,用NaOH溶液吸收CO2得到pH=8的混合溶液,则吸收过程中水的电离平衡
Ⅱ.0.010mol/L的一元酸HA溶液中HA、A-的物质的量分数δ(X)随pH变化如图所示。HA对应的电离平衡常数为Ka,由图确定下列数据:

(4)K=
(5)若将0.20mol/LNaA溶液和cmol/L盐酸等体积混合,若所得溶液为中性,则c=
向100 mL 0.01 mol·L-1 Ba(OH)2(aq)中滴加0.1 mol·L-1 NaHCO3(aq),测得溶液电导率的变化如图。

下列说法错误的是

下列说法错误的是
| A.a→b发生的主要反应:Ba2++2OH-+2HCO |
| B.b→c,溶液中的c(OH-)减小 |
| C.c点溶液存在:c(OH-)-c(H+)=c(HCO |
| D.溶液中水的电离程度:c>b>a |
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


