解答题-工业流程题 适中0.65 引用1 组卷307
碳酸亚铁在干燥空气中为白色固体,可用于制铁盐、兽药、补血剂等。利用废铁屑(含少量碳、氧化铝和氧化铁杂质)为原料制取碳酸亚铁,并探究碳酸亚铁的部分性质。回答下列问题:
Ⅰ.制碳酸亚铁,工艺流程如图:
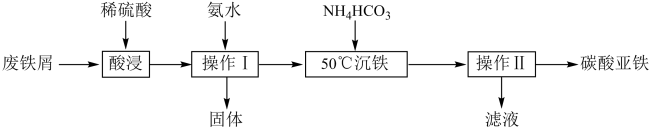
常温下几种金属阳离子开始沉淀与完全沉淀时的pH如表:
(1)酸浸时,所发生氧化还原反应的离子方程式为_______ 。
(2)加入氨水调控pH的范围是_______ ,“固体”的成分是_______ 。
(3)在工业生产中加入的NH4HCO3,需过量,下列分析错误的是_______ (填标号)。
a.使Fe2+充分转化为碳酸亚铁
b.碳酸氢铵受热分解
c.促进Fe2+、CO 的水解
的水解
Ⅱ.探究碳酸亚铁的性质
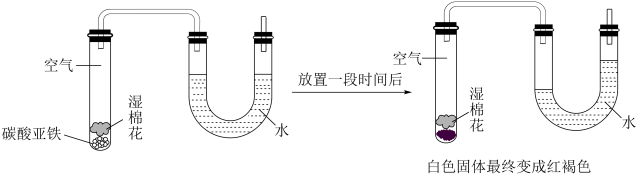
实验:
(4)由上面实验可以得出碳酸亚铁的相关性质是_______ ,写出碳酸亚铁变成红褐色固体所发生反应的化学方程式_______ 。
(5)已知:100.8≈6.3,25℃时,Ksp(FeCO3)=3.0×10-11、Ksp[Fe(OH)2]=1.6×10-14。现将碳酸亚铁加入0.1mol·L-1Na2CO3(pH=11.6)溶液中,经计算可知_______ (填“有”或“无”)Fe(OH)2生成。
Ⅰ.制碳酸亚铁,工艺流程如图:

常温下几种金属阳离子开始沉淀与完全沉淀时的pH如表:
| Fe2+ | Fe3+ | Al3+ | |
| 开始沉淀 | 7.5 | 2.7 | 3.8 |
| 完全沉淀 | 9.5 | 3.7 | 4.7 |
(1)酸浸时,所发生氧化还原反应的离子方程式为
(2)加入氨水调控pH的范围是
(3)在工业生产中加入的NH4HCO3,需过量,下列分析错误的是
a.使Fe2+充分转化为碳酸亚铁
b.碳酸氢铵受热分解
c.促进Fe2+、CO
Ⅱ.探究碳酸亚铁的性质

实验:
(4)由上面实验可以得出碳酸亚铁的相关性质是
(5)已知:100.8≈6.3,25℃时,Ksp(FeCO3)=3.0×10-11、Ksp[Fe(OH)2]=1.6×10-14。现将碳酸亚铁加入0.1mol·L-1Na2CO3(pH=11.6)溶液中,经计算可知
2022·四川德阳·二模
类题推荐
碱式碳酸钻[2CoCO3·3Co(OH)2·H2O]可用于催化剂、磁性材料研究等领域。现由某钴废料(主要含有Co,还有少量的Cu、Fe、Ca的化合物)制取碱式碳酸钴并分别回收铁、铜的工艺流程如下:
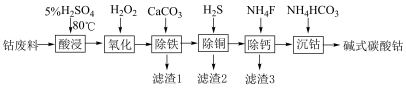
已知:含0.010mol/L金属离子的溶液,生成氢氧化物沉淀时的pH如下表。
回答下列问题:.
(1)“氧化”时加入H2O2的目的是______________ 。
(2)“除铁”时用CaCO3调节溶液pH的范围是___________ 。
(3)滤渣2的主要成分是______ (填化学式)。“除铜”时,通H2S之前,必须先过滤除去滤渣1的原因是______________ 。
(4)已知Ksp(CaF2)=4.0×10-9, =3.16。取“除铜”后的溶液100mL,其中c(Ca2+)=0.01mol/L,加入NH4F固体以除去Ca2+(忽略溶液体积的变化),当除钙率为96%时,溶液中c(F-)=
=3.16。取“除铜”后的溶液100mL,其中c(Ca2+)=0.01mol/L,加入NH4F固体以除去Ca2+(忽略溶液体积的变化),当除钙率为96%时,溶液中c(F-)=_______ mol/L。
(5)“沉钴”时发生反应的离子方程式为_______________ 。
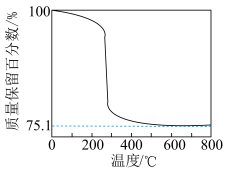
(6)已知碱式碳酸钴M=535g/mol。在空气中煅烧碱式碳酸钴[2CoCO3·3Co(OH)2·H2O]可得钴的某种氧化物,其热重曲线如图所示。经计算可知,800℃时所得钴的氧化物的化学式为____________ 。

已知:含0.010mol/L金属离子的溶液,生成氢氧化物沉淀时的pH如下表。
| Fe3+ | Fe2+ | Cu2+ | |
| 开始沉淀pH | 3.0 | 9.7 | 5.0 |
| 完全沉淀pH | 4.0 | 11.0 | 6.5 |
(1)“氧化”时加入H2O2的目的是
(2)“除铁”时用CaCO3调节溶液pH的范围是
(3)滤渣2的主要成分是
(4)已知Ksp(CaF2)=4.0×10-9,
(5)“沉钴”时发生反应的离子方程式为
(6)已知碱式碳酸钴M=535g/mol。在空气中煅烧碱式碳酸钴[2CoCO3·3Co(OH)2·H2O]可得钴的某种氧化物,其热重曲线如图所示。经计算可知,800℃时所得钴的氧化物的化学式为

工业上以菱锰矿(主要成分是MnCO3,还含有Fe2+、Ni2+等)为原料制备电解锰的工艺流程如图所示。

溶液中金属离子开始沉淀和完全沉淀的pH如下表所示:
回答下列问题:
(1)浸出槽中发生多个反应:如主要成分与稀硫酸的反应、MnO2与Fe2+间的氧化还原反应等。这两个反应的离子方程式分别为___________ 、___________ 。
(2)加入氨水的目的是为除去杂质,根据流程图及表中数据,pH应调控在___________ 范围内。常温下,Ksp[Fe(OH)3]=4.0×10-38,当pH=4时,溶液中c(Fe3+)=___________ 。
(3)加入硫化铵是为除去剩余的Ni2+,由此可判断相同温度下溶解度:NiS_______ Ni(OH)2(填“大于”或“小于”)。
(4)电解硫酸锰溶液的化学方程式为___________ 。
(5)工业上也可以用MnO2和Al粉作为原料,用铝热反应来制取金属锰,反应的化学方程式为_____ 。
(6)将分离出电解锰后的稀硫酸收集、循环使用,其意义是________ 。

溶液中金属离子开始沉淀和完全沉淀的pH如下表所示:
金属离子 | Ni2+ | Mn2+ | Fe3+ | Fe2+ |
| 开始沉淀时(c=0.01mol‧L-1)的pH | 7.2 | 8.3 | 2.2 | 7.5 |
| 沉淀完全时(c=1.0×10-5mol‧L-1)的pH | 8.7 | 9.8 | 3.2 | 9.0 |
(1)浸出槽中发生多个反应:如主要成分与稀硫酸的反应、MnO2与Fe2+间的氧化还原反应等。这两个反应的离子方程式分别为
(2)加入氨水的目的是为除去杂质,根据流程图及表中数据,pH应调控在
(3)加入硫化铵是为除去剩余的Ni2+,由此可判断相同温度下溶解度:NiS
(4)电解硫酸锰溶液的化学方程式为
(5)工业上也可以用MnO2和Al粉作为原料,用铝热反应来制取金属锰,反应的化学方程式为
(6)将分离出电解锰后的稀硫酸收集、循环使用,其意义是
金属回收与利用有利于环境保护。以某废渣(主要含Cd,还含少量Zn、Cu、Fe、Co等单质)为原料回收Cd,工艺流程如图所示:

已知几种金属离子沉淀的pH如表所示。
请回答下列问题:
(1)“酸浸”中加入稀硫酸,充分反应后过滤得到滤渣1的主要成分是_______ (填化学式)。
(2)“除钴”时,向含Co2+的浸液中加入Zn和Sb2O3,恰好产生CoSb合金,写出该反应的离子方程式:_______ 。若将该反应设计成原电池,锌在_______ 极发生反应。
(3)“除铁”时,先加入KMnO4氧化Fe2+ ,后加ZnO调溶液pH。加入ZnO调节溶液pH的范围为_______ 。 过滤,得滤渣2为MnO2和_______ (填化学式)。
(4)“电解”过程中以石墨为电极得到粗镉的电解总反应的化学方程式为_______ 。
(5)已知:常温下,Ksp[Cd(OH)2]≈2.0×10-16.如果用生石灰处理含Cd2+的电解废液,当pH=10时,c(Cd2+)=_______ mol/L。

已知几种金属离子沉淀的pH如表所示。
| 离子 | Fe3+ | Fe2+ | Cd2+ |
| 开始沉淀的pH | 1.5 | 6.5 | 7.2 |
| 完全沉淀的pH | 3.3 | 9.9 | ? |
请回答下列问题:
(1)“酸浸”中加入稀硫酸,充分反应后过滤得到滤渣1的主要成分是
(2)“除钴”时,向含Co2+的浸液中加入Zn和Sb2O3,恰好产生CoSb合金,写出该反应的离子方程式:
(3)“除铁”时,先加入KMnO4氧化Fe2+ ,后加ZnO调溶液pH。加入ZnO调节溶液pH的范围为
(4)“电解”过程中以石墨为电极得到粗镉的电解总反应的化学方程式为
(5)已知:常温下,Ksp[Cd(OH)2]≈2.0×10-16.如果用生石灰处理含Cd2+的电解废液,当pH=10时,c(Cd2+)=
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


