解答题-实验探究题 适中0.65 引用2 组卷266
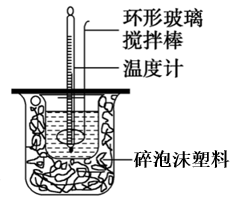
I.某同学设计下图简易装置测定中和热。回答下列问题:
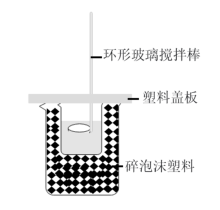
(1)该装置中缺少的仪器是___________ 。碎泡沫的作用:______
(2)50 mL 0.10 mol/L的盐酸与50 mL 0.11 mol/L的NaOH溶液混合后,测得反应放出的热量为285J,则中和热△H=___________ 。若将盐酸换成醋酸,会导致测定结果偏___________ (填小或者大)若将环形玻璃搅拌棒换为金属搅拌棒,则测得反应放出的热量将___________ (填“偏多”“偏少”或“不变”)。
II.氮是地球上含量丰富的一种元素,其单质及化合物在工农业生产、生活中有着重要作用。
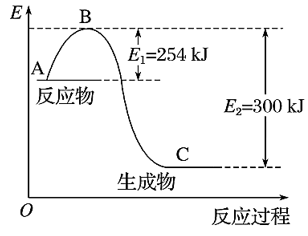
(3)如图是 1 mol NO2(g)和 1 mol CO(g)反应生成 1 mol CO2(g)和 1 mol NO(g)过程中能量变化示意图。
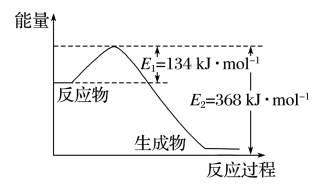
①该反应是___________ (填“吸热”或“放热”)反应。
②请写出反应的热化学方程式___________ 。
③若在该反应体系中加入催化剂对反应热___________ (填“有”或“没有”)影响。
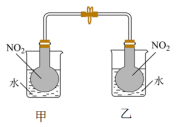
(4)已知,可逆反应2NO2(g) N2O4(g) ΔH = −56.9 kJ/mol。该反应正向是
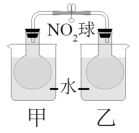
N2O4(g) ΔH = −56.9 kJ/mol。该反应正向是___________ 反应。(填放热或吸热)在乙烧杯中投入一定量的CaO固体,此烧杯中NO2球的红棕色变深。说明CaO与水反应是___________ 反应(填吸热或者放热)

(1)该装置中缺少的仪器是
(2)50 mL 0.10 mol/L的盐酸与50 mL 0.11 mol/L的NaOH溶液混合后,测得反应放出的热量为285J,则中和热△H=
II.氮是地球上含量丰富的一种元素,其单质及化合物在工农业生产、生活中有着重要作用。
(3)如图是 1 mol NO2(g)和 1 mol CO(g)反应生成 1 mol CO2(g)和 1 mol NO(g)过程中能量变化示意图。

①该反应是
②请写出反应的热化学方程式
③若在该反应体系中加入催化剂对反应热
(4)已知,可逆反应2NO2(g)

21-22高二上·新疆巴音郭楞·期中
类题推荐
I.某同学设计下图简易装置测定中和热。回答下列问题:
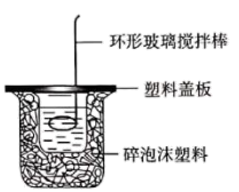
(1)该装置中缺少的仪器是___________ 。
(2)50mL 0.10mol/L的盐酸与50mL 0.11mol/L的NaOH溶液混合后,测得反应放出的热量为285J,则中和热 =
=___________ 。若将环形玻璃搅拌棒换为金属搅拌棒,则测得反应放出的热量将___________ (填“偏多”“偏少”或“不变”)。
Ⅱ.2021年世界环境日中国主题:人与自然和谐共生。
(3)以TiO2为催化剂的光热化学循环分解CO2反应为温室气体的减排提供了一个新途径,断开各分子中1mol化学键吸收的能量如下表所示,则以TiO2为催化剂分解CO2(g)生成CO(g)和O2(g)的热化学方程式为___________ 。
(4)以太阳能为热源,金属氧化物为催化剂可以分解水制H2和O2,实现能源绿色化,其过程如下:
过程Ⅰ:

过程Ⅱ:

总反应:

则过程Ⅱ的 =
=___________ 。

(1)该装置中缺少的仪器是
(2)50mL 0.10mol/L的盐酸与50mL 0.11mol/L的NaOH溶液混合后,测得反应放出的热量为285J,则中和热
Ⅱ.2021年世界环境日中国主题:人与自然和谐共生。
(3)以TiO2为催化剂的光热化学循环分解CO2反应为温室气体的减排提供了一个新途径,断开各分子中1mol化学键吸收的能量如下表所示,则以TiO2为催化剂分解CO2(g)生成CO(g)和O2(g)的热化学方程式为
| 化学键 | C=O | C≡O | O=O |
| 能量/J | 799 | 1072 | 496 |
(4)以太阳能为热源,金属氧化物为催化剂可以分解水制H2和O2,实现能源绿色化,其过程如下:
过程Ⅰ:
过程Ⅱ:
总反应:
则过程Ⅱ的
Ⅰ.分别取 盐酸与
盐酸与 溶液进行中和反应。通过测定反应过程中所放出的热量可计算中和热。回答下列问题:
溶液进行中和反应。通过测定反应过程中所放出的热量可计算中和热。回答下列问题:
(1)理论上稀强酸、稀强碱溶液反应生成1 mol水时放出57.3 kJ的热量,写出表示稀硫酸和稀NaOH溶液反应的中和热的热化学方程式:______ 。
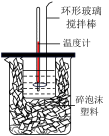
(2)如图,若将环形玻璃搅拌棒换成铜棒,会导致测定结果______ (填“偏低”“偏高”或“无影响”)。
依据该学生的实验数据计算,该实验测得的中和热
______ (结果保留一位小数)。[假设盐酸和NaOH溶液的密度都是 中和后生成溶液的比热容
中和后生成溶液的比热容 ]
]
(4)假定该学生的操作完全同上,实验中改用 盐酸与100 mL
盐酸与100 mL 溶液进行反应,与上述实验相比,所放出的热量
溶液进行反应,与上述实验相比,所放出的热量______ (填“相等”或“不相等”),所求中和热______ (填“相等”或“不相等”)。
Ⅱ.可逆反应 在平衡移动时的颜色变化可以用来指示放热过程和吸热过程。下面是某同学的部分实验报告。
在平衡移动时的颜色变化可以用来指示放热过程和吸热过程。下面是某同学的部分实验报告。
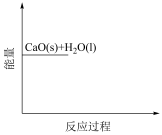
(5)根据甲烧杯中的现象,请画出CaO与 反应过程的能量变化示意图
反应过程的能量变化示意图______ 。 晶体溶于水是
晶体溶于水是_____ (填“放热”或“吸热”)过程,乙烧杯中 球的红棕色变浅,说明反应
球的红棕色变浅,说明反应 的
的
_____ 0(填“>”或“<”)。
(1)理论上稀强酸、稀强碱溶液反应生成1 mol水时放出57.3 kJ的热量,写出表示稀硫酸和稀NaOH溶液反应的中和热的热化学方程式:
(2)如图,若将环形玻璃搅拌棒换成铜棒,会导致测定结果
| 实验序号 | 起始温度 | 终止温度 | |
| 盐酸 | NaOH溶液 | 混合溶液 | |
| 1 | 20.0 | 20.1 | 23.2 |
| 2 | 20.2 | 20.4 | 23.4 |
| 3. | 20.5 | 20.6 | 23.6 |
(4)假定该学生的操作完全同上,实验中改用
Ⅱ.可逆反应
| 1.向甲烧杯中投入一定量的CaO固体,此烧杯中 2.向乙烧杯中加入 |
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网