解答题-结构与性质 适中0.65 引用2 组卷223
Mn和Ni是构成合金钢金(即铁合金)的主要元素。请回答下列问题:
(1)Mn在元素周期表中的位置_______ ,
(2)Ni的价电子排布式为_______ ,属于_______ 区的元素;
(3)过硫酸盐(S2O )氧化法常用于测定钢中锰的含量,H2S2O8的结构式如图所示,H2S2O8中S的轨道杂化方式为
)氧化法常用于测定钢中锰的含量,H2S2O8的结构式如图所示,H2S2O8中S的轨道杂化方式为_______ ;

(4)NiO、FeO属于_______ 晶体,已知r(Ni2+)>r(Fe2+),则熔点NiO_______ FeO(填“<"或“>’’),原因是_______ 。
(5)铜盐是自然界中重要的盐,向CuSO4溶液中加入过量稀氨水,所涉及的化学反应有_______ ,_______ ;
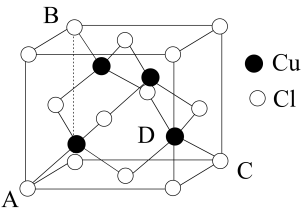
(6)已知CuCl的晶胞结构如图所示:晶胞中边长为688pm,阿伏加德罗常数的值为NA,则该晶体密度为_______ g·cm-3(列出计算式即可)。
(1)Mn在元素周期表中的位置
(2)Ni的价电子排布式为
(3)过硫酸盐(S2O

(4)NiO、FeO属于
(5)铜盐是自然界中重要的盐,向CuSO4溶液中加入过量稀氨水,所涉及的化学反应有
(6)已知CuCl的晶胞结构如图所示:晶胞中边长为688pm,阿伏加德罗常数的值为NA,则该晶体密度为

21-22高二下·重庆渝北·阶段练习
类题推荐
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网