解答题-结构与性质 适中0.65 引用1 组卷164
2020年10月,中国载人深潜器“奋斗者”号在马里亚纳海沟成功下潜突破1万米,“奋斗者”号选择了中国自主研发的全新高强高韧钛合金作为外壳材料,金属钛可用钙钛矿冶炼。请回答下列问题:
(1)Ti的四卤化物熔点如下表所示,TiF4熔点高于其他三种卤化物,自TiCl4至TiI4熔点依次升高,原因是___________ 。
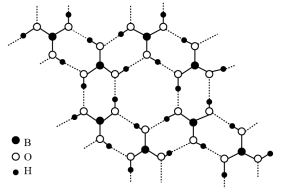
(2)常温常压下硼酸(H3BO3)晶体结构为层状,其二维平面结构如图。1mol硼酸(H3BO3)晶体中含有___________ mol氢键,从氢键的角度解释硼酸在冷水中的溶解度小而加热时溶解度增大:___________ 。
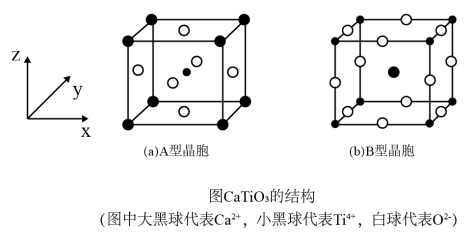
(3)钙钛矿(CaTiO3)的晶胞有A型和B型,将A型晶胞体心的Ti4+移至原点可得到B型晶胞。
①钛酸钙其中Ti4+的核外电子排布式为___________ ;钛酸钙中两种阳离子中半径较大的是___________ 。若某B型钙钛矿的晶胞密度为ρ g/cm3,NA为阿伏加德罗常数的值,晶胞中氧离子之间的最短距离为___________ cm(用含ρ和NA的代数式表示)。
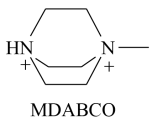
②某有机钙钛矿MDABCONH4I3具有A型钛酸钙晶胞结构。MDABCO的结构如图所示,则MDABCO所含元素电负性由大到小为___________ ,N原子的杂化轨道类型为___________ 。若在MDABCONH4I3的晶胞中MDABCO的分数坐标为(0,0,0),I-的一种分数坐标为( ,
, ,0),则
,0),则 的分数坐标为
的分数坐标为___________ ,与MDABCO距离最近的I-有___________ 个。
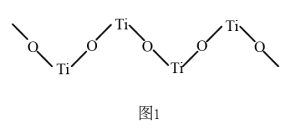
③TiO2难溶于水和稀酸,但能溶于浓硫酸,析出含有钛酰离子的晶体,钛酰离子常成为链状聚合形式的阳离子,其结构形式如图1,化学式为___________ 。
(1)Ti的四卤化物熔点如下表所示,TiF4熔点高于其他三种卤化物,自TiCl4至TiI4熔点依次升高,原因是
| 化合物 | TiF4 | TiCl4 | TiBr4 | TiI4 |
| 熔点/℃ | 377 | -24.12 | 38.3 | 155 |
(2)常温常压下硼酸(H3BO3)晶体结构为层状,其二维平面结构如图。1mol硼酸(H3BO3)晶体中含有

(3)钙钛矿(CaTiO3)的晶胞有A型和B型,将A型晶胞体心的Ti4+移至原点可得到B型晶胞。

①钛酸钙其中Ti4+的核外电子排布式为
②某有机钙钛矿MDABCONH4I3具有A型钛酸钙晶胞结构。MDABCO的结构如图所示,则MDABCO所含元素电负性由大到小为

③TiO2难溶于水和稀酸,但能溶于浓硫酸,析出含有钛酰离子的晶体,钛酰离子常成为链状聚合形式的阳离子,其结构形式如图1,化学式为

21-22高二上·四川内江·阶段练习
类题推荐
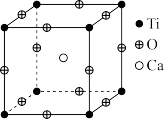
在高温超导领域,有一类化合物是钙钛矿型材料,此类化合物中最早被发现的是钛酸钙,其晶胞结构如图所示。试回答下列问题:
(1)基态Ti原子的核外电子排布式为____ 。
(2)Ti的四卤化物熔点如表所示,TiF4熔点高于其他三种卤化物,自TiCl4至TiI4熔点依次升高,原因是____ 。
(3)该钙钛矿的化学式为____ ,其组成元素的电负性由大到小的顺序是____ ;金属离子与氧离子间的作用力为____ ,该晶体中每个氧离子周围与它最近且距离相等的氧离子有____ 个。若晶胞参数为a pm,则晶体密度为____ g·cm-3(列出计算式,用NA表示阿伏加德罗常数的值)。

(1)基态Ti原子的核外电子排布式为
(2)Ti的四卤化物熔点如表所示,TiF4熔点高于其他三种卤化物,自TiCl4至TiI4熔点依次升高,原因是
| 化合物 | TiF4 | TiCl4 | TiBr4 | TiI4 |
| 熔点/℃ | 377 | -24.12 | 38.3 | 155 |
钛(Ti)被称为“未来金属”,其化合物广泛用于国防、电讯器材、医疗器械和化工设备等领域。回答下列问题:
(1)基态钛原子的价电子排布式为___________ ,与钛同周期的元素中,基态原子的未成对电子数与钛相同的有___________ 种。
(2)Ti的四卤化物熔点如下表所示,TiF4熔点高于其它三种卤化物,自TiCl4至TiI4熔点依次升高,原因是___________ 。
(3)Ti(IV)的某配合物可用于催化环烯烃聚合,其结构如图所示:___________ 。
②请在图中标出配位键___________ (用“→”表示);
③配合物中非金属元素的含氧酸根的中心原子杂化轨道类型是sp2的是___________ 。
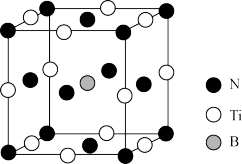
(4)用B掺杂TiN后(晶胞结构中只是B原子部分代替钛原子),其晶胞结构如图所示,距离Ti最近的B有___________ 个,Ti与B的最近距离为___________ nm;掺杂B后的晶体密度是TiN晶体的___________ 倍。(已知掺杂B后的晶体密度为ρg/cm3,阿伏加德罗常数的值为NA)
(1)基态钛原子的价电子排布式为
(2)Ti的四卤化物熔点如下表所示,TiF4熔点高于其它三种卤化物,自TiCl4至TiI4熔点依次升高,原因是
| 化合物 | TiF4 | TiCl4 | TiBr4 | TiI4 |
| 熔点/℃ | 377 | -24.12 | 38.3 | 155 |
(3)Ti(IV)的某配合物可用于催化环烯烃聚合,其结构如图所示:

②请在图中标出配位键
③配合物中非金属元素的含氧酸根的中心原子杂化轨道类型是sp2的是
(4)用B掺杂TiN后(晶胞结构中只是B原子部分代替钛原子),其晶胞结构如图所示,距离Ti最近的B有
钙钛矿(CaTiO3)型化合物是一类可用于生产太阳能电池、传感器、固体电阻器等的功能材料,回答下列问题:
(1)基态Ti原子的核外电子排布式为______ 。
(2)Ti的四卤化物熔点如表所示,TiF4熔点明显高于其他三种卤化物,TiCl4至TiI4熔点依次升高,原因是_______ 。
(3)CaTiO3组成元素的电负性最大的为______ (用元素符号表示)。
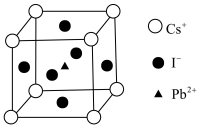
(4)某种金属卤化物无机钙钛矿的晶胞结构如图所示,晶胞的边长apm,则该物质的化学式为______ ;晶体的密度ρ=______ g•cm-3(设阿伏加德罗常数的值为NA,用含a、NA的代数式表示)。
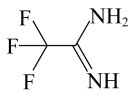
(5)我国科学家设计了一种钝化剂三氟乙脒(结构如图所示)来抑制上述金属卤化物钙钛矿晶粒表面缺陷,其中σ键与π键数目之比为______ ,两个碳原子的杂化类型分别为______ 。
(1)基态Ti原子的核外电子排布式为
(2)Ti的四卤化物熔点如表所示,TiF4熔点明显高于其他三种卤化物,TiCl4至TiI4熔点依次升高,原因是
| 化合物 | TiF4 | TiCl4 | TiBr4 | TiI4 |
| 熔点/℃ | 377 | -24.12 | 38.3 | 155 |
(4)某种金属卤化物无机钙钛矿的晶胞结构如图所示,晶胞的边长apm,则该物质的化学式为

(5)我国科学家设计了一种钝化剂三氟乙脒(结构如图所示)来抑制上述金属卤化物钙钛矿晶粒表面缺陷,其中σ键与π键数目之比为

组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


