解答题-原理综合题 适中0.65 引用1 组卷455
氨气中氢含量高,是一种优良的小分子储氢载体,且安全、易储运;氨气及铵盐同时也是空气和水体污染物,需用化学方法除去。
Ⅰ.氨热分解法制氢气:
(1)已知反应
 kJ/mol,在
kJ/mol,在___________ (较高/较低)温度下反应能自发进行。
(2)某兴趣小组对该反应进行了实验探究。在一定温度和催化剂的条件下,将0.1mol 通入3L的密闭容器中进行反应(此时容器内总压为200kPa),各物质的分压随时间的变化曲线如图所示。
通入3L的密闭容器中进行反应(此时容器内总压为200kPa),各物质的分压随时间的变化曲线如图所示。
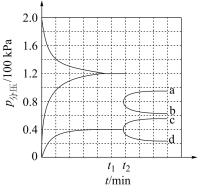
①若保持容器体积不变, 时反应达到平衡,用H2的浓度变化表示0~
时反应达到平衡,用H2的浓度变化表示0~ 时间内的反应速率v(H2)
时间内的反应速率v(H2)______  (用含
(用含 的代数式表示)
的代数式表示)
② 时将容器体积迅速缩小至原来的一半并保持不变,图中能正确表示压缩后
时将容器体积迅速缩小至原来的一半并保持不变,图中能正确表示压缩后 分压变化趋势的曲线是
分压变化趋势的曲线是______ (用图中a、b、c、d表示)。
③下列措施一定可以提高平衡体系中 的体积分数,又能加快反应速率的是
的体积分数,又能加快反应速率的是___________ 。
a.适当升高温度 b.适当降低温度 c.加入催化剂 d.降低压强 e.将生成物中的氮气液化分离出体系
(3)Ⅱ:某研究小组用NaClO氧化法处理氨氮废水,使氨氮(包含 、
、 等微粒)完全氧化成氮气而减少水污染。氧化过程中进水pH对氨氮去除率的影响如图所示:
等微粒)完全氧化成氮气而减少水污染。氧化过程中进水pH对氨氮去除率的影响如图所示:
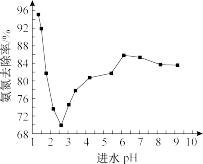
(已知:HClO的氧化性比NaClO强;NH3比 更易被氧化)
更易被氧化)
①氨氮去除率随进水pH的增大先降低后升高的原因为___________ 。
②电化学除氨原理为:氨氮被电极表面产生的强氧化性物质氧化而去除,实际过程中在氨氮废水中投加氯离子,能显著提高去除效率,其原因是___________ 。(排除导电性变化原因)
Ⅰ.氨热分解法制氢气:
(1)已知反应
(2)某兴趣小组对该反应进行了实验探究。在一定温度和催化剂的条件下,将0.1mol

①若保持容器体积不变,
②
③下列措施一定可以提高平衡体系中
a.适当升高温度 b.适当降低温度 c.加入催化剂 d.降低压强 e.将生成物中的氮气液化分离出体系
(3)Ⅱ:某研究小组用NaClO氧化法处理氨氮废水,使氨氮(包含

(已知:HClO的氧化性比NaClO强;NH3比
①氨氮去除率随进水pH的增大先降低后升高的原因为
②电化学除氨原理为:氨氮被电极表面产生的强氧化性物质氧化而去除,实际过程中在氨氮废水中投加氯离子,能显著提高去除效率,其原因是
2022·辽宁沈阳·二模
类题推荐
氨气中氢含量高,是一种优良的小分子储氢载体,且安全、易储运,可通过下面方法由氨气得到氢气。
方法:氨热分解法制氢气,反应2NH3(g) N2(g)+3H2(g) ΔH=+90.8 kJ·mol-1;
N2(g)+3H2(g) ΔH=+90.8 kJ·mol-1;
(1)已知该反应的ΔS=198.9 J·mol-1·K-1,在下列哪些温度下反应能自发进行?______(填字母);
(2)某兴趣小组对该反应进行了实验探究。在一定温度和催化剂的条件下,将0.1mol NH3通入2L的密闭容器中进行反应(此时容器内总压为200kPa),各物质的分压随时间的变化曲线如图所示。
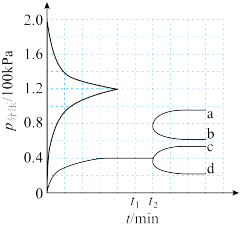
①若保持容器体积不变,t1时反应达到平衡,用H2的浓度变化表示0~t1时间内的反应速率v(H2)=___________ mol·L-1·min-1(用含t1的代数式表示)。
②t2时将容器体积迅速缩小至原来的一半并保持不变,图中能正确表示压缩后N2分压变化趋势的曲线是___________ (用图中a、b、c、d表示),理由是___________ 。
方法:氨热分解法制氢气,反应2NH3(g)
(1)已知该反应的ΔS=198.9 J·mol-1·K-1,在下列哪些温度下反应能自发进行?______(填字母);
| A.25 ℃ | B.125 ℃ | C.225 ℃ | D.325 ℃ |
(2)某兴趣小组对该反应进行了实验探究。在一定温度和催化剂的条件下,将0.1mol NH3通入2L的密闭容器中进行反应(此时容器内总压为200kPa),各物质的分压随时间的变化曲线如图所示。

①若保持容器体积不变,t1时反应达到平衡,用H2的浓度变化表示0~t1时间内的反应速率v(H2)=
②t2时将容器体积迅速缩小至原来的一半并保持不变,图中能正确表示压缩后N2分压变化趋势的曲线是
氨气中氢含量高,是一种优良的小分子储氢载体,且安全、易储运,可通过下面两种方法由氨气得到氢气。
方法Ⅰ:氨热分解法制氢气。相关化学键的键能数据如下:
一定温度下,利用催化剂将 分解为
分解为 和
和 。回答下列问题:
。回答下列问题:
(1)反应

___________  。
。
(2)此反应在___________ (填“高温”或“低温”)条件下能自发进行。
(3)某兴趣小组对该反应进行了实验探究。在一定温度和催化剂的条件下,将0.1mol 通入3L的密闭容器中进行反应(此时容器内总压为200kPa),各物质的分压随时间的变化曲线如图所示。
通入3L的密闭容器中进行反应(此时容器内总压为200kPa),各物质的分压随时间的变化曲线如图所示。

①若保持容器体积不变, 时反应达到平衡,用
时反应达到平衡,用 的压强变化表示0~
的压强变化表示0~ 时间内的反应速率
时间内的反应速率
___________ Kpa/min(用含 的代数式表示)。
的代数式表示)。
② 时将容器体积迅速缩小至原来的一半并保持不变,图中能正确表示压缩后
时将容器体积迅速缩小至原来的一半并保持不变,图中能正确表示压缩后 分压变化趋势的曲线是
分压变化趋势的曲线是___________ (用图中a、b、c、d表示),理由是___________ 。
③在该温度下,反应的标准平衡常数
___________ 。(已知:分压=总压×该组分物质的量分数,对于反应 ,
, ,其中
,其中 ,
, 、
、 、
、 、
、 为各级分的平衡分压。)
为各级分的平衡分压。)
方法Ⅰ:氨热分解法制氢气。相关化学键的键能数据如下:
| 化学键 | N≡N | H—H | N—H |
| 键能( | 946.0 | 436.0 | 390.8 |
(1)反应
(2)此反应在
(3)某兴趣小组对该反应进行了实验探究。在一定温度和催化剂的条件下,将0.1mol

①若保持容器体积不变,
②
③在该温度下,反应的标准平衡常数
氨气中氢含量高,是一种优良的小分子储氢载体,且安全、易储运,可通过下面方法由氨气得到氢气。
方法:氨热分解法制氢气
反应2NH3(g) N2(g)+3H2(g) ΔH=+90.8 kJ·mol-1;
N2(g)+3H2(g) ΔH=+90.8 kJ·mol-1;
(1)已知该反应的ΔS=198.9 J·mol-1·K-1,在下列哪些温度下反应能自发进行?___________(填字母);
(2)某兴趣小组对该反应进行了实验探究。在一定温度和催化剂的条件下,将0.1mol NH3通入3L的密闭容器中进行反应(此时容器内总压为200kPa),各物质的分压随时间的变化曲线如图所示。

①若保持容器体积不变,t1时反应达到平衡,用H2的浓度变化表示0~t1时间内的反应速率v(H2)=___________ mol·L-1·min-1(用含t1的代数式表示);
②t2时将容器体积迅速缩小至原来的一半并保持不变,图中能正确表示压缩后N2分压变化趋势的曲线是___________ (用图中a、b、c、d表示),理由是___________ ;
③在该温度下,反应的标准平衡常数Kθ=___________ 。(已知:分压=总压×该组分物质的量分数,对于反应dD(g)+eE(g) gG(g)+hH(g),Kθ=
gG(g)+hH(g),Kθ= ,其中pθ=100 kPa,pG、pH、pD、pE为各组分的平衡分压)。
,其中pθ=100 kPa,pG、pH、pD、pE为各组分的平衡分压)。
方法:氨热分解法制氢气
反应2NH3(g)
(1)已知该反应的ΔS=198.9 J·mol-1·K-1,在下列哪些温度下反应能自发进行?___________(填字母);
| A.25 ℃ | B.125 ℃ | C.225 ℃ | D.325 ℃ |

①若保持容器体积不变,t1时反应达到平衡,用H2的浓度变化表示0~t1时间内的反应速率v(H2)=
②t2时将容器体积迅速缩小至原来的一半并保持不变,图中能正确表示压缩后N2分压变化趋势的曲线是
③在该温度下,反应的标准平衡常数Kθ=
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


