单选题 适中0.65 引用1 组卷142
利用Cu+2FeCl3=CuCl2+2FeCl2,可设计如图所示原电池装置,下列说法不正确的是
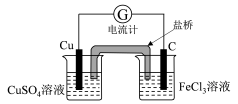

| A.该电池的负极是Cu |
| B.电池工作过程中,电子流向为:Cu→盐桥→C |
| C.盐桥中阳离子进入右池 |
| D.正极电极反应为:Fe3++e-=Fe2+ |
19-20高二上·重庆·期末
类题推荐
如图是某同学设计的原电池装置,下列叙述中正确的是
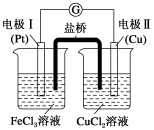

| A.电极I上发生还原反应,作原电池的负极 |
| B.电极Ⅱ的电极反应为Cu2++2e-=Cu |
| C.盐桥中的阴离子向FeCl3溶液中迁移 |
| D.该原电池的总反应为2Fe3++Cu=Cu2++2Fe2+ |
如下图所示原电池的总反应为:Cu+2Ag+ Cu2++2Ag,下列叙述正确的是
Cu2++2Ag,下列叙述正确的是
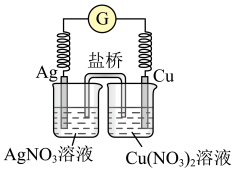

| A.反应过程中银电极上有气泡 |
| B.盐桥中阳离子进入右池 |
| C.电池工作时,电子流向为:Cu→盐桥→Ag |
| D.工作一段时间后,右烧杯中电极重量减轻 |
某铜锌原电池的结构如图所示,下列说法正确的是
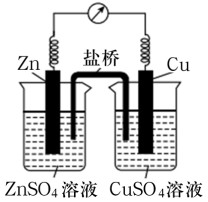

| A.Zn电极为该原电池的正极 |
| B.电池工作时,电子由Zn电极流出,经溶液和盐桥流入Cu电极 |
| C.Cu电极上的电极反应式为Cu-2e-=Cu2+ |
| D.若盐桥中的电解质为KCl,则电池工作时K+向右侧移动 |
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


