解答题-工业流程题 较难0.4 引用5 组卷855
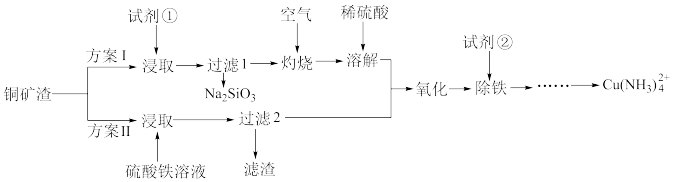
铜氨溶液在纤维工业有广泛应用。实验室模拟用废弃辉铜矿渣(主要含Cu2S,还含有少量FeS、SiO2)为原料制备Cu(NH3) 的流程如图:
的流程如图:
已知:常温下,Ksp[Cu(OH)2]=2×10-20,Cu2++4NH3 Cu(NH3)
Cu(NH3) K=1×1013
K=1×1013
回答下列问题:
(1)实验前将矿渣粉碎的目的是________ ,方案I中试剂①是________ 。
(2)方案II中,“过滤2”所得滤渣的主要成分除S外,还有________ (填化学式)。Cu2S和硫酸铁溶液反应的离子方程式是________ 。
(3)“除铁”前,“氧化”的目的是________ ,试剂②最好选用________ (填化学式)。如何证明铁元素被完全除尽?________ 。
(4)从环保角度看,两种方案更优的是________ 。
(5)常温下,向CuSO4溶液中加入浓氨水,生成Cu(OH)2沉淀,继续加入浓氨水,沉淀溶解生成Cu(NH3) 。沉淀开始溶解时溶液的pH为10,则
。沉淀开始溶解时溶液的pH为10,则 =
=________ 。

已知:常温下,Ksp[Cu(OH)2]=2×10-20,Cu2++4NH3
回答下列问题:
(1)实验前将矿渣粉碎的目的是
(2)方案II中,“过滤2”所得滤渣的主要成分除S外,还有
(3)“除铁”前,“氧化”的目的是
(4)从环保角度看,两种方案更优的是
(5)常温下,向CuSO4溶液中加入浓氨水,生成Cu(OH)2沉淀,继续加入浓氨水,沉淀溶解生成Cu(NH3)
2022·云南昆明·一模
类题推荐
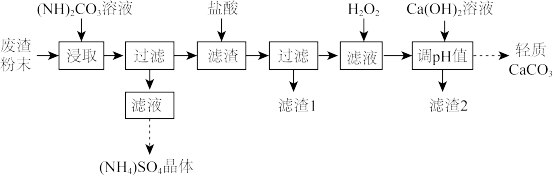
实验室以工业废渣(主要含CaSO4∙2H2O,还含少量SiO2、Al2O3、FeO、Fe2O3)为原料制取(NH4)2SO4晶体和轻质CaCO3,其实验流程如下:
已知:①金属离子形成氢氧化物沉淀的pH范围(pH=8.5时Al(OH)3开始溶解)
②已知常温下,Ksp(CaSO4)=4.8×10-5,Ksp(CaCO3)=3×10-9
回答下列问题:
(1)废渣粉末“浸取”时,主要反应的离子方程式为_____________________________ 。实验时需向(NH4)2CO3溶液中加入适量浓氨水的目的是______________________ 。
(2)废渣粉末“浸取”时,反应温度需控制在60~70℃,合适的加热方式为_________ 。若温度过高将会导致CaSO4的转化率下降,其原因是_______________________ 。
(3)滤渣1成分是_______________ (填化学式)。
(4)加适量H2O2的作用是________________________________ (用离子方程式表示)。“调pH值”除铁和铝时,应调节溶液的pH范围为_________________ 。

已知:①金属离子形成氢氧化物沉淀的pH范围(pH=8.5时Al(OH)3开始溶解)
| 金属离子 | Al3+ | Fe3+ | Fe2+ | Ca2+ |
| 开始沉淀时pH | 3.4 | 2.7 | 7.6 | 11.3 |
| 完全沉淀时pH | 4.7 | 3.7 | 9.6 | / |
②已知常温下,Ksp(CaSO4)=4.8×10-5,Ksp(CaCO3)=3×10-9
回答下列问题:
(1)废渣粉末“浸取”时,主要反应的离子方程式为
(2)废渣粉末“浸取”时,反应温度需控制在60~70℃,合适的加热方式为
(3)滤渣1成分是
(4)加适量H2O2的作用是
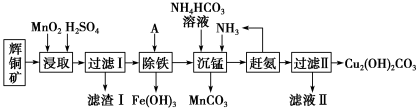
铜及其化合物在工业生产上有许多用途。某工厂以辉铜矿(主要成分为Cu2S,含少量Fe2O3、SiO2等杂质)为原料制备不溶于水的碱式碳酸铜的流程如下:
已知:①常温下几种物质开始形成沉淀与完全沉淀时的pH如下表
②Ksp[Fe(OH)3]=4.0×10-38
(1)滤渣I中主要成分是MnO2、S、SiO2,写出“浸取”反应中生成S的化学方程式:___________ 。
(2)常温下“除铁”时加入的试剂A可用CuO等,调节pH调的范围为___________ ,若加A后溶液的pH调为5,则溶液中Fe3+的浓度为___________ mol/L。
(3)写出“沉锰”(除Mn2+)过程中反应的离子方程式:___________ 。
(4)“赶氨”时,最适宜的操作方法是___________ 。
(5)滤液Ⅱ经蒸发结晶得到的盐主要是___________ (写化学式)。

已知:①常温下几种物质开始形成沉淀与完全沉淀时的pH如下表
| 金属离子 | Fe2+ | Fe3+ | Cu2+ | Mn2+ |
| 开始沉淀 | 7.5 | 2.7 | 5.6 | 8.3 |
| 完全沉淀 | 9.0 | 3.7 | 6.7 | 9.8 |
(1)滤渣I中主要成分是MnO2、S、SiO2,写出“浸取”反应中生成S的化学方程式:
(2)常温下“除铁”时加入的试剂A可用CuO等,调节pH调的范围为
(3)写出“沉锰”(除Mn2+)过程中反应的离子方程式:
(4)“赶氨”时,最适宜的操作方法是
(5)滤液Ⅱ经蒸发结晶得到的盐主要是
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网



