单选题 适中0.65 引用2 组卷395
用久置于空气中的生石灰[主要成分为CaO,还含有Ca(OH)2和CaCO3]制取KClO3的流程如下:
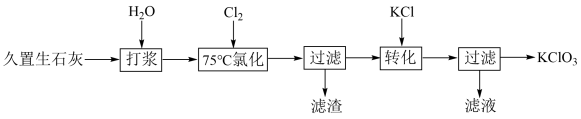
已知75℃时,Cl2在碱性条件下会转化为Cl-和 ,室温下KClO3的溶解度远小于KCl。下列说法正确的是
,室温下KClO3的溶解度远小于KCl。下列说法正确的是

已知75℃时,Cl2在碱性条件下会转化为Cl-和

| A.氯化反应的离子方程式为Cl2+4OH- |
| B.转化时发生反应的类型为复分解反应 |
| C.滤液中大量存在的离子是Ca2+、K+、Cl-和 |
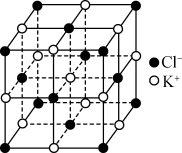
| D.如图所示KCl晶胞中含有14个K+ |
2022·江苏·一模
类题推荐
较低温度下,Cl2遇碱转化为Cl-和C1O-;较高温度下氯气和碱转化为Cl-和 。用久置空气中的生石灰制取KClO3的流程如下。
。用久置空气中的生石灰制取KClO3的流程如下。
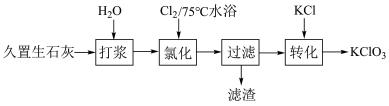
下面有关说法不正确的是
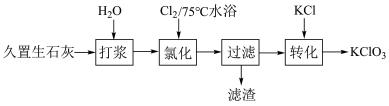
下面有关说法不正确的是
| A.久置生石灰中含有碱性氧化物、碱和盐 |
| B.“氯化”中主要发生的化学反应为 |
| C.“过滤”得到滤渣中的碳酸钙加工成为纳米碳酸钙,分散到水中即得到碳酸钙胶体 |
| D.“转化”时发生的化学反应属于氧化还原反应 |
以电石渣[主要成分为Ca(OH)2和CaCO3]为原料制备KClO3的步骤如下:
步骤1:将电石渣与水混合,形成浆料。
步骤2:控制电石渣过量,75℃时向浆料中通入Cl2,该过程生成Ca(ClO)2,Ca(ClO)2进一步转化为Ca(ClO3)2,少量Ca(ClO)2分解为CaCl2和O2。氯化过程中Cl2转化为Ca(ClO3)2的总反应方程式为 。充分反应后过滤。
。充分反应后过滤。
步骤3:向滤液中加入稍过量KCl固体,蒸发浓缩、冷却至25℃结晶,得KClO3。
下列说法正确的是
步骤1:将电石渣与水混合,形成浆料。
步骤2:控制电石渣过量,75℃时向浆料中通入Cl2,该过程生成Ca(ClO)2,Ca(ClO)2进一步转化为Ca(ClO3)2,少量Ca(ClO)2分解为CaCl2和O2。氯化过程中Cl2转化为Ca(ClO3)2的总反应方程式为
步骤3:向滤液中加入稍过量KCl固体,蒸发浓缩、冷却至25℃结晶,得KClO3。
下列说法正确的是
| A.控制通入 |
| B.25℃时, |
| C.步骤2中,过滤所得滤液中 |
| D.生成 |
以电石渣[主要成分为Ca(OH)2和CaCO3]为原料制备KClO3的步骤如下:
步骤1:将电石渣与水混合,形成浆料。
步骤2:控制电石渣过量,75℃时向浆料中通入Cl2,该过程会生成Ca(ClO)2,Ca(ClO)2会进一步转化为Ca(ClO3)2,少量Ca(ClO)2分解为CaCl2和O2,过滤。
步骤3:向滤液中加入稍过量KCl固体,蒸发浓缩、冷却至25℃结晶,得KClO3。
下列说法正确的是
步骤1:将电石渣与水混合,形成浆料。
步骤2:控制电石渣过量,75℃时向浆料中通入Cl2,该过程会生成Ca(ClO)2,Ca(ClO)2会进一步转化为Ca(ClO3)2,少量Ca(ClO)2分解为CaCl2和O2,过滤。
步骤3:向滤液中加入稍过量KCl固体,蒸发浓缩、冷却至25℃结晶,得KClO3。
下列说法正确的是
| A.控制通入Cl2的速率,可以提高Cl2的利用率 |
| B.25℃时,Ca(ClO3)2的溶解度比KClO3的溶解度小 |
| C.步骤2中,过滤所得滤液中 |
| D.生成 Ca(ClO)2的化学方程式为 |
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


