解答题-原理综合题 适中0.65 引用2 组卷198
汽车尾气主要含有一氧化碳、二氧化硫、一氧化氮等物质,是造成城市空气污染的主要因素之一、请回答下列问题:
(1)目前解决汽车尾气污染问题所采取的措施主要有___________ (至少填两种)。
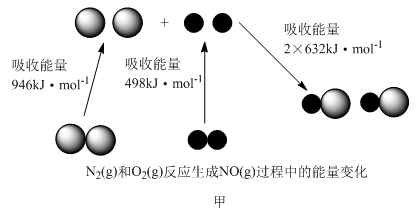
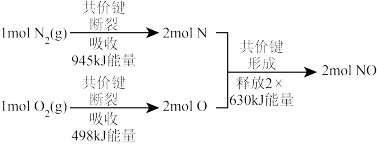
(2)已知汽缸中氮气和氧气反应生成一氧化氮的能量变化值如图所示,则由该反应生成1molNO时,应___________ (填“释放”或“吸收”)___________ kJ能量。
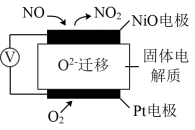
(3)通过NO传感器可监测汽车尾气中NO的含量,其工作原理如图所示:
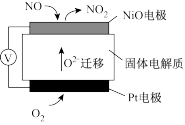
①Pt电极上发生的是___________ 反应(填“氧化”或“还原”)。
②外电路中,电子流动方向是从___________ 电极流向___________ 电极(填“NiO”或“Pt”)。
③NiO电极上的电极反应式为___________ 。
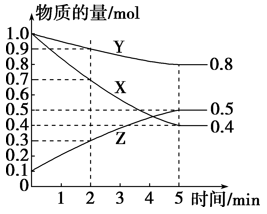
(4)在恒温恒容的密闭容器中,充入等物质的量的CO和NO混合气体,发生如下反应:2CO(g)+2NO(g)⇌2CO2(g)+N2(g),t0时达到平衡,测得反应过程中CO2的体积分数与时间的关系如下图所示。
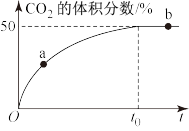
①比较大小:a处v正___________ b处v逆(填“>”、“<”或“=”)
②平衡后往该密闭容器中再充入一定量的氦气,则CO2的体积分数___________ 50%。(填“>”、“<”或“=”)
③能说明上述反应已达化学平衡状态的是___________ (填字母)。
A.v正(CO)=v逆(NO) B.混合气体密度保持不变
C.反应容器内压强保持不变 D.混合气体的平均摩尔质量不变
(1)目前解决汽车尾气污染问题所采取的措施主要有
(2)已知汽缸中氮气和氧气反应生成一氧化氮的能量变化值如图所示,则由该反应生成1molNO时,应

(3)通过NO传感器可监测汽车尾气中NO的含量,其工作原理如图所示:

①Pt电极上发生的是
②外电路中,电子流动方向是从
③NiO电极上的电极反应式为
(4)在恒温恒容的密闭容器中,充入等物质的量的CO和NO混合气体,发生如下反应:2CO(g)+2NO(g)⇌2CO2(g)+N2(g),t0时达到平衡,测得反应过程中CO2的体积分数与时间的关系如下图所示。

①比较大小:a处v正
②平衡后往该密闭容器中再充入一定量的氦气,则CO2的体积分数
③能说明上述反应已达化学平衡状态的是
A.v正(CO)=v逆(NO) B.混合气体密度保持不变
C.反应容器内压强保持不变 D.混合气体的平均摩尔质量不变
20-21高一下·福建宁德·期中
类题推荐
研究氮的氧化物\碳的氧化物等大气污染物的处理有重要意义。
(1)汽车尾气中NO生成过程中的能量变化如图所示。

生成1 mol NO(g)_______ ( 填“吸收"或“放出")_______ kJ 的热量。
(2)汽车排气管内安装的催化转化器可使尾气的主要污染物(NO和CO)转化为无毒的大气循环物质。一定温度下,在恒容密闭容器中发生反应:2NO(g)+2CO(g) 2CO2(g)+N2(g)。下列能判断该反应达到化学平衡状态的是_______(填序号)。
2CO2(g)+N2(g)。下列能判断该反应达到化学平衡状态的是_______(填序号)。
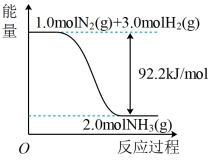
(3)用CO2和H2合成甲醇有利于减少碳排放,其反应原理为CO2(g) +3H2(g)=CH3OH(g) +H2O(g)。向甲、乙两个体积都为2.0L的恒容密闭容器中均充入1 mol CO2和3 mol H2,甲在T1乙在T2温度下发生上述反应,反应过程中n(CH3OH)随时间(t)的变化见下表:
①T1_______ T2(填“>”“<”或“=”)。
②甲容器中,0 ~6 min内的平均反应速率v(H2)=_______ 。
③甲容器中CO2的平衡转化率为_______
(4)一种室温下“可呼吸”的Na-CO2电池装置如图所示,电池的总反应为3CO2 +4Na=2Na2CO3+C。

①电极a为_______ 极(填“正”或“负")。
②电极b发生的电极反应为_______ 。
(1)汽车尾气中NO生成过程中的能量变化如图所示。

生成1 mol NO(g)
(2)汽车排气管内安装的催化转化器可使尾气的主要污染物(NO和CO)转化为无毒的大气循环物质。一定温度下,在恒容密闭容器中发生反应:2NO(g)+2CO(g)
| A.反应速率v(NO)=v(CO) | B.混合气体中NO的物质的量分数保持不变 |
| C.混合气体的密度不再改变 | D.混合气体的压强不再改变 |
| t/min | 0 | 3 | 6 | 12 | 24 | 36 |
| n甲(CH3OH)/mol | 0 | 0.36 | 0.60 | 0.82 | 0.80 | 0.80 |
| n乙(CH3OH)/mol | 0 | 0.30 | 0.50 | 0.68 | 0.85 | 0.85 |
②甲容器中,0 ~6 min内的平均反应速率v(H2)=
③甲容器中CO2的平衡转化率为
(4)一种室温下“可呼吸”的Na-CO2电池装置如图所示,电池的总反应为3CO2 +4Na=2Na2CO3+C。

①电极a为
②电极b发生的电极反应为
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网