解答题-实验探究题 适中0.65 引用1 组卷155
实验室可用乙酸和乙醇为原料制备乙酸乙酯,制备装置如图所示(夹持和加热装置已省略)。
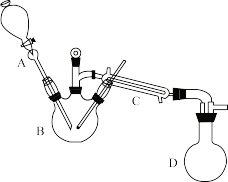
I.在三颈烧瓶中加入适量的乙醇,再缓慢加入浓硫酸,使其混合均好实验仪器。
II.通过仪器A向三颈烧瓶中加入乙醇和冰醋酸的混合液,小火加热至110~120℃,控制A中液体的滴速和馏出速率大致相等,滴加完毕后,继续加热15分钟。
II.依次用饱和Na2CO3溶液、饱和食盐水和饱和CaCl2溶液洗涤馏出液。
IV.分液,向分液后的有机层中加入无水氯化镁,静置,过滤除去氯化镁固体,进一步蒸馏纯化,收集馏分。
回答下列问题:
(1)仪器A和C的名称分别是_______ 、_______ ,冷水从C仪器_______ (填“上”或“下”)口进。
(2)反应发生装置B的加热方式是_______ ,为了减少产物乙酸乙酯的挥发,可以对仪器D采取的措施是_______ 。
(3)在加热反应过程中控制滴速和馏出速率大致相等的原因是_______ 。
(4)用饱和Na2CO3溶液洗涤时,反应的离子方程式为_______ 。
(5)用CaCl2溶液洗涤除去乙醇之前,先要用饱和食盐水洗涤,原因是_______ 。加入无水氯化镁的作用是_______ 。

I.在三颈烧瓶中加入适量的乙醇,再缓慢加入浓硫酸,使其混合均好实验仪器。
II.通过仪器A向三颈烧瓶中加入乙醇和冰醋酸的混合液,小火加热至110~120℃,控制A中液体的滴速和馏出速率大致相等,滴加完毕后,继续加热15分钟。
II.依次用饱和Na2CO3溶液、饱和食盐水和饱和CaCl2溶液洗涤馏出液。
IV.分液,向分液后的有机层中加入无水氯化镁,静置,过滤除去氯化镁固体,进一步蒸馏纯化,收集馏分。
回答下列问题:
(1)仪器A和C的名称分别是
(2)反应发生装置B的加热方式是
(3)在加热反应过程中控制滴速和馏出速率大致相等的原因是
(4)用饱和Na2CO3溶液洗涤时,反应的离子方程式为
(5)用CaCl2溶液洗涤除去乙醇之前,先要用饱和食盐水洗涤,原因是
21-22高三下·安徽·阶段练习
类题推荐
间溴苯甲醛常用作医药中间体,实验室以苯甲醛为原料,在无水AlCl3催化下加热制备间溴苯甲醛。
I.催化剂的制备
如图是实验室制取少量无水AlCl3的相关实验装置。已知无水氯化铝易升华,极易潮解。

(1)若气体A是Cl2,且由KMnO4和浓盐酸反应制取,该反应的离子方程式为___________ 。
(2)若气体A为Cl2,乙中的药品是碱石灰,则碱石灰的作用是___________ 。
II.间溴苯甲醛的制备
实验所用装置如图 (夹持及加热装置已省略),已知相关物质的沸点如下表所示:
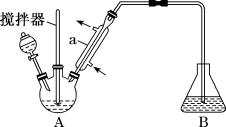
实验步骤如下:
步骤1:将一定配比的无水AlCl3、1,2-二氯乙烷和苯甲醛在三颈烧瓶中充分混合后,升温至60℃,缓慢滴加经浓硫酸干燥过的液溴,维持温度不变,反应一段时间后,冷却。
步骤2:将反应混合物缓慢加入一定量的稀盐酸中,搅拌、静置、分液。有机相用10% NaHCO3溶液洗涤。
步骤3:往洗涤后的有机相中加入适量无水MgSO4固体,放置一段时间后,进行下一操作。
步骤4:减压蒸馏有机相,收集相应馏分。
(3)仪器a的名称为___________ ,本实验需要控制反应温度为60℃,为了更好地控制反应温度。宜采用的加热方式是___________ 。
(4)步骤2分液时有机相处于___________ (填“上层”或“下层”),NaHCO3可以除去有机相中的Br2,反应中1mol Br2参与反应,转移1mol电子且产生无色气体,反应的离子方程式为___________ 。
(5)步骤3中加入无水MgSO4固体的作用是___________ 。
I.催化剂的制备
如图是实验室制取少量无水AlCl3的相关实验装置。已知无水氯化铝易升华,极易潮解。

(1)若气体A是Cl2,且由KMnO4和浓盐酸反应制取,该反应的离子方程式为
(2)若气体A为Cl2,乙中的药品是碱石灰,则碱石灰的作用是
II.间溴苯甲醛的制备
实验所用装置如图 (夹持及加热装置已省略),已知相关物质的沸点如下表所示:
| 物质 | 液溴 | 苯甲醛 | 1,2-二氯乙烷 | 间溴苯甲醛 |
| 沸点/℃ | 58.8 | 179 | 83.5 | 229 |

实验步骤如下:
步骤1:将一定配比的无水AlCl3、1,2-二氯乙烷和苯甲醛在三颈烧瓶中充分混合后,升温至60℃,缓慢滴加经浓硫酸干燥过的液溴,维持温度不变,反应一段时间后,冷却。
步骤2:将反应混合物缓慢加入一定量的稀盐酸中,搅拌、静置、分液。有机相用10% NaHCO3溶液洗涤。
步骤3:往洗涤后的有机相中加入适量无水MgSO4固体,放置一段时间后,进行下一操作。
步骤4:减压蒸馏有机相,收集相应馏分。
(3)仪器a的名称为
(4)步骤2分液时有机相处于
(5)步骤3中加入无水MgSO4固体的作用是
间溴苯甲醛常用作医药中间体,实验室以苯甲醛为原料,在无水AlCl3催化下加热制备间溴苯甲醛。
I.催化剂的制备
如图1是实验室制取少量无水AlCl3的相关实验装置。已知无水氯化铝易升华,极易潮解。
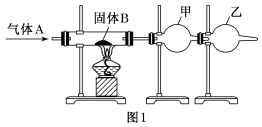
(1)若气体A是Cl2,且由KMnO4和浓盐酸反应制取,该反应的离子方程式为_______ 。
(2)若固体B是AlCl3·6H2O,则气体A是_______ ,通入气体A的目的是_______ 。
(3)若气体A为Cl2,乙中的药品是碱石灰,则碱石灰的作用是___________ 。
II.间溴苯甲醛的制备
实验所用装置如图2(夹持及加热装置已省略):
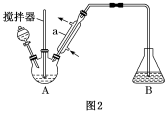
已知相关物质的沸点如下表所示:
实验步骤如下:
步骤1:将一定配比的无水AlCl3、1,2-二氯乙烷和苯甲醛在三颈烧瓶中充分混合后,升温至60℃,缓慢滴加经浓硫酸干燥过的液溴,维持温度不变,反应一段时间后,冷却。
步骤2:将反应混合物缓慢加入一定量的稀盐酸中,搅拌、静置、分液。有机相用10%NaHCO3溶液洗涤。
步骤3:往洗涤后的有机相中加入适量无水MgSO4固体,放置一段时间后,进行下一操作。
步骤4:减压蒸馏有机相,收集相应馏分。
(4)仪器a的名称为___________ ,本实验需要控制反应温度为60℃,为了更好地控制反应温度,宜采用的加热方式是___________ 。
(5)步骤2分液时有机相处于___________ (填“上层”或“下层”),NaHCO3可以除去有机相中的Br2,反应中1molBr2参与反应,转移1mol电子且产生无色气体,反应的离子方程式为_______ 。
(6)步骤3中将加入无水MgSO4固体的有机相放置一段时间后,进行的下一操作是_______ 。
I.催化剂的制备
如图1是实验室制取少量无水AlCl3的相关实验装置。已知无水氯化铝易升华,极易潮解。

(1)若气体A是Cl2,且由KMnO4和浓盐酸反应制取,该反应的离子方程式为
(2)若固体B是AlCl3·6H2O,则气体A是
(3)若气体A为Cl2,乙中的药品是碱石灰,则碱石灰的作用是
II.间溴苯甲醛的制备
实验所用装置如图2(夹持及加热装置已省略):

已知相关物质的沸点如下表所示:
| 物质 | 沸点/℃ |
| 液溴 | 58.8 |
| 苯甲醛 | 179 |
| 1,2-二氯乙烷 | 83.5 |
| 间溴苯甲醛 | 229 |
步骤1:将一定配比的无水AlCl3、1,2-二氯乙烷和苯甲醛在三颈烧瓶中充分混合后,升温至60℃,缓慢滴加经浓硫酸干燥过的液溴,维持温度不变,反应一段时间后,冷却。
步骤2:将反应混合物缓慢加入一定量的稀盐酸中,搅拌、静置、分液。有机相用10%NaHCO3溶液洗涤。
步骤3:往洗涤后的有机相中加入适量无水MgSO4固体,放置一段时间后,进行下一操作。
步骤4:减压蒸馏有机相,收集相应馏分。
(4)仪器a的名称为
(5)步骤2分液时有机相处于
(6)步骤3中将加入无水MgSO4固体的有机相放置一段时间后,进行的下一操作是
某化学兴趣小组用如下装置制备乙酸乙酯(夹持和加热装置省略)。
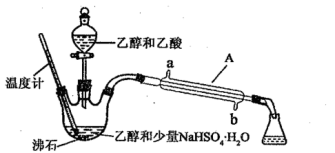
查阅资料可知:
(1)乙醇可以和氯化钙反应生成微溶于水的CaCl2•6C2H5OH
(2)相关物质的沸点(101kPa)、密度见下表:
其实验步骤如下,请回答:

查阅资料可知:
(1)乙醇可以和氯化钙反应生成微溶于水的CaCl2•6C2H5OH
(2)相关物质的沸点(101kPa)、密度见下表:
| 物质 | 乙醇 | 乙酸 | 乙酸乙酯 | 水 |
| 沸点/℃ | 78.3 | 117.9 | 77.1 | 100 |
| 密度/ | 0.785 | 1.049 | 0.901 | 0.997 |
| 1.打开分液漏斗活塞,滴入一部分混合液,小火加热进行蒸馏。 | (1)NaHSO4·H2O的作用是 |
| 2.当温度达到80℃时,蒸馏管口有液体流出,再从分液漏斗滴入剩余混合。液,维持反应温度在80~90℃之间,反应一段时间得到粗产品。 | (2)该实验中三颈烧瓶适宜的加热方式是 |
| 3.粗产品用饱和氯化钙溶液洗涤2次,分出酯层,再向酯层中加无水硫酸钠固体,过滤。 | (3)饱和氯化钙溶液的作用是 |
| 4.对滤液进行第二次蒸馏,收集相应温度的馏分。 | (4)收集馏分的适宜温度为 A.65~70℃ B.77~80℃ C.100~105℃ D.117~120℃ |
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


