解答题-原理综合题 较难0.4 引用5 组卷731
铁的腐蚀与防护与生产生活密切相关。
Ⅰ.研究铁的腐蚀
实验步骤如下:
步骤1:将铁粉放置于0.002
 溶液中浸泡,过滤后用水洗涤。
溶液中浸泡,过滤后用水洗涤。
步骤2:向15.00 mL 1 NaCl溶液(用盐酸调pH=1.78)中加入浸泡过的Fe粉。
NaCl溶液(用盐酸调pH=1.78)中加入浸泡过的Fe粉。
步骤3:采集溶液pH随时间变化的数据。
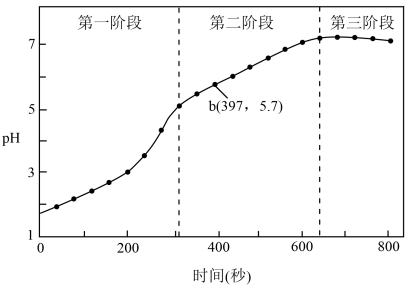
(1)第一阶段,主要发生析氢腐蚀,Cu上发生的电极反应为___________ 。
(2)第二、三阶段主要发生吸氧腐蚀。
①选取b点进行分析,经检验溶液中含有 ,写出Fe被腐蚀的总反应
,写出Fe被腐蚀的总反应___________ 。
②取b点溶液向其中滴加KSCN无明显现象,加入稀盐酸后立即变红。写出b点 被氧化的离子方程式
被氧化的离子方程式___________ 。
③依据b点发生的反应,分析第二阶段pH上升的原因是___________ 。
Ⅱ.研究铁的防护
(3)在铁表面镀锌可有效防止铁被腐蚀
已知: 放电的速率缓慢且平稳,有利于得到致密、细腻的镀层。
放电的速率缓慢且平稳,有利于得到致密、细腻的镀层。
①镀件Fe应与电源的___________ 相连。
②向 电解液中加入NaCN溶液,将
电解液中加入NaCN溶液,将 转化为
转化为 ,电解得到的镀层更加致密、细腻,原因是
,电解得到的镀层更加致密、细腻,原因是___________ 。
(4)电镀后的废水中含有 ,一种测定其含量的方法是:取废水50 mL,再加KI溶液1 mL,用c
,一种测定其含量的方法是:取废水50 mL,再加KI溶液1 mL,用c 
 溶液滴定,消耗
溶液滴定,消耗 溶液V mL。已知:
溶液V mL。已知: (无色)
(无色)  ,
,
 。
。
①滴定终点的现象是___________ 。
②废水中 的含量是
的含量是___________  (填计算式)。
(填计算式)。
Ⅰ.研究铁的腐蚀
实验步骤如下:
步骤1:将铁粉放置于0.002
步骤2:向15.00 mL 1
步骤3:采集溶液pH随时间变化的数据。

(1)第一阶段,主要发生析氢腐蚀,Cu上发生的电极反应为
(2)第二、三阶段主要发生吸氧腐蚀。
①选取b点进行分析,经检验溶液中含有
②取b点溶液向其中滴加KSCN无明显现象,加入稀盐酸后立即变红。写出b点
③依据b点发生的反应,分析第二阶段pH上升的原因是
Ⅱ.研究铁的防护
(3)在铁表面镀锌可有效防止铁被腐蚀
已知:
①镀件Fe应与电源的
②向
(4)电镀后的废水中含有
①滴定终点的现象是
②废水中
2022·北京丰台·一模
类题推荐
铁的腐蚀和防护与生产生活密切相关。已知:氢氧化物沉淀的 如下表(开始沉淀时金属离子浓度为
如下表(开始沉淀时金属离子浓度为 )。
)。
(1)研究铁的腐蚀。将一定量铁粉和碳粉混合后置于一密闭容器中,加入 和盐酸的混合溶液。测得溶液
和盐酸的混合溶液。测得溶液 和压强随时间变化的曲线如所示。
和压强随时间变化的曲线如所示。
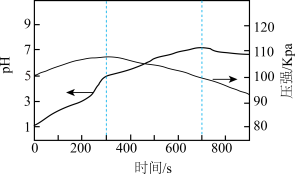
①容器内压强先增大后减小,除温度影响外的原因是_______ 。
②反应过程中,混合液里先期生成的 会被氧化生成
会被氧化生成 ,反应的离子方程式为
,反应的离子方程式为_______ 。
③ 后
后 略下降,原因是
略下降,原因是_______ 。
(2)研究铁的防护。
①在铁表面镀锌可有效防止铁被腐蚀。
已知:镀层金属析出缓慢、平稳时,镀层致密、细腻;溶液中 与
与 可发生反应:
可发生反应: 。以通入一定量
。以通入一定量 的
的 溶液为电镀液热镀锌,得到的镀层更加致密、细腻,原因是
溶液为电镀液热镀锌,得到的镀层更加致密、细腻,原因是_______ 。
②镀锌废液的回收。镀锌废液中含有 等阳离子。请设计利用该电镀废液回收
等阳离子。请设计利用该电镀废液回收 溶液的实验方案:
溶液的实验方案:_______ 。(实验中可选用试剂: 、
、 溶液、
溶液、 氨水)
氨水)
| 沉淀物 | |||
| 开始沉淀 | 1.1 | 5.8 | 5.9 |
| 完全沉淀 | 3.2 | 8.8 | 8.0 |

①容器内压强先增大后减小,除温度影响外的原因是
②反应过程中,混合液里先期生成的
③
(2)研究铁的防护。
①在铁表面镀锌可有效防止铁被腐蚀。
已知:镀层金属析出缓慢、平稳时,镀层致密、细腻;溶液中
②镀锌废液的回收。镀锌废液中含有
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网