填空题 适中0.65 引用1 组卷187
甲烷燃料电池采用铂为电极,作为化学电源进行电解实验
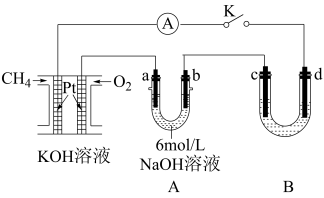
(1)写出燃料电池的正、负极反应式
负极:_______ ,
正极:_______ 。
(2)已知 A 中两个电极的材料分别为石墨和铁,用该装置可以制备高铁酸钾K2FeO4。资料显示: FeO 在溶液中呈紫红色。闭合 K,一段时间后,发现某电极附近溶液变成紫红色,该电极是
在溶液中呈紫红色。闭合 K,一段时间后,发现某电极附近溶液变成紫红色,该电极是_______ (填 a 或 b),该电极的电极反应式 为:_______ 。
(3)若 B 中的溶液为饱和 NaCl 溶液,用该装置模拟氯碱工业。
① 检验 c 电极产物的方法是:_______ 。
② 写出 d 电极的电极反应式:_______ 。
(4)若用 B 装置模拟工业粗铜精炼,则 c 极为_______ ,电解质溶液为_______ 。电解一段时间后, 电解液浓度_______ (填“变大” 、“不变”或“变小”);当燃料电池消耗标准状况下 O2的体积为 0.112L 时,理论上可以得到纯铜_______ g。

(1)写出燃料电池的正、负极反应式
负极:
正极:
(2)已知 A 中两个电极的材料分别为石墨和铁,用该装置可以制备高铁酸钾K2FeO4。资料显示: FeO
(3)若 B 中的溶液为饱和 NaCl 溶液,用该装置模拟氯碱工业。
① 检验 c 电极产物的方法是:
② 写出 d 电极的电极反应式:
(4)若用 B 装置模拟工业粗铜精炼,则 c 极为
21-22高二上·北京东城·阶段练习
类题推荐
为探究原电池和电解池的工作原理,某研究性学习小组分别用如图所示装置进行实验。
Ⅰ.用图1甲装置进行第一组实验:
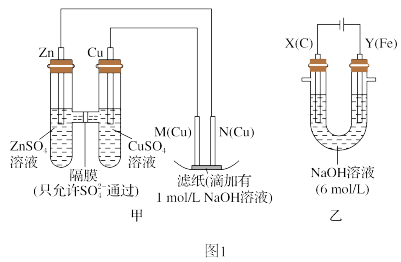
(1)实验过程中,
_______ (填“从左向右”、“从右向左”或“不”)移动。
(2)电极M处滤纸上可观察到的现象是_______ 。
(3)该小组同学用图1乙装置进行第二组实验时发现,两极均有气体产生,且Y极溶液逐渐变成紫红色,停止实验后观察到铁电极明显变细,电解液仍然澄清。查阅资料知,高铁酸根离子( )在溶液中呈紫红色。
)在溶液中呈紫红色。
①电解过程中,Y极发生的电极反应为 和
和_______ 。
②电解一段时间后,若在X极收集到672mL气体,Y电极(铁电极)质量减小0.28g,则在Y极收集到的气体体积为_______ mL(气体均为标准状况下的体积)。
Ⅱ.某同学设计如图2所示燃料电池探究氯碱工业原理和粗铜的精炼原理:
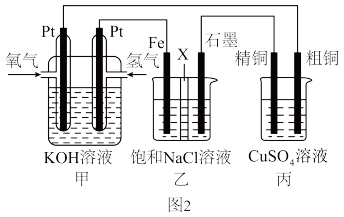
(4)下列说法正确的是_______(填字母)。
(5)如果粗铜中含有锌,银等杂质,丙装置中反应一段时间后,硫酸铜溶液浓度将_______ (填“增大”、“减小”或“不变”)。若在标准状况下,有224mL氧气参加反应,则丙装置中阴极析出铜的质量为_______ g。
Ⅲ.以铬酸钾( )为原料,用电化学法制备重铬酸钾的实验装置如图3所示(已知
)为原料,用电化学法制备重铬酸钾的实验装置如图3所示(已知
 ):
):
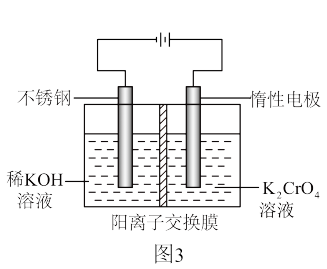
(6)分析阳极区能得到重铬酸钾溶液的原因_______ 。
(7)电解一段时间后,测得阳极区溶液中 物质的量由a mol变为b mol,则此时铬酸钾的转化率为
物质的量由a mol变为b mol,则此时铬酸钾的转化率为_______ 。
Ⅰ.用图1甲装置进行第一组实验:

(1)实验过程中,
(2)电极M处滤纸上可观察到的现象是
(3)该小组同学用图1乙装置进行第二组实验时发现,两极均有气体产生,且Y极溶液逐渐变成紫红色,停止实验后观察到铁电极明显变细,电解液仍然澄清。查阅资料知,高铁酸根离子(
①电解过程中,Y极发生的电极反应为
②电解一段时间后,若在X极收集到672mL气体,Y电极(铁电极)质量减小0.28g,则在Y极收集到的气体体积为
Ⅱ.某同学设计如图2所示燃料电池探究氯碱工业原理和粗铜的精炼原理:

(4)下列说法正确的是_______(填字母)。
| A.装置甲中通入氢气的电极为正极,装置乙中石墨电极为阳极 |
| B.装置甲中负极的电极反应式为 |
| C.反应一段时间后,在乙装置中滴入酚酞溶液,铁极区的溶液先变红 |
| D.若用隔膜法电解饱和食盐水生成NaClO,则X应为阳离子交换膜 |
Ⅲ.以铬酸钾(

(6)分析阳极区能得到重铬酸钾溶液的原因
(7)电解一段时间后,测得阳极区溶液中
如图所示,其中甲池的总反应为2CH3OH+3O2+4KOH=2K2CO3+6H2O,回答下问题:
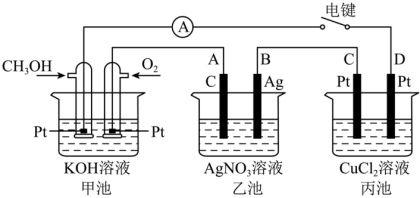
请回答下列问题:
(1)甲池为_______ (填“原电池”、“电解池”或“电镀池”),负极的电极反应式为_______ 。
(2)乙池A(石墨)电极的名称为_______ (填“正极”、“负极”、“阴极”或“阳极”),乙池中总反应式为_______ 。
(3)当乙池中B极质量增加5.40g时,甲池中理论上消耗O2的体积为_______ mL(标准状况下),丙池中析出_______ g铜。
(4)一段时间后,断开电键K。下列物质能使乙池恢复到反应前浓度的是_______(填选项字母)。
(5)若丙中电极不变,将其溶液换成含酚酞的NaCl溶液,电键闭合一段时间后,丙中D极附近观察到的现象是_______ ,溶液的pH将_______ (填“增大”、“减小”或“不变”)。C电极上的电极反应式为_______ ,检验该电极反应产物的方法是_______ 。
(6)若用丙装置电解精炼铜,粗铜(内含Zn、Fe、Ni等杂质)应该放在_______ (填C、D)极,电解进行一段时间后,电解质溶液中CuSO4的浓度将_______ (填“增大”、“减小”或“不变”)。

请回答下列问题:
(1)甲池为
(2)乙池A(石墨)电极的名称为
(3)当乙池中B极质量增加5.40g时,甲池中理论上消耗O2的体积为
(4)一段时间后,断开电键K。下列物质能使乙池恢复到反应前浓度的是_______(填选项字母)。
| A.Ag | B.Ag2O | C.AgOH | D.AgCl |
(6)若用丙装置电解精炼铜,粗铜(内含Zn、Fe、Ni等杂质)应该放在
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网



