解答题-实验探究题 适中0.65 引用1 组卷33
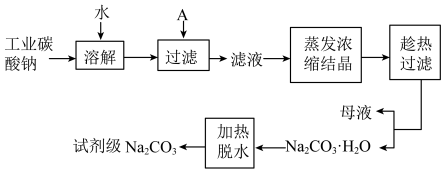
实验室设计了如下实验方案测定含有NaCl杂质的 样品含量
样品含量
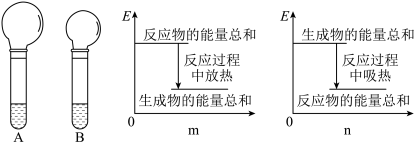
(1)【方案一】:用如图装置测定生成 气体的质量已确定含量你认为该方法测定结果将比真实值
气体的质量已确定含量你认为该方法测定结果将比真实值___________ (填“偏大”或“偏小”),理由: ___________

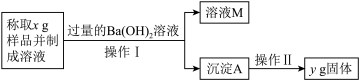
(2)【方案二】:用加热分解的方法测定碳酸氢钠的质量分数,样品中碳酸氢钠的质量分数可表示为:_____ (注意你的表达式中所用的有关符号的含义)
(1)【方案一】:用如图装置测定生成

(2)【方案二】:用加热分解的方法测定碳酸氢钠的质量分数,样品中碳酸氢钠的质量分数可表示为:
20-21高二上·上海徐汇·阶段练习
类题推荐
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网