解答题-结构与性质 较难0.4 引用10 组卷2778
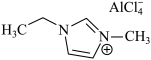
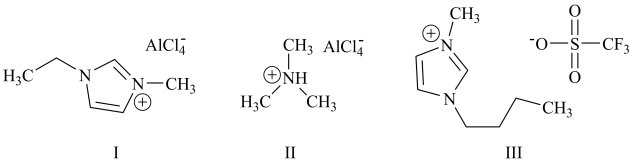
铝离子电池能量密度高、成本低且安全性高,是有前景的下一代储能电池。铝离子电池一般采用离子液体作为电解质,几种离子液体的结构如下。
(1)基态铝原子的核外电子排布式为___________ 。
(2)基态氮原子的价层电子排布图为___________(填编号)。
(3)化合物I中碳原子的杂化轨道类型为___________ ,化合物II中阳离子的空间构型为___________ 。
(4)化合物III中O、F、S电负性由大到小的顺序为___________ 。
(5)传统的有机溶剂大多易挥发,而离子液体有相对难挥发的优点,原因是___________ 。
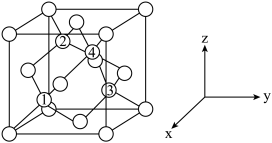
(6)铝离子电池的其中一种正极材料为AlMn2O4,其晶胞中铝原子的骨架如图所示。___________ 。
②以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子分数坐标,如图中原子1的坐标为( ,
, ,
, ),原子2的坐标为(
),原子2的坐标为( ,
, ,
, ),则原子3的坐标为
),则原子3的坐标为_____ 。
③已知该晶体属于立方晶系,晶胞参数为apm,阿伏加德罗常数的值为NA,则晶体的密度为______ g·cm-3(列出计算式)。
(1)基态铝原子的核外电子排布式为
(2)基态氮原子的价层电子排布图为___________(填编号)。
A.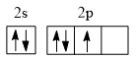 | B.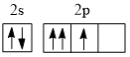 | C.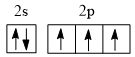 | D.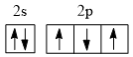 |
(4)化合物III中O、F、S电负性由大到小的顺序为
(5)传统的有机溶剂大多易挥发,而离子液体有相对难挥发的优点,原因是
(6)铝离子电池的其中一种正极材料为AlMn2O4,其晶胞中铝原子的骨架如图所示。
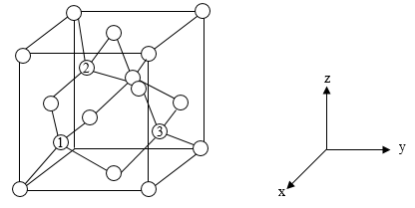
②以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子分数坐标,如图中原子1的坐标为(
③已知该晶体属于立方晶系,晶胞参数为apm,阿伏加德罗常数的值为NA,则晶体的密度为
2022·广东广州·一模
类题推荐
钠、镁、铝、铜及其化合物在生活中具有重要作用。回答下列问题:
(1)基态 的价层轨道表示式为
的价层轨道表示式为________ 。
(2)Na、Mg、Al的第一电离能从小到大的顺序为_______ (填元素符号)。
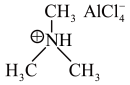
(3)铝离子电池一般采用离子液体作为电解质,某含铝离子液体的结构如图:_______ ;传统的有机溶剂大多易挥发,而离子液体相对难挥发,原因是________ 。
(4)几种氧化物的化学键中离子键成分的百分数和氧化物的熔点如下表:
离子键成分的百分数:MgO高于 ,其原因是
,其原因是_______ 。
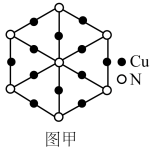
(5)氮、铜形成的某一种化合物 ,为立方晶系晶体,晶胞中氮原子只有一种位置,沿体对角线投影如图甲所示。
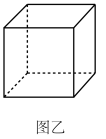
,为立方晶系晶体,晶胞中氮原子只有一种位置,沿体对角线投影如图甲所示。___ 个,请在图乙中画出该晶胞的结构示意图____ (○为N,●为Cu)已知晶胞中最近的两个Cu原子间距离为a pm,则晶体的密度为_____  (用含a、
(用含a、 的代数式表示)。
的代数式表示)。
(1)基态
(2)Na、Mg、Al的第一电离能从小到大的顺序为
(3)铝离子电池一般采用离子液体作为电解质,某含铝离子液体的结构如图:
(4)几种氧化物的化学键中离子键成分的百分数和氧化物的熔点如下表:
| 氧化物 | MgO | ||
| 离子键的百分数/% | 62 | 50 | 41 |
| 熔点/℃ | 1132 | 2852 | 2054 |
(5)氮、铜形成的某一种化合物
钠、镁、铝、铜及其化合物在生活中具有重要作用。回答下列问题:
(1)基态Cu+的价层轨道表示式为___________ 。
(2)Na、Mg、Al的第一电离能由大到小的顺序为___________ (填元素符号)。
(3)铝离子电池一般采用离子液体作为电解质,某含铝离子液体的结构如图:
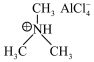
该化合物中阴离子的空间构型为___________ ;传统的有机溶剂大多易挥发,而离子液体相对难挥发,原因是___________ 。
(4)几种氧化物的化学键中离子键成分的百分数和氧化物的熔点如下表:
离子键成分的百分数:MgO高于Al2O3,其原因是___________ ;熔点:MgO高于Na2O,从结构的角度解释其原因是___________ 。
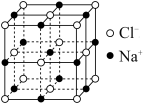
(5)NaCl的晶胞如图所示。NaCl的密度为ρ g/cm3,在NaCl晶体里Na+和Cl-的最短距离为apm,则阿伏加德罗常数的值为___________ (用含a、ρ的表达式表示)。
(1)基态Cu+的价层轨道表示式为
(2)Na、Mg、Al的第一电离能由大到小的顺序为
(3)铝离子电池一般采用离子液体作为电解质,某含铝离子液体的结构如图:

该化合物中阴离子的空间构型为
(4)几种氧化物的化学键中离子键成分的百分数和氧化物的熔点如下表:
| 氧化物 | Na2O | MgO | Al2O3 |
| 离子键的百分数/% | 62 | 50 | 41 |
| 熔点/℃ | 1132 | 2852 | 2054 |
(5)NaCl的晶胞如图所示。NaCl的密度为ρ g/cm3,在NaCl晶体里Na+和Cl-的最短距离为apm,则阿伏加德罗常数的值为

组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网