解答题-原理综合题 适中0.65 引用2 组卷97
碳和氮的氧化物等有害气体的处理成为科学研究的重要内容。
(1)用活性炭还原法处理氮氧化物。有关反应为:C(s)+2NO(g)⇌N2(g)+CO2(g)。某研究小组向一个容积不变的密闭容器(容器容积为3L,固体试样体积忽略不计)中加入NO和足量的活性炭,在恒温(T℃)条件下反应,测得不同时间(t)时各物质的物质的量(n)如表:
①10min-20min时间内,用v(NO)表示的反应速率为_______ 。
②T℃时,该反应的平衡常数为_______ (保留两位小数),若某-时刻,容器中有1.2molC、1.2molNO、0.75molN2和1.08molCO2,此时v(正)_______ v(逆)(填“>、<、=”)。
③下列各项能判断该反应达到平衡状态的是_______ 。
A.容器内压强保持不变 B.2v(NO)正=v(N2)逆
C.容器内CO2的体积分数不变 D.混合气体的密度保持不变
④一定温度下,随着NO的起始浓度增大,则NO的平衡转化率_______ (填“增大”、“不变”或“减小”)。
(2)在3L容积可变的密闭容器中发生反应H2(g)+CO2(g)⇌H2O(g)+CO(g),恒温下c(CO)随时间t变化的曲线I如图所示。若在t0时分别改变一个条件,曲线I变成曲线II和曲线III。
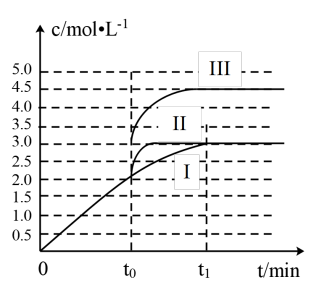
①当曲线I变成曲线II时,改变的条件是_______ ;
②当曲线I变成曲线III时,改变的条件及改变条件的变化量分别是_______ 。
(1)用活性炭还原法处理氮氧化物。有关反应为:C(s)+2NO(g)⇌N2(g)+CO2(g)。某研究小组向一个容积不变的密闭容器(容器容积为3L,固体试样体积忽略不计)中加入NO和足量的活性炭,在恒温(T℃)条件下反应,测得不同时间(t)时各物质的物质的量(n)如表:
 | NO | N2 | CO2 |
| 0 | 2.00 | 0 | 0 |
| 10 | 1.16 | 0.42 | 0.42 |
| 20 | 0.80 | 0.60 | 0.60 |
| 30 | 0.80 | 0.60 | 0.60 |
①10min-20min时间内,用v(NO)表示的反应速率为
②T℃时,该反应的平衡常数为
③下列各项能判断该反应达到平衡状态的是
A.容器内压强保持不变 B.2v(NO)正=v(N2)逆
C.容器内CO2的体积分数不变 D.混合气体的密度保持不变
④一定温度下,随着NO的起始浓度增大,则NO的平衡转化率
(2)在3L容积可变的密闭容器中发生反应H2(g)+CO2(g)⇌H2O(g)+CO(g),恒温下c(CO)随时间t变化的曲线I如图所示。若在t0时分别改变一个条件,曲线I变成曲线II和曲线III。

①当曲线I变成曲线II时,改变的条件是
②当曲线I变成曲线III时,改变的条件及改变条件的变化量分别是
21-22高二上·辽宁沈阳·阶段练习
类题推荐
用活性炭还原法处理氮氧化物,有关反应为C(s)+2NO(g) N2(g)+CO2(g)。某研究小组向某密闭的真空容器(假设容器体积不变,固体试样体积忽略不计)中加入NO和足量的活性炭,恒温(T1 ℃)条件下反应,反应进行到不同时间测得各物质的浓度如表:
N2(g)+CO2(g)。某研究小组向某密闭的真空容器(假设容器体积不变,固体试样体积忽略不计)中加入NO和足量的活性炭,恒温(T1 ℃)条件下反应,反应进行到不同时间测得各物质的浓度如表:
(1)10~20 min的时间段内,以CO2表示的反应速率为____________ 。
(2)写出该反应的平衡常数的表达式K=_________ 。
(3)下列各项能作为判断该反应达到平衡状态的是 。(填序号字母)
(4)30 min时改变某一条件,反应重新达到平衡,则改变的条件可能是_____________ 。
(5)一定温度下,随着NO的起始浓度增大,则NO的平衡转化率______ (填“增大”“不变”或“减小”)。
物 质 浓度/mol·L-1 时间/min | NO | N2 | CO2 |
| 0 | 1.00 | 0 | 0 |
| 10 | 0.58 | 0.21 | 0.21 |
| 20 | 0.40 | 0.30 | 0.30 |
| 30 | 0.40 | 0.30 | 0.30 |
| 40 | 0.32 | 0.34 | 0.17 |
| 50 | 0.32 | 0.34 | 0.17 |
(2)写出该反应的平衡常数的表达式K=
(3)下列各项能作为判断该反应达到平衡状态的是 。(填序号字母)
| A.容器内压强保持不变 |
| B.2v正(NO)=v逆(N2) |
| C.容器内CO2的体积分数不变 |
| D.混合气体的密度保持不变 |
(5)一定温度下,随着NO的起始浓度增大,则NO的平衡转化率
碳和氮是动植物体中的重要组成元素,向大气中过度排放二氧化碳会造成温室效应,氮氧化物会产生光化学烟雾,目前,这些有毒有害气体的处理成为科学研究的重要内容.
(1)用活性炭还原法处理氮氧化物.有关反应为:C(s)+2NO(g) N2(g)+CO2(g).
N2(g)+CO2(g).
某研究小组向一个容器容积为3L且容积不变的密闭真空容器(固体试样体积忽略不计)中加入NO和足量的活性炭,在恒温(T1℃)条件下反应,测得不同时间(t)时各物质的物质的量(n)如表:
①根据表中数据,计算T1℃时该反应的平衡常数为_____ (保留两位小数).若某一时刻,容器中有1.2molC、1.2molNO、0.75molN2和1.08molCO2,此时v(正)_____ v(逆)(填“>、<、=”)
②下列各项能判断该反应达到平衡状态的是_____ (填序号字母).
A.v(NO)(正)=2v(N2)(逆) B.容器内CO2和N2的体积比为1:1
C.混合气体的平均相对分子质量保持不变 D.容器内压强保持不变
③一定温度下,随着NO的起始浓度增大,则NO的平衡转化率_____ (填“增大”、“不变”或“减小”).
(2)在3L容积可变的密闭容器中发生上述反应:H2(g)+CO2(g) H2O(g)+CO(g),恒温下c(CO)随反应时间t变化的曲线Ⅰ如图所示.
H2O(g)+CO(g),恒温下c(CO)随反应时间t变化的曲线Ⅰ如图所示.
①若在t0时改变一个条件,使曲线Ⅰ变成曲线Ⅱ,则改变的条件是_____ ;
②若在t0时刻将容器体积快速压缩至2L(其他条件不变),请在图中画出c(CO)随反应时间t变化的曲线_____ .
(3)已知:CO(g)+H2O(g)⇌H2(g)+CO2(g)△H=﹣41.2kJ/mol,850℃时在一体积为10L的恒容密闭容器中,通入一定量的CO和H2O,CO和H2O浓度变化如图所示:下列说法正确的是_____ (填序号)

A.达到平衡时,氢气的物质的量是0.12mol
B.达到平衡时,反应体系最终会放出49.44kJ热量
C.第6min时,若升高温度,反应平衡常数会减小
D.第8min时,若充入氦气,会导致v正(CO)<v逆(H2O)
(4)850℃时,若在容积为2L的密闭容器中同时充入1.0mol CO,3.0mol H2O,amol CO2和bmol H2.若达平衡时各组分体积分数都与(3)中平衡时相同,则a=_____ mol,b=_____ mol.
(1)用活性炭还原法处理氮氧化物.有关反应为:C(s)+2NO(g)
某研究小组向一个容器容积为3L且容积不变的密闭真空容器(固体试样体积忽略不计)中加入NO和足量的活性炭,在恒温(T1℃)条件下反应,测得不同时间(t)时各物质的物质的量(n)如表:
| n/mol t/min | NO | N2 | CO2 |
| 0 | 2.00 | 0 | 0 |
| 10 | 1.16 | 0.42 | 0.42 |
| 20 | 0.80 | 0.60 | 0.60 |
| 30 | 0.80 | 0.60 | 0.60 |
②下列各项能判断该反应达到平衡状态的是
A.v(NO)(正)=2v(N2)(逆) B.容器内CO2和N2的体积比为1:1
C.混合气体的平均相对分子质量保持不变 D.容器内压强保持不变
③一定温度下,随着NO的起始浓度增大,则NO的平衡转化率
(2)在3L容积可变的密闭容器中发生上述反应:H2(g)+CO2(g)

①若在t0时改变一个条件,使曲线Ⅰ变成曲线Ⅱ,则改变的条件是
②若在t0时刻将容器体积快速压缩至2L(其他条件不变),请在图中画出c(CO)随反应时间t变化的曲线
(3)已知:CO(g)+H2O(g)⇌H2(g)+CO2(g)△H=﹣41.2kJ/mol,850℃时在一体积为10L的恒容密闭容器中,通入一定量的CO和H2O,CO和H2O浓度变化如图所示:下列说法正确的是

A.达到平衡时,氢气的物质的量是0.12mol
B.达到平衡时,反应体系最终会放出49.44kJ热量
C.第6min时,若升高温度,反应平衡常数会减小
D.第8min时,若充入氦气,会导致v正(CO)<v逆(H2O)
(4)850℃时,若在容积为2L的密闭容器中同时充入1.0mol CO,3.0mol H2O,amol CO2和bmol H2.若达平衡时各组分体积分数都与(3)中平衡时相同,则a=
氮是地球上含量丰富的一种元素,氮及其化合物在工农业生产、生活中有着重要作用。回答下列关于氮元素的有关问题。
(1)用CH4催化还原氮氧化物可以消除氮氧化物的污染。已知:
①CH4(g)+4NO2(g) =4NO(g) + CO2(g) +2H2O(g) ;△H= -574 kJ·mol-1
②CH4(g) +4NO(g) =2N2(g) + CO2(g) + 2H2O(g);△H= -1160 kJ·mol-1
③H2O(g) = H2O(l) ; △H= -44.0 kJ·mol-1
写出CH4(g)与NO2(g)反应生成N2(g)、CO2(g)和H2O(1)的热化学方程式___________ ,该反应的熵变△S_____ 0(填“>”、“<”、“="”" )。
(2)用活性炭还原法处理氮氧化物。有关反应为:C(s)+2NO(g) N2(g)+CO2(g) 。某研究小组向某密闭的真空容器(假设容器体积不变,固体试样体积忽略不计)中加入NO和足量的活性炭,恒温(T1℃)条件下反应,反应进行到不同时间测得各物质的浓度如右表:
N2(g)+CO2(g) 。某研究小组向某密闭的真空容器(假设容器体积不变,固体试样体积忽略不计)中加入NO和足量的活性炭,恒温(T1℃)条件下反应,反应进行到不同时间测得各物质的浓度如右表:
①10 min~20 min以v(CO2) 表示的反应速率为_____________ 。
②该反应的平衡常数的表达式为:K=_________ ,根据表中数据,计算T1℃时该反应的平衡常数为________ (保留两位小数)。
③下列各项能作为判断该反应达到平衡的是____ (填序号字母)。
a.容器内压强保持不变 b.2v (NO)(正)= v (N2)(逆)
c.容器内CO2的体积分数不变 d.混合气体的密度保持不变
④30 min后,改变某一条件,反应重新达到平衡,则改变的条件可能是______________ 。
⑤一定温度下,随着NO的起始浓度增大,则NO的平衡转化率________ (填“增大”、“不变”或“减小”) 。
(1)用CH4催化还原氮氧化物可以消除氮氧化物的污染。已知:
①CH4(g)+4NO2(g) =4NO(g) + CO2(g) +2H2O(g) ;△H= -574 kJ·mol-1
②CH4(g) +4NO(g) =2N2(g) + CO2(g) + 2H2O(g);△H= -1160 kJ·mol-1
③H2O(g) = H2O(l) ; △H= -44.0 kJ·mol-1
写出CH4(g)与NO2(g)反应生成N2(g)、CO2(g)和H2O(1)的热化学方程式
(2)用活性炭还原法处理氮氧化物。有关反应为:C(s)+2NO(g)
浓度/(mol/L) 时间/min | NO | N2 | CO2 |
| 0 | 1.00 | 0 | 0 |
| 10 | 0.58 | 0.21 | 0.21 |
| 20 | 0.40 | 0.30 | 0.30 |
| 30 | 0.40 | 0.30 | 0.30 |
| 40 | 0.32 | 0.34 | 0.17 |
| 50 | 0.32 | 0.34 | 0.17 |
①10 min~20 min以v(CO2) 表示的反应速率为
②该反应的平衡常数的表达式为:K=
③下列各项能作为判断该反应达到平衡的是
a.容器内压强保持不变 b.2v (NO)(正)= v (N2)(逆)
c.容器内CO2的体积分数不变 d.混合气体的密度保持不变
④30 min后,改变某一条件,反应重新达到平衡,则改变的条件可能是
⑤一定温度下,随着NO的起始浓度增大,则NO的平衡转化率
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


