解答题-实验探究题 适中0.65 引用1 组卷261
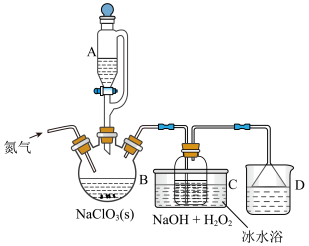
二氧化氯(ClO2)是一种高效消毒灭菌剂,可有效灭活新冠病毒,但其稳定性较差,故常采用H2O2和NaOH混合溶液将其吸收转化为NaClO2保存。现利用如下装置及试剂制备NaClO2。
已知:①ClO2的熔点为-59℃,沸点为11℃。纯ClO2易分解爆炸;ClO2极易溶于水,且在碱性环境中发生反应2ClO2+2OH-= +
+ +H2O。
+H2O。
②高于60℃时NaClO2分解成NaClO3和NaCl
回答下列问题:
(1)仪器A的名称是___________ ,其优点是___________ 。
(2)B为ClO2的发生装置,生成ClO2的离子方程式为___________ 。
(3)实验过程中持续通入N2的速度不能太快也不能太慢的原因是___________ ;实验室制取N2有多种方法,请根据元素化合物知识和氧化还原反应相关理论,结合下列供选试剂,选出一种可行的方法,化学方程式为___________ 。
可供选择的试剂:CuO(s)、NH3(g)、Cl2(g)、O2(g)、饱和NaNO2溶液、饱和NH4Cl溶液
(4)装置C需要采用冰水浴,可能的原因为___________ ;该装置中H2O2和NaOH需要按照一定比例加入,NaOH过量时导致的后果是___________ 。
(5)NaClO2饱和溶液在温度低于38℃时析出的晶体是NaClO2·3H2O,高于38℃时析出晶体是NaClO2。从NaClO2溶液中获得NaClO2固体的操作:
①减压,55℃蒸发结晶;②___________ ;③无水乙醇洗涤;④___________ ,得到成品。
(6)某同学根据“SO2+2OH-+H2O2= +2H2O”推测产品中含Na2SO4杂质,请设计简单实验证明:
+2H2O”推测产品中含Na2SO4杂质,请设计简单实验证明:___________ 。
已知:①ClO2的熔点为-59℃,沸点为11℃。纯ClO2易分解爆炸;ClO2极易溶于水,且在碱性环境中发生反应2ClO2+2OH-=
②高于60℃时NaClO2分解成NaClO3和NaCl

回答下列问题:
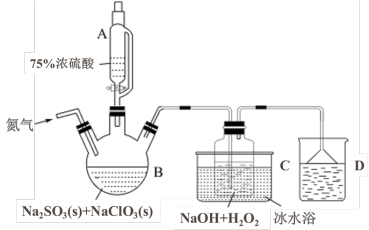
(1)仪器A的名称是
(2)B为ClO2的发生装置,生成ClO2的离子方程式为
(3)实验过程中持续通入N2的速度不能太快也不能太慢的原因是
可供选择的试剂:CuO(s)、NH3(g)、Cl2(g)、O2(g)、饱和NaNO2溶液、饱和NH4Cl溶液
(4)装置C需要采用冰水浴,可能的原因为
(5)NaClO2饱和溶液在温度低于38℃时析出的晶体是NaClO2·3H2O,高于38℃时析出晶体是NaClO2。从NaClO2溶液中获得NaClO2固体的操作:
①减压,55℃蒸发结晶;②
(6)某同学根据“SO2+2OH-+H2O2=
21-22高三下·广东·阶段练习
类题推荐
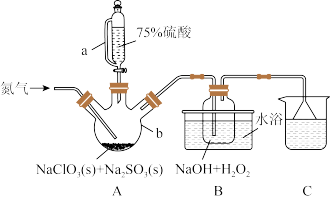
二氧化氯(ClO2)是一种高效消毒灭菌剂,可有效灭活新冠病毒,但其稳定性较差,故常采用H2O2和NaOH混合溶液将其吸收转化为NaClO2保存。现利用如下装置及试剂制备NaClO2。
已知:①ClO2的熔点为−59℃,沸点为11℃,纯的或浓度较大的ClO2易分解爆炸;ClO2极易溶于水。
②饱和NaClO2溶液中析出晶体成分与温度的关系如下表所示:
回答下列问题:
(1)仪器b的名称为___________ 使用a添加液体的优点___________ 。
(2)装置B水浴方式为___________ (填“冰水浴”或“80℃水浴”);其中生成NaClO2的离子方程式为___________ 。
(3)实验过程中持续通入N2的速度不能太慢也不能太快的原因是___________
(4)从NaClO2溶液中获得NaClO2固体的操作:
①减压,55℃蒸发结晶;②___________ ;③无水乙醇洗涤;④___________ ,得到成品。
(5)NaClO2,纯度的测定:称取ag产品配成250mL溶液,取25.00mL溶液,加入足量的KI溶液和稀硫酸(4H++ +4I-=2I2+Cl-+2H2O),充分反应后加入指示剂,用b mol∙L−1Na2S2O3标准溶液滴定至终点(I2+2
+4I-=2I2+Cl-+2H2O),充分反应后加入指示剂,用b mol∙L−1Na2S2O3标准溶液滴定至终点(I2+2 =2I-+
=2I-+ ),平均消耗标准溶液的体积为VmL,则产品中NaClO2,的质量分数是
),平均消耗标准溶液的体积为VmL,则产品中NaClO2,的质量分数是__________ (用含a、b、v的代数式表示)
已知:①ClO2的熔点为−59℃,沸点为11℃,纯的或浓度较大的ClO2易分解爆炸;ClO2极易溶于水。
②饱和NaClO2溶液中析出晶体成分与温度的关系如下表所示:
| 温度/℃ | <38 | 38~60 | >60 |
| 晶体成分 | NaClO2·3H2O | NaClO2 | NaClO2分解成NaClO3和NaCl |

回答下列问题:
(1)仪器b的名称为
(2)装置B水浴方式为
(3)实验过程中持续通入N2的速度不能太慢也不能太快的原因是
(4)从NaClO2溶液中获得NaClO2固体的操作:
①减压,55℃蒸发结晶;②
(5)NaClO2,纯度的测定:称取ag产品配成250mL溶液,取25.00mL溶液,加入足量的KI溶液和稀硫酸(4H++
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网