解答题-实验探究题 适中0.65 引用1 组卷45
物质的量是联系宏观和微观的桥梁,请回答下列问题:
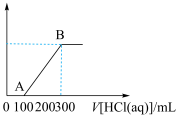
(1)将NaOH、 的固体混合物完全溶解于水,配制成溶液,然后向该溶液中逐滴加入
的固体混合物完全溶解于水,配制成溶液,然后向该溶液中逐滴加入 的盐酸,所加盐酸的体积与产生
的盐酸,所加盐酸的体积与产生 的体积(标准状况)关系如图所示,回答下列问题:
的体积(标准状况)关系如图所示,回答下列问题:
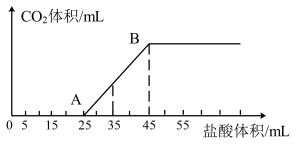
①AB段发生反应的离子方程式为_______ 。
②当加入35mL盐酸时,产生 的体积(标准状况)为
的体积(标准状况)为_______ mL。
③原混合溶液中NaOH与 的物质的量之比为
的物质的量之比为_______ 。
(2)用质量分数为98%的浓硫酸(密度为 )配制成
)配制成 的稀硫酸。现实验室仅需要这种硫酸220mL,试回答下列问题:
的稀硫酸。现实验室仅需要这种硫酸220mL,试回答下列问题:
①经计算,浓硫酸的浓度为_______  。
。
②本实验必须用到的仪器有量筒、烧杯、玻璃棒、_______ 、_______ 。
③若出现以下情况,对所配溶液浓度有何影响?(填“偏高”、“偏低”或“无影响”)
Ⅰ.没有用蒸馏水洗涤烧杯和玻璃棒_______ 。
Ⅱ.定容后塞上瓶塞反复摇匀,静置后,液面低于刻度线,再加水至刻度线_______ 。
(1)将NaOH、

①AB段发生反应的离子方程式为
②当加入35mL盐酸时,产生
③原混合溶液中NaOH与
(2)用质量分数为98%的浓硫酸(密度为
①经计算,浓硫酸的浓度为
②本实验必须用到的仪器有量筒、烧杯、玻璃棒、
③若出现以下情况,对所配溶液浓度有何影响?(填“偏高”、“偏低”或“无影响”)
Ⅰ.没有用蒸馏水洗涤烧杯和玻璃棒
Ⅱ.定容后塞上瓶塞反复摇匀,静置后,液面低于刻度线,再加水至刻度线
21-22高一下·黑龙江齐齐哈尔·开学考试
类题推荐
下图是某浓盐酸试剂瓶标签上的内容:
回答下列问题:
(1)实验室需用1.0mol/L的稀盐酸250mL,若用该浓盐酸配制,则用量筒量取浓盐酸的体积是_______ mL。配制过程所需玻璃仪器,除量筒、烧杯、玻璃棒外还需_______ (填仪器名称)。
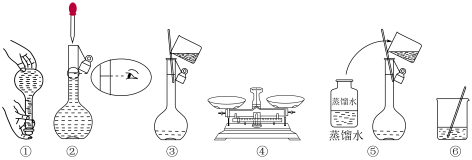
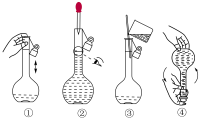
(2)下列使用容量瓶的操作正确的是_______(填标号)。
(3)若出现以下情况,对所配溶液的浓度将有何影响?(填“偏高”“偏低”或“无影响”)。
①用量筒量取浓盐酸时俯视观察凹液面_______ 。
②量取浓盐酸后用蒸馏水洗涤量筒并将洗涤液注入容量瓶_______ 。
③定容时,加蒸馏水不慎超过刻度线,再用胶头滴管吸出多余溶液_______ 。
(4)某种胃药的有效成分为碳酸钙,用所配制的稀盐酸溶液测定其中碳酸钙的含量,操作如下(设该药片中的其他成分不与盐酸或氢氧化钠反应):
①向一粒研碎后的药品(1.0g)中加入20.00mL蒸馏水
②加入 稀盐酸
稀盐酸
③用 溶液中和过量的稀盐酸,消耗NaOH溶液的体积为13.00mL
溶液中和过量的稀盐酸,消耗NaOH溶液的体积为13.00mL
根据上述实验步骤,计算这种药片中碳酸钙的质量分数为_______ 。
| 盐酸 分子式:HCl 相对分子质量:36.5 密度: HCl的质量分数:36.5% |
(1)实验室需用1.0mol/L的稀盐酸250mL,若用该浓盐酸配制,则用量筒量取浓盐酸的体积是
(2)下列使用容量瓶的操作正确的是_______(填标号)。
A. | B. | C. | D.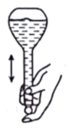 |
①用量筒量取浓盐酸时俯视观察凹液面
②量取浓盐酸后用蒸馏水洗涤量筒并将洗涤液注入容量瓶
③定容时,加蒸馏水不慎超过刻度线,再用胶头滴管吸出多余溶液
(4)某种胃药的有效成分为碳酸钙,用所配制的稀盐酸溶液测定其中碳酸钙的含量,操作如下(设该药片中的其他成分不与盐酸或氢氧化钠反应):
①向一粒研碎后的药品(1.0g)中加入20.00mL蒸馏水
②加入
③用
根据上述实验步骤,计算这种药片中碳酸钙的质量分数为
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网