单选题 适中0.65 引用1 组卷297
下列说法错误的是

| A.在25℃和101kPa时,1moL |
| B.已知冰的熔化热为6.0 |
| C.中和反应反应热的测定,需要测量三次温度,第三次测量反应后体系的最高温度 |
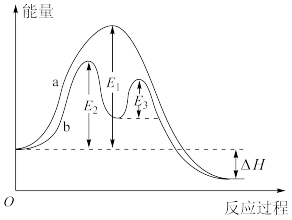
| D.某反应过程能量变化如图,b为在有催化剂作用下的反应过程 |
21-22高三上·天津·期末
类题推荐
下列说法不正确 的是
| A.已知冰的熔化热为6.0kJ/mol,冰中氢键键能为20kJ/mol,假设1mol冰中有2mol氢键,且熔化热完全用于破坏冰的氢键,则最多只能破坏冰中15%的氢键 |
| B.已知H+(aq)+OH-(aq)=H2O(l) ΔH=-57.3kJ/mol,则HCl和NH3·H2O反应生成1molH2O(1)时放出热量大于57.3kJ |
| C.已知:正丁烷(g)=异丁烷(g)△H<0,则异丁烷比正丁烷稳定 |
| D.可以通过测定C(石墨,s)和CO(g)的燃烧热间接计算C(石墨,s)+ |
下列说法正确的是

| A.已知2C(s)+2O2(g)=2CO2(g) ∆H1;2C(s)+O2(g)=2CO(g) ∆H2,则∆H1>∆H2 |
| B.已知冰的熔化热为6.0 kJ·mol-1,冰中氢键键能为20.0 kJ·mol-1,假设1 mol冰中有2 mol氢键,且熔化热完全用于破坏冰中的氢键,则最多只能破坏1 mol冰中5%氢键 |
| C.已知H+(aq)+OH-(aq)=H2O(l) ∆H=-57.3kJ/mol则1mol强酸的稀溶液与足量的强碱反应放出热量均为 |
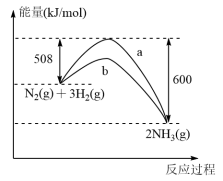
| D.如图,可知b为加入催化剂后的能量变化,正反应活化能比逆反应活化能低 |
下列说法错误的是
| A.已知冰的熔化热为6.0 kJ⋅mol |
| B.已知一定温度下,醋酸溶液的物质的量浓度为c,若加水稀释,则 |
| C.甲烷的燃烧热为890.3 kJ⋅mol |
| D.500℃、30MPa下,将0.5 mol |
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


