解答题-原理综合题 适中0.65 引用2 组卷706
利用CO2可合成尿素、醇等系列重要化工原料。回答下列有关问题:
(1)以CO2和NH3为原料合成尿素是利用CO2的成功范例。在尿素合成塔中的主要反应可表示如下:
反应1:2NH3(g)+CO2(g) NH2CO2NH4(s) △H1=-159.47kJ·mol-1
NH2CO2NH4(s) △H1=-159.47kJ·mol-1
反应2:NH2CO2NH4(s) CO(NH2)2(s)+H2O(g) △H2=+72.49kJ·mol-1
CO(NH2)2(s)+H2O(g) △H2=+72.49kJ·mol-1
反应3:2NH3(g)+CO2(g) CO(NH2)2(s)+H2O(g) △H3
CO(NH2)2(s)+H2O(g) △H3
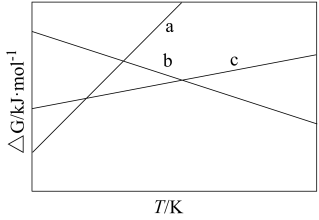
反应1、2和3的△G(自由能变化)随温度的变化关系如图所示。图中对应于反应3的线条是____ 。提高尿素产率的方法有____ 、____ 。____ (用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。以惰性电极电解尿素[CO(NH2)2]的碱性溶液,阳极有N2产生,写出阳极的电极反应方程式____ 。
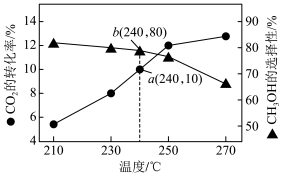
(2)工业上利用CO2可以制备甲醇,某一刚性容器中充入1molCO2和3molH2,在催化剂存在的条件下进行反应,测得温度与平衡转化率、产物选择性的关系如图所示。 CH3OH(g)+H2O(g) △H1
CH3OH(g)+H2O(g) △H1
反应2:CO2(g)+H2(g) CO(g)+H2O(g) △H2
CO(g)+H2O(g) △H2
已知:CH3OH选择性= ,反应1为
,反应1为____ (填“放热”或“吸热”)反应,有研究表明,在原料气中掺入适量的CO有利于提高CH3OH选择性,说明其可能的原因是____ ,有利于提高CH3OH选择性反应条件还可以是____ (填标号)。
A.高温高压 B.高温低压 C.低温高压 D.低温低压
(1)以CO2和NH3为原料合成尿素是利用CO2的成功范例。在尿素合成塔中的主要反应可表示如下:
反应1:2NH3(g)+CO2(g)
反应2:NH2CO2NH4(s)
反应3:2NH3(g)+CO2(g)
反应1、2和3的△G(自由能变化)随温度的变化关系如图所示。图中对应于反应3的线条是
(2)工业上利用CO2可以制备甲醇,某一刚性容器中充入1molCO2和3molH2,在催化剂存在的条件下进行反应,测得温度与平衡转化率、产物选择性的关系如图所示。
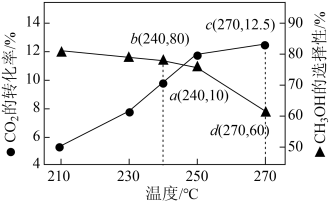
反应2:CO2(g)+H2(g)
已知:CH3OH选择性=
A.高温高压 B.高温低压 C.低温高压 D.低温低压
2022·山东济宁·一模
类题推荐
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网